Clear Sky Science · es
Fragmentos de SLIT3 orquestan la expansión neurovascular y la termogénesis en el tejido adiposo marrón
Cómo la “grasa buena” de nuestro cuerpo nos ayuda a mantener el calor
Cuando entramos en un ambiente frío, nuestro organismo se pone en marcha para conservar la temperatura. Un actor clave en esta respuesta es la grasa parda, un tipo especial de tejido adiposo que quema calorías para generar calor. Este estudio revela cómo la grasa parda organiza sus pequeños vasos sanguíneos y fibras nerviosas para aumentar la producción de calor, desvelando un sistema de comunicación oculto que algún día podría explotarse para mejorar el metabolismo y tratar enfermedades relacionadas con la obesidad.
Una caldera oculta dentro del cuerpo
El tejido adiposo marrón, o grasa parda, funciona como una caldera interna. A diferencia de la grasa blanca, que almacena energía, la grasa parda consume combustible para generar calor cuando nos exponemos al frío. Para hacerlo de forma eficiente, las células de la grasa parda necesitan un abundante suministro sanguíneo que aporte oxígeno y nutrientes, y una densa red de nervios simpáticos que indiquen cuándo aumentar la producción de calor. En el frío, estos vasos y nervios se expanden de manera notable. Sin embargo, hasta ahora no quedaba claro cómo coordinaban su crecimiento con tanta precisión las distintas partes del tejido.
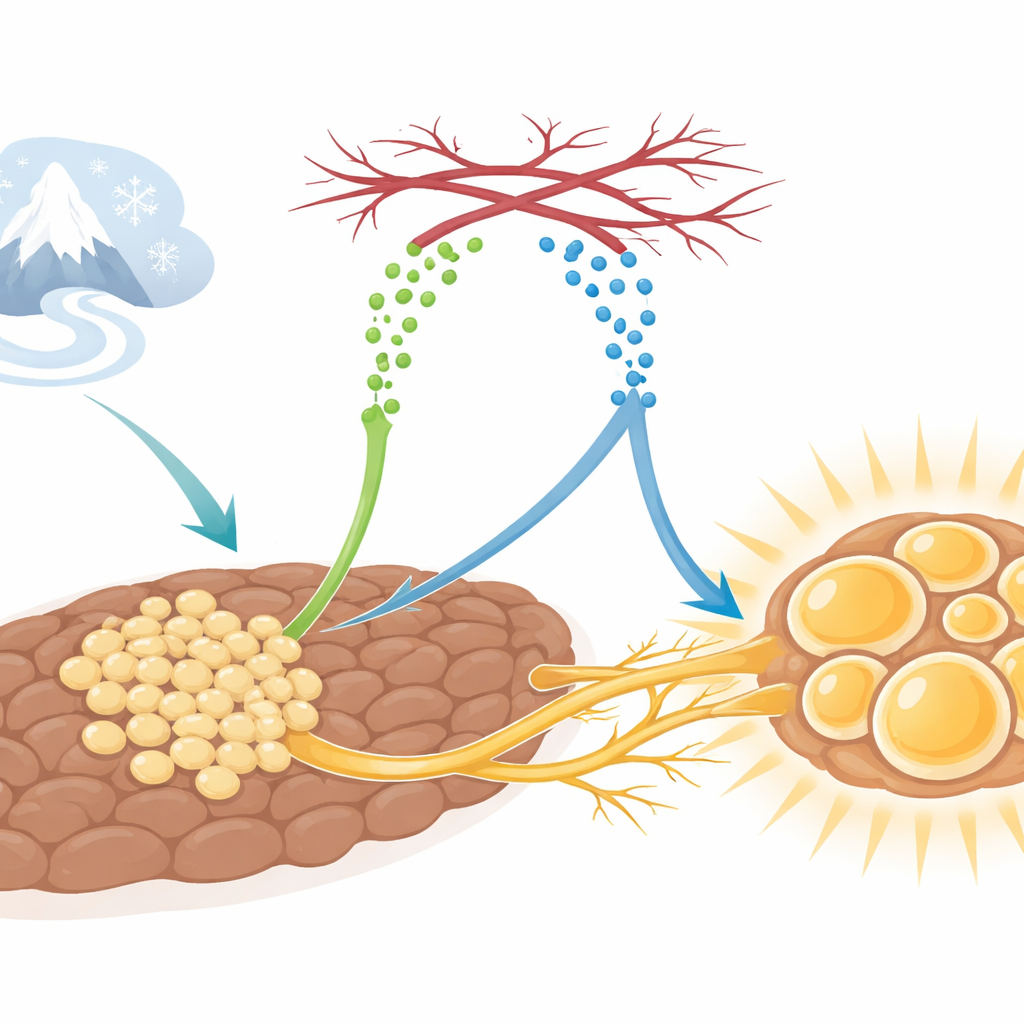
La molécula mensajera que lo pone en marcha
Los investigadores descubrieron que una proteína llamada SLIT3, producida por células inmaduras del tejido adiposo conocidas como progenitores adipocitarios, es central para esta coordinación. En ratones expuestos al frío, los niveles de SLIT3 en la grasa parda aumentan. Cuando el equipo bloqueó SLIT3 específicamente en la grasa parda o en estos progenitores, los animales tuvieron dificultades para mantener la temperatura corporal en el frío. Su grasa parda se volvió más “blanca”, con gotas lipídicas más grandes, menor expresión de genes termogénicos como Ucp1 y reducción del gasto energético, aunque la ingesta de alimento y los niveles de actividad no cambiaron. Esto situó a SLIT3 como un organizador clave de la respuesta de la grasa parda al frío, no tanto modificando la maquinaria intracelular de cada célula, sino dando forma al entorno tisular circundante.
Construyendo vasos y cables nerviosos juntos
Al investigar más a fondo, los científicos hallaron que la grasa parda sin SLIT3 tenía menos capilares y menos fibras nerviosas simpáticas recorriendo el tejido. La imagen tridimensional confirmó que la red nerviosa era marcadamente más escasa. Importante: cuando la señal nerviosa habitual se evitó mediante un fármaco que activa directamente la grasa parda, las células respondieron con normalidad. Esto mostró que SLIT3 no es necesario para que las células grasas consuman combustible, sino para construir el “cableado” neurovascular que permite al cerebro controlarlas. El equipo identificó a los progenitores adipocitarios como la principal fuente local de SLIT3 y demostró que eliminar SLIT3 sólo en estas células era suficiente para atenuar el crecimiento de vasos, el crecimiento nervioso y la producción de calor durante la exposición al frío.
Una proteína, dos fragmentos, dos funciones
SLIT3 no actúa como una señal única y estática. Los investigadores mostraron que una enzima llamada BMP1 corta SLIT3 en dos fragmentos separados con roles distintos. El fragmento N-terminal (SLIT3-N) estimula principalmente el crecimiento de los capilares, actuando a través de receptores en las células endoteliales que recubren los vasos sanguíneos. El fragmento C-terminal (SLIT3-C) promueve sobre todo la expansión de los nervios simpáticos. Identificaron un receptor llamado PLXNA1 en las fibras nerviosas como un socio de unión directo para SLIT3-C, apoyado por ensayos bioquímicos de unión y modelos estructurales por ordenador. Cuando se redujo PLXNA1, se perdió la capacidad de SLIT3 o SLIT3-C para potenciar el crecimiento nervioso y elevar la temperatura de la grasa parda, y la densidad nerviosa global y los niveles de noradrenalina en el tejido cayeron bruscamente.
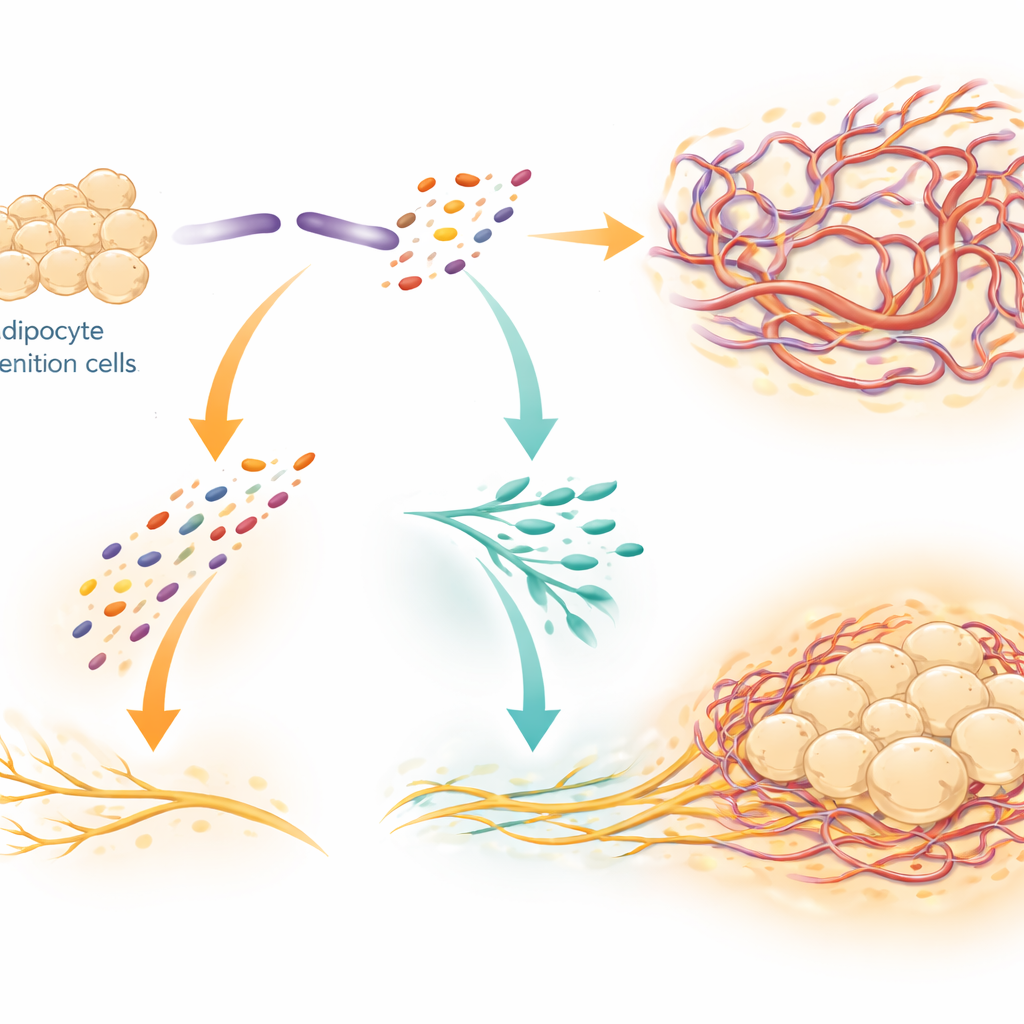
Vínculos con el metabolismo y la salud humana
Para explorar si este sistema tiene relevancia en humanos, los autores analizaron muestras de tejido adiposo de amplias cohortes de personas con obesidad. Una mayor expresión de SLIT3 en el tejido adiposo se asoció con perfiles más saludables: más de la hormona adiponectina, menos células inmunitarias inflamatorias en la grasa visceral, mejor control de la glucemia y niveles más altos de la adipocina beneficiosa omentina. Estudios genéticos en trabajos previos también han vinculado variantes cercanas a SLIT3 y su receptor PLXNA1 con obesidad y resistencia a la insulina. En conjunto, estos hallazgos sugieren que la vía de SLIT3 podría contribuir a mantener un tejido adiposo y un equilibrio metabólico saludables en humanos.
Qué significa esto para mantenerse caliente y saludable
En conjunto, el estudio revela que las células inmaduras del tejido adiposo en la grasa parda hacen más que convertirse en adipocitos maduros; esculpen activamente la red de soporte del tejido. Al liberar SLIT3 y permitir que se corte en dos fragmentos, impulsan de forma independiente pero sincronizada el crecimiento de vasos y nervios necesarios para una termogénesis eficaz. Este sistema de señalización “dos en uno” y finamente ajustado garantiza que la grasa parda pueda activarse rápidamente cuando el entorno exige más calor. A largo plazo, comprender y aprovechar con seguridad esta vía podría abrir nuevas vías para aumentar el consumo de energía, mejorar la salud del tejido adiposo y combatir las enfermedades metabólicas.
Cita: Serdan, T.D.A., Cervantes, H., Frank, B. et al. SLIT3 fragments orchestrate neurovascular expansion and thermogenesis in brown adipose tissue. Nat Commun 17, 2445 (2026). https://doi.org/10.1038/s41467-026-70310-9
Palabras clave: tejido adiposo marrón, termogénesis, remodelado neurovascular, señalización SLIT3, salud metabólica