Clear Sky Science · es
La activación de NF-κB en astrocitos perjudica la cicatrización tras una lesión cerebral traumática en ratones machos
Por qué las contusiones cerebrales no siempre cicatrizan de forma limpia
Cuando alguien recibe un golpe en la cabeza, la lesión visible en el exterior es solo parte de la historia. En lo profundo del cerebro se desplega una respuesta de curación compleja que puede determinar si una persona se recupera bien o desarrolla problemas persistentes de pensamiento, estado de ánimo o movimiento. Este estudio en ratones machos revela cómo una vía de estrés clave dentro de las células de soporte llamadas astrocitos puede convertir una respuesta de curación normal en una que en realidad agrava el daño tras una lesión cerebral traumática.
Los primeros intervinientes ocultos del cerebro
Los astrocitos son células con forma de estrella que rodean las neuronas y los vasos sanguíneos, ayudando a mantener estable el entorno interno del cerebro. Tras una lesión craneal, cambian rápidamente de forma y comportamiento, formando una barrera alrededor del área dañada y ayudando a reparar el tejido. Los investigadores se centraron en un interruptor molecular dentro de estas células llamado NF-κB, conocido por regular la inflamación en muchos tejidos. Se preguntaron si, después de una lesión de cráneo cerrado similar a las conmociones y contusiones humanas comunes, este interruptor ayuda o perjudica la capacidad del cerebro para sanar.
Un interruptor de estrés que se enciende tras el impacto
Al analizar la actividad génica en tejido cerebral de ratón después de la lesión, el equipo encontró un aumento de genes vinculados a la inflamación y a la señalización de NF-κB, especialmente entre los tres y siete días tras el trauma, cuando el daño secundario se intensifica. Utilizando ratones reporteros, mostraron que la activación de NF-κB no estaba difundida por todo el cerebro sino concentrada alrededor del sitio del impacto. Allí fue especialmente activa en la microglía (los centinelas inmunitarios del cerebro) y en los astrocitos que forman el borde de la herida. Ese momento y ubicación sugirieron que NF-κB en astrocitos podría ser un regulador crítico de cómo el cerebro organiza su cicatriz y controla la respuesta inmune.
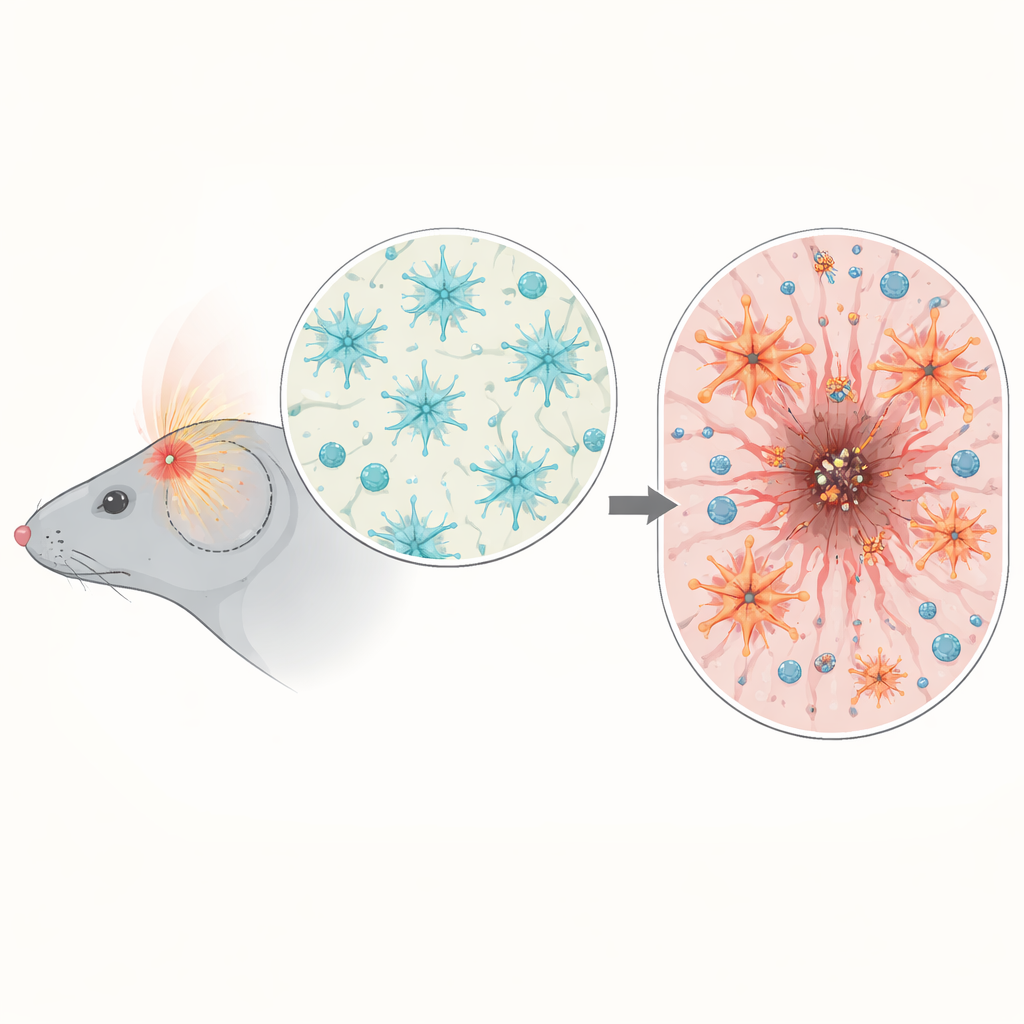
Exceso de activación de los astrocitos
Para probar la relación causal, los científicos diseñaron ratones en los que los astrocitos tenían la actividad de NF-κB artificialmente aumentada o reducida, pero solo después de completado el desarrollo cerebral. Cuando estos ratones sufrieron un trauma craneal, aquellos con NF-κB sobreactivado en astrocitos perdieron más peso, mostraron puntuaciones neurológicas tempranas peores y presentaron lesiones cerebrales más grandes y persistentes tanto en secciones de tejido como en exploraciones por resonancia magnética. En lugar de formar una cicatriz ordenada y bien definida que aislara el núcleo dañado, sus astrocitos produjeron un borde grueso y desorganizado que no logró reducir la herida con el tiempo. Se alteró el equilibrio normal de proteínas de matriz de soporte alrededor de la lesión y una estructura barrera externa clave, conocida como limitante glial, se formó pobremente, dejando el cerebro circundante menos protegido.
Cuando los programas de curación se descarrilan
Sumergiéndose en los detalles moleculares, el equipo aisló astrocitos y células inmunitarias cercanas para su análisis génico pormenorizado. En animales sanos, la lesión normalmente suprime algunas funciones celulares de mantenimiento de los astrocitos mientras activa genes que respaldan el cierre de heridas y la regeneración. En contraste, los astrocitos con NF-κB crónicamente activo ya parecían “lesionados” incluso antes del trauma, y tras el impacto no lograron activar completamente programas de reparación beneficiosos, como aquellos asociados a una transformación controlada que ayuda a las células a construir un borde eficaz. En su lugar, favorecieron fuertemente genes inflamatorios, adoptaron rasgos de un estado de astrocito tóxico vinculado al envejecimiento y a enfermedades neurodegenerativas, y mostraron signos de un perfil secretor tipo “senescencia” asociado a heridas crónicas y no resueltas.
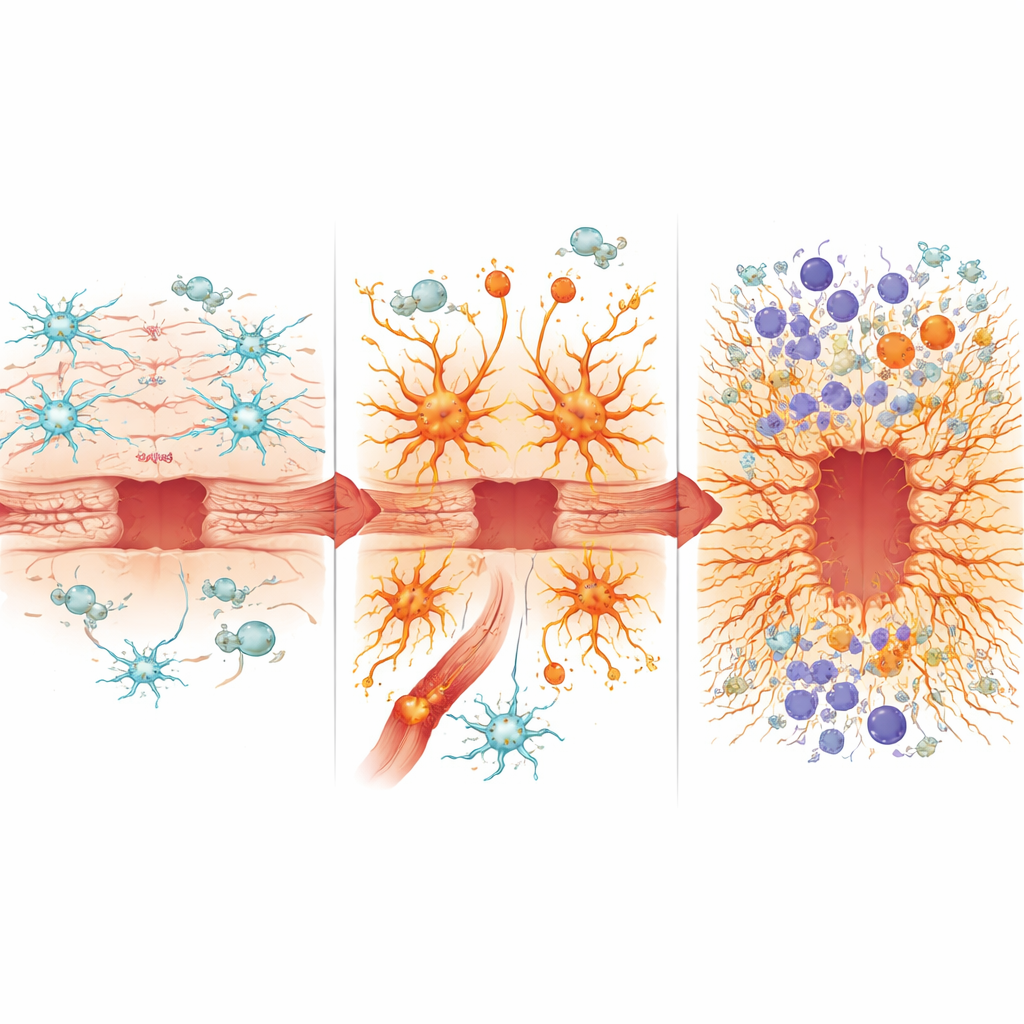
Avivando el fuego inmunitario
Estos astrocitos mal programados también remodelaron el paisaje inmune del cerebro. La barrera hematoencefálica se volvió más permeable, permitiendo la entrada de más células inmunitarias periféricas. Los ratones con NF-κB sobreactivado en astrocitos mostraron una infiltración mayor de células mieloides inflamatorias y mezclas alteradas de neutrófilos, monocitos y células dendríticas, así como un aumento de células T citotóxicas que pueden dañar aún más el tejido. Las células inmunitarias en este entorno expresaron señales más potentes impulsadas por vías de interferón e inflamasoma, ambas asociadas con inflamación agresiva y potencialmente neurotóxica. Al mismo tiempo, los niveles de varias proteínas protectoras o pro-reparadoras, como la osteopontina, se redujeron, mientras que otras vinculadas al estrés oxidativo, sobrecarga de hierro y formación de cicatrices, incluyendo hemo oxigenasa-1 y lipocalina-2, se elevaron. La proporción entre osteopontina y lipocalina-2 emergió como un marcador simple que se correspondía con una mejor o peor cicatrización en las distintas cepas de ratón.
Qué significa esto para la recuperación tras lesiones en la cabeza
En conjunto, los hallazgos muestran que cuando la vía de estrés NF-κB en astrocitos está crónicamente activada, estas células pasan de apoyar una reparación organizada a promover una cicatrización caótica y una inflamación prolongada. En lugar de construir un borde limpio que contenga el daño y permita la remodelación del tejido, contribuyen a crear un nicho filtrante e inflamatorio que agranda la lesión y compromete el resultado a largo plazo. Aunque el estudio se realizó en ratones machos, apunta a NF-κB en astrocitos como un objetivo prometedor para terapias destinadas a mejorar la recuperación tras una lesión cerebral traumática y sugiere que los niveles sanguíneos de moléculas como la osteopontina y la lipocalina-2 podrían, algún día, ayudar a los clínicos a controlar qué tan bien está sanando el cerebro de un paciente.
Cita: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Palabras clave: lesión cerebral traumática, astrocitos, neuroinflamación, formación de cicatriz cerebral, NF-kappa B