Clear Sky Science · es
NAA40 y NAC cooperan en la acetilación cotraduccional de histonas en humanos
Cómo las células afinan sus interruptores genéticos
Dentro de cada célula humana, las proteínas recién sintetizadas reciben pequeñas modificaciones químicas a medida que emergen de las máquinas ribosómicas que las fabrican. Estos ajustes diminutos pueden determinar a dónde va una proteína, cuánto tiempo dura y hasta cómo se activan o desactivan nuestros genes. Este artículo se centra en una proteína muy específica llamada NAA40 y en un complejo auxiliar denominado NAC, revelando cómo actúan conjuntamente en el ribosoma para modificar las histonas —los carretes alrededor de los que se enrolla el ADN— y, con ello, influir en la actividad génica y potencialmente en el desarrollo del cáncer.
Una pequeña tapa que cambia el comportamiento de las histonas
Muchas proteínas humanas reciben una pequeña «tapa» química en su extremo N-terminal, un proceso conocido como acetilación N-terminal. Las histonas H2A y H4, que ayudan a empaquetar el ADN en la cromatina, casi siempre llevan esta modificación. NAA40 es inusual entre las enzimas porque se especializa casi exclusivamente en añadir esta tapa a estas histonas mientras se están sintetizando. Esta marca de acetilación compite con otras señales químicas como la fosforilación y la metilación en la misma región de las histonas, por lo que la actuación (o no) de NAA40 puede alterar el grado de empaquetamiento del ADN y la regulación génica. De manera relevante, niveles alterados de NAA40 se han asociado con varios tipos de cáncer, lo que la convierte en un objetivo prometedor para nuevas terapias.
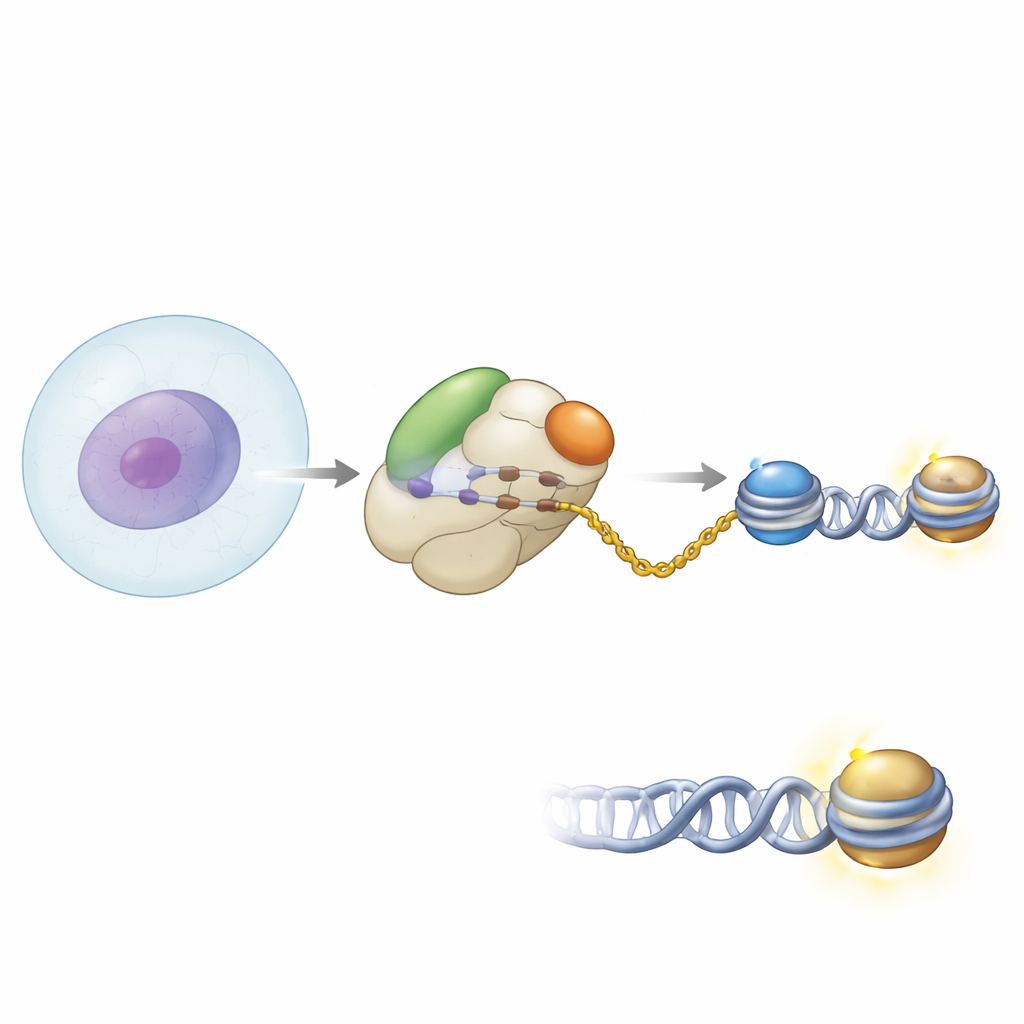
Asociación en la puerta de la fábrica de proteínas
Los autores usaron métodos bioquímicos y criomicroscopía electrónica de alta resolución para ver cómo se posiciona NAA40 en el ribosoma humano. Encontraron que NAA40 se sitúa justo en la salida del túnel por donde emergen las cadenas proteicas nacientes. Allí no actúa sola: se une junto al complejo asociado a polipéptidos nacientes, o NAC, un ayudante ribosómico frecuente que vigila las nuevas proteínas al salir. Las instantáneas estructurales mostraron a NAA40 anclada al ribosoma mediante un segmento helicoidal cargado positivamente en su extremo N-terminal, mientras que NAC se fija a la superficie ribosómica a través de una de sus subunidades. Un dominio flexible de NAC se extiende para contactar con NAA40, actuando como puente que aproxima la enzima al ribosoma.
Por qué NAC es necesario para la sintonía de histonas
Para probar la importancia de esta asociación, los investigadores reconstruyeron estas interacciones con componentes purificados en tubos de ensayo. Observaron que NAA40 por sí sola se une débilmente a los ribosomas, pero cuando NAC está presente la unión al ribosoma se vuelve mucho más fuerte. Si suprimen una región específica «UBA» de NAC que contacta con NAA40, esta unión potenciada desaparece. En células humanas, la depleción de NAC condujo a una reducción de la acetilación de H4 dependiente de NAA40 y a un aumento correspondiente de una marca de fosforilación rival en la misma cola de la histona. Este cambio se produjo sin alterar la cantidad o la ubicación de NAA40, lo que indica que la función principal de NAC es reclutar y posicionar correctamente a NAA40 en los ribosomas en traducción para que las histonas puedan modificarse de manera eficiente conforme se sintetizan.
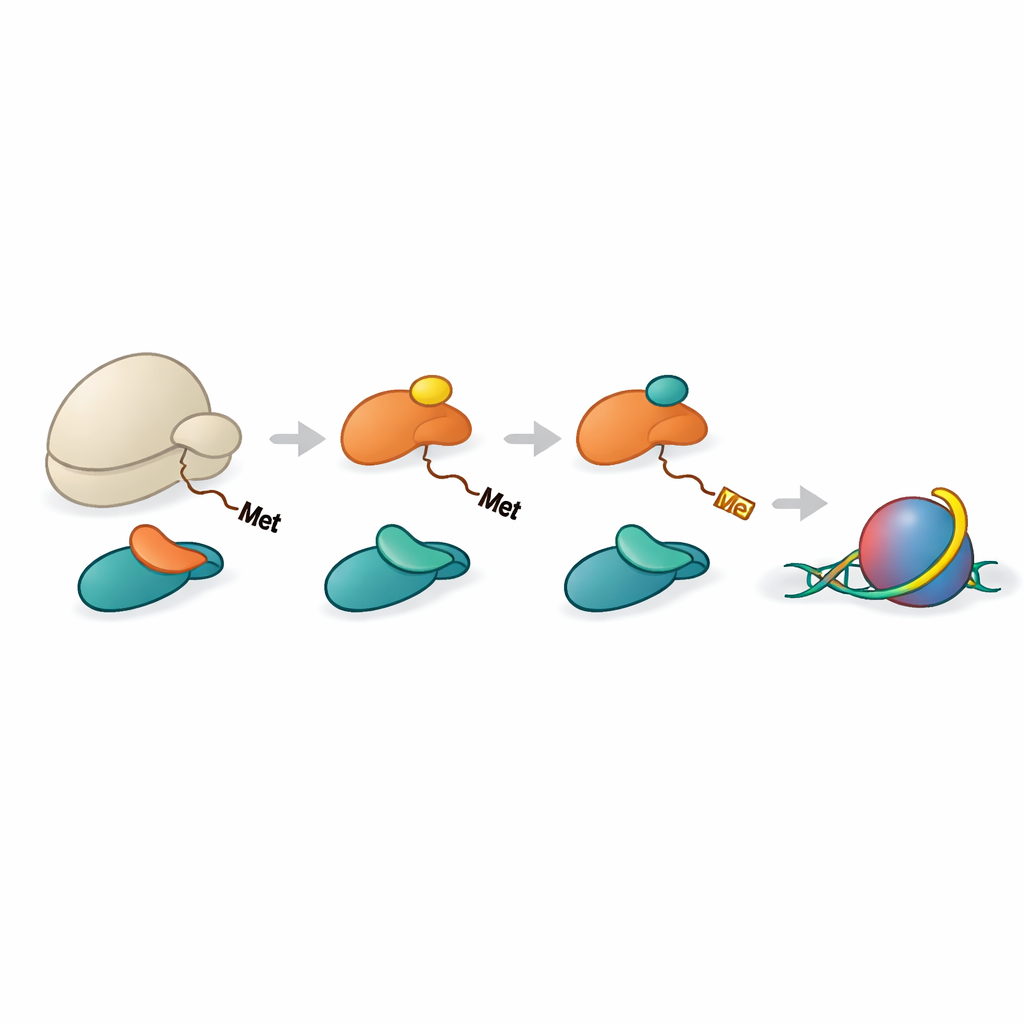
Una cadena de montaje coordinada para el procesado de histonas
Las histonas H2A y H4 deben perder primero su aminoácido metionina inicial antes de que NAA40 pueda reconocerlas. Otra enzima, METAP1, realiza este recorte. El equipo mostró que NAC puede ayudar a reunir a METAP1 y NAA40 en el ribosoma, formando una ensamblaje multienzimático en la salida peptídica. Estructuras de alta resolución de complejos reconstruidos revelaron a METAP1 y NAA40 unidos lado a lado en el ribosoma, con sus sitios activos posicionados a distancias casi iguales respecto al túnel de salida. Esta geometría permite que, una vez que la cola de la histona se extiende apenas una docena aproximada de aminoácidos más allá del ribosoma, METAP1 pueda eliminar la metionina inicial y NAA40 pueda añadir inmediatamente la tapa acetilo, minimizando cualquier demora entre ambos pasos.
Implicaciones para el control génico y el cáncer
En conjunto, el estudio demuestra que NAA40 no simplemente circula por la célula buscando histonas para modificar; en cambio, está acoplada al ribosoma por medio de NAC, formando parte de una estación de procesamiento organizada que prepara las histonas en el mismo momento en que se sintetizan. Al acoplar estrechamente la eliminación de la metionina y la adición de la acetilación, la célula asegura que H2A, H4 y la variante vinculada al daño del ADN H2A.X reciban rápidamente una marca de acetilación que puede moldear la estructura de la cromatina y la expresión génica. Dado que las perturbaciones en este paso temprano de marcaje de histonas pueden favorecer el crecimiento canceroso, entender la disposición precisa de NAA40, NAC y METAP1 en el ribosoma proporciona un plano estructural que podría guiar el diseño de fármacos destinados a modular este punto crítico de control epigenético.
Cita: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Palabras clave: acetilación de histonas, NAA40, ribosoma, complejo asociado a polipéptidos nacientes, regulación epigenética