Clear Sky Science · es
Una transición dependiente del ciclo celular de acetilación a fosforilación regula la maduración oportuna del centrosoma
Mantener nuestro cargamento genético en el camino
Cada vez que una célula de nuestro cuerpo se divide, debe repartir su ADN con una precisión exquisita. Cuando este proceso falla, las células pueden ganar o perder cromosomas, un estado peligroso vinculado al cáncer y a otras enfermedades. Este estudio descubre un dispositivo molecular de temporización que ayuda a las células a construir las diminutas estructuras necesarias para separar los cromosomas correctamente, revelando un posible punto débil que futuras terapias contra el cáncer podrían aprovechar.
Los pequeños centros de tráfico de la célula
En el corazón de cada célula en división se encuentran los centrosomas, pequeñas estructuras que actúan como centros de tráfico para las fibras que separan los cromosomas. Antes de que una célula entre en división, estos centros deben «madurar»: incrementan su contenido de proteínas auxiliares y se convierten en organizadores potentes de microtúbulos, las fibras dinámicas que forman el huso de división. Si esta maduración ocurre demasiado pronto, demasiado tarde o no ocurre, los cromosomas pueden distribuirse incorrectamente, conduciendo a células con un número anormal de cromosomas. Entender cómo las células activan los centrosomas en el momento justo ha sido una cuestión central en la biología celular.
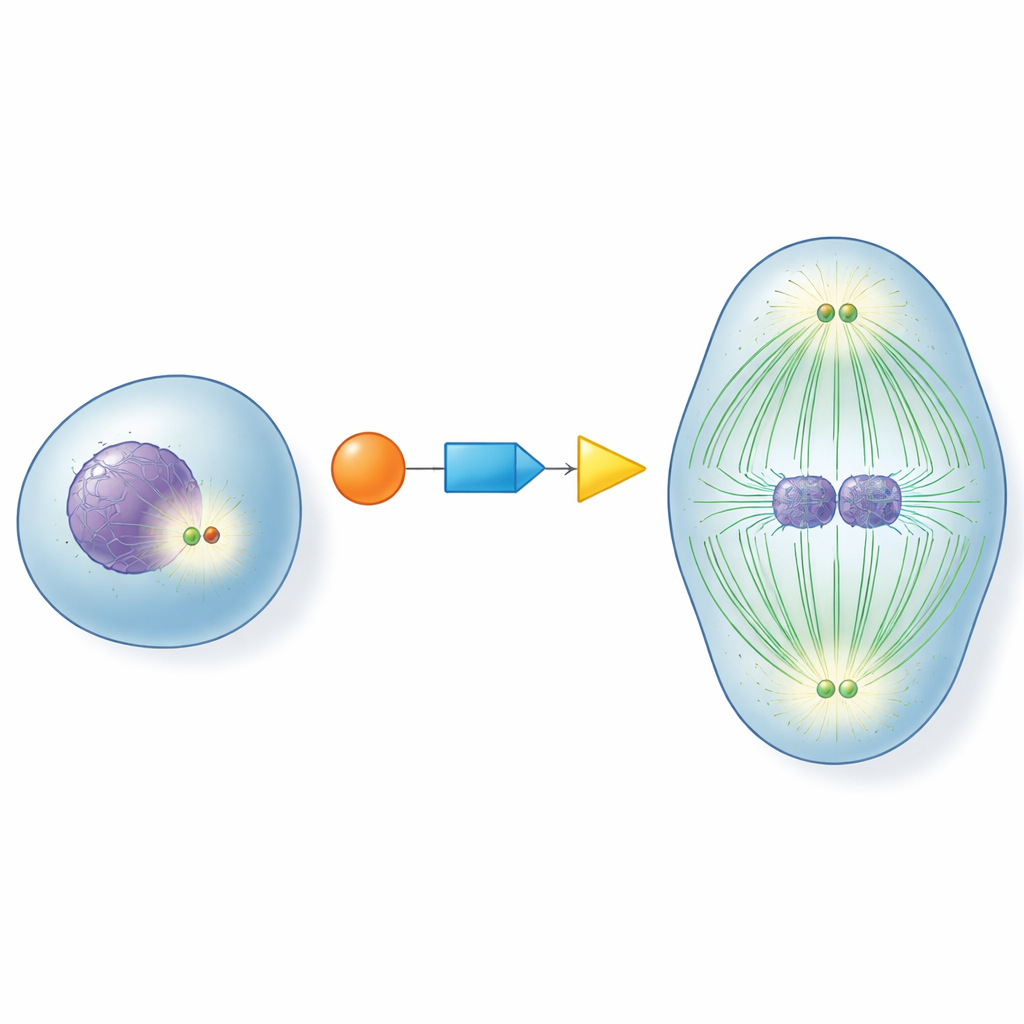
Un relevo molecular para una sincronización perfecta
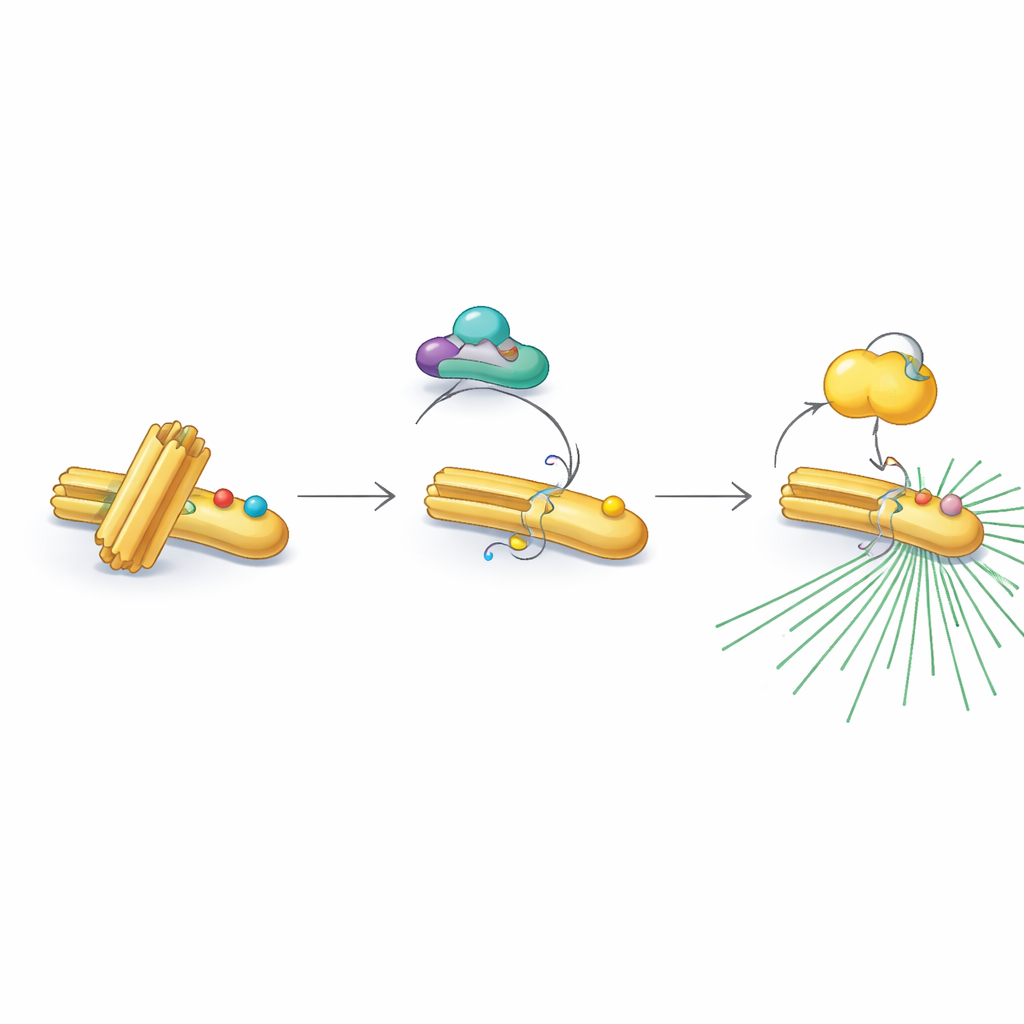
Los autores se centraron en tres proteínas clave que actúan juntas como un relevo: CDK1, un controlador maestro del ciclo celular; RNF40, conocido hasta ahora principalmente por modificar las proteínas que empaquetan el ADN; y PLK1, un impulsor importante de la división celular. Descubrieron que RNF40 está físicamente presente en los centrosomas a lo largo del ciclo celular y se une directamente a PLK1. A medida que las células se acercan a la división, CDK1 marca químicamente a RNF40 en dos puntos específicos, lo que a su vez convierte a RNF40 en un mejor sitio de anclaje para PLK1. Esta cadena CDK1–RNF40–PLK1 asegura que PLK1 llegue a los centrosomas precisamente durante la fase tardía de preparación para la división, desencadenando una maduración robusta del centrosoma, crecimiento de microtúbulos y el ensamblaje de un huso bipolar bien formado.
Un interruptor proteico que cambia de forma
De manera intrigante, RNF40 no acepta siempre estas marcas activadoras. En las fases no divididas y de copia del ADN, RNF40 porta una decoración química diferente —grupos acetilo— en dos posiciones cercanas. Estas marcas acetilo son añadidas por una enzima llamada PCAF y eliminadas posteriormente por un socio desacetilante, HDAC1. La versión acetilada de RNF40 resiste la modificación por CDK1, bloqueando efectivamente el siguiente paso del relevo. A medida que las células entran en la etapa final previa a la división, HDAC1 borra gradualmente las marcas de acetilación, permitiendo que CDK1 añada grupos fosfato en su lugar. Este cambio finamente temporizado de acetilación a fosforilación convierte a RNF40 de un estado de «espera» a un estado «activo», listo para reclutar PLK1 y poner en marcha el centrosoma.
Qué ocurre cuando la sincronización falla
Para investigar cuán crucial es este interruptor, los investigadores diseñaron células en las que RNF40 ya no podía ser fosforilada, o en las que se le obligaba a permanecer en un estado que imita la acetilación. En ambos casos, PLK1 no logró acumularse correctamente en los centrosomas. Estas células mostraron un crecimiento de microtúbulos debilitado desde los centrosomas, husos malformados y cromosomas desalineados. Muchas terminaron con cromosomas de más o de menos —una condición anormal conocida como aneuploidía— y algunas se volvieron binucleadas, señales de errores catastróficos en la división. En modelos de cáncer, las células bloqueadas en el estado de RNF40 «acetilado» formaron tumores más pequeños en ratones y fueron más sensibles a los fármacos de quimioterapia comúnmente usados para tratar el cáncer colorrectal, lo que sugiere que interrumpir este interruptor puede frenar el crecimiento tumoral.
Vínculos con el cáncer humano y posibilidades futuras
El equipo también examinó datos de pacientes y muestras tumorales. Encontraron que RNF40 suele estar anormalmente abundante en cánceres colorrectales y que ciertas mutaciones asociadas al cáncer cerca de sus sitios de modificación perturban su fosforilación, socavando la función correcta del centrosoma. Estas observaciones conectan el mecanismo de temporización recién descrito directamente con la enfermedad humana. Al identificar una proteína específica que coordina cuándo maduran los centrosomas y cómo se separan los cromosomas, el estudio resalta un «nodo» de señalización que podría apuntarse para forzar a las células cancerosas de división rápida a cometer errores letales durante la división, mientras deja a las células sanas menos afectadas.
Un nuevo punto de apoyo para la división celular fiel
Para el público general, el mensaje clave es que las células dependen de un interruptor químico finamente ajustado en una sola proteína, RNF40, para decidir exactamente cuándo activar la maquinaria que separa los cromosomas. Esta transición de acetilación a fosforilación se comporta como un semáforo en una intersección concurrida, que se vuelve verde solo cuando la célula está realmente lista para dividirse. Cuando el semáforo falla, las células tropiezan durante la división, acumulan errores genéticos y pueden volverse cancerosas. Comprender y controlar este interruptor puede abrir nuevas vías para tratamientos que desestabilicen selectivamente a las células cancerosas saboteando su capacidad de dividirse limpiamente.
Cita: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Palabras clave: maduración del centrosoma, división celular, inestabilidad cromosómica, señalización PLK1, cáncer colorrectal