Clear Sky Science · es
Restaurar la desregulación sináptica postnatal temprana rescata la degeneración de las motoneuronas en un modelo murino de atrofia muscular espinal y bulbar
Por qué pequeños cambios tempranos pueden importar para la debilidad muscular posterior
La atrofia muscular espinal y bulbar (SBMA) es una enfermedad hereditaria rara en la que los adultos, por lo general hombres, pierden lentamente fuerza en las extremidades, el tronco y la garganta. Los síntomas aparecen a mitad de la vida, pero problemas sutiles comienzan mucho antes. Este estudio plantea una pregunta sorprendente: ¿podrían eventos breves en los primeros días tras el nacimiento preparar en silencio el terreno para la pérdida de células nerviosas décadas después —y podría corregir esos fallos tempranos proteger el movimiento?
Una enfermedad enraizada en un interruptor sensible a hormonas
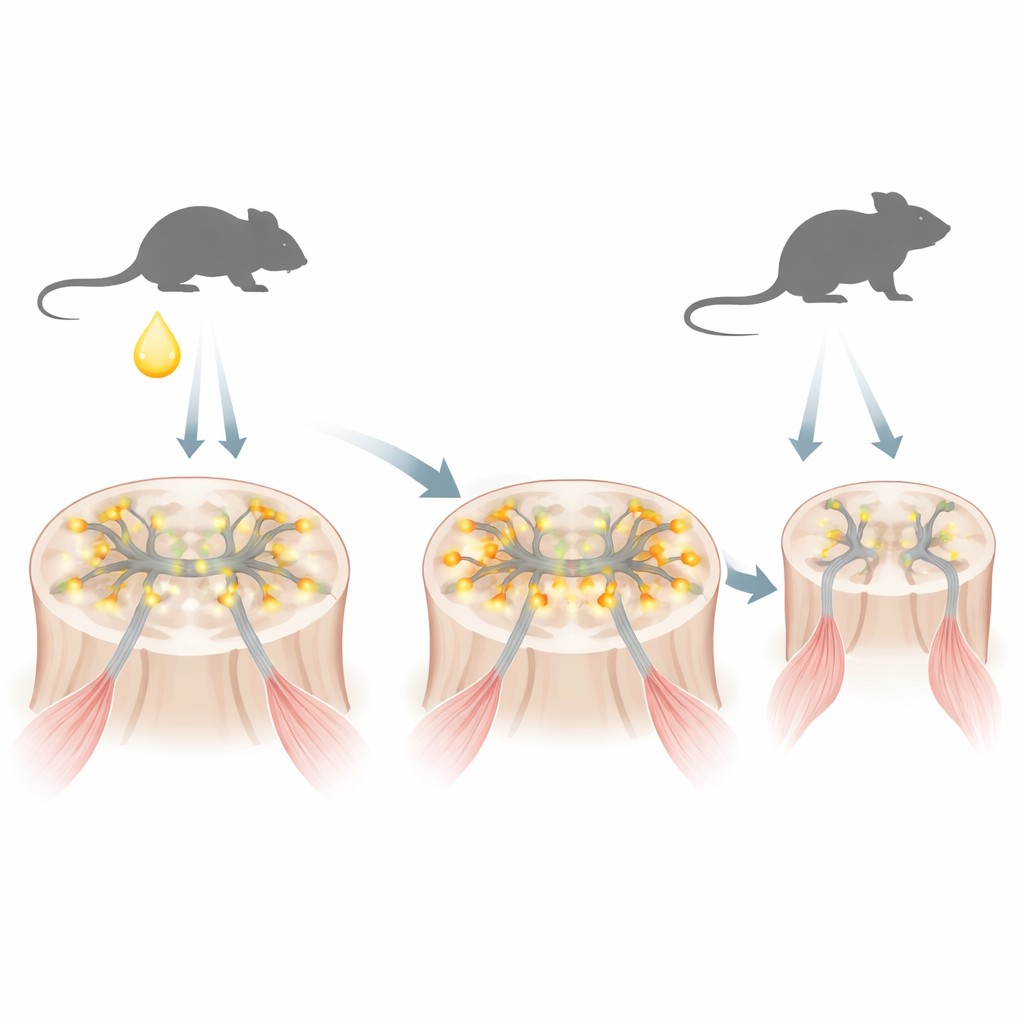
La SBMA es causada por una versión alterada del receptor de andrógenos, una proteína que detecta hormonas masculinas como la testosterona. El receptor alterado contiene una cadena excesivamente larga del aminoácido glutamina. En un modelo de ratón que imita la enfermedad humana, los autores hallaron que justo después del nacimiento, cuando la testosterona aumenta brevemente en los recién nacidos machos, este receptor mutante se acumula rápidamente en los núcleos de las motoneuronas —las células nerviosas que controlan los músculos. En esta etapa temprana la proteína aún no se ha agru pado en los grandes agregados típicamente vinculados a la neurodegeneración, pero ya está cambiando qué genes se activan y cuáles se silencian.
Sobreexcitación sináptica temprana y motoneuronas inquietas
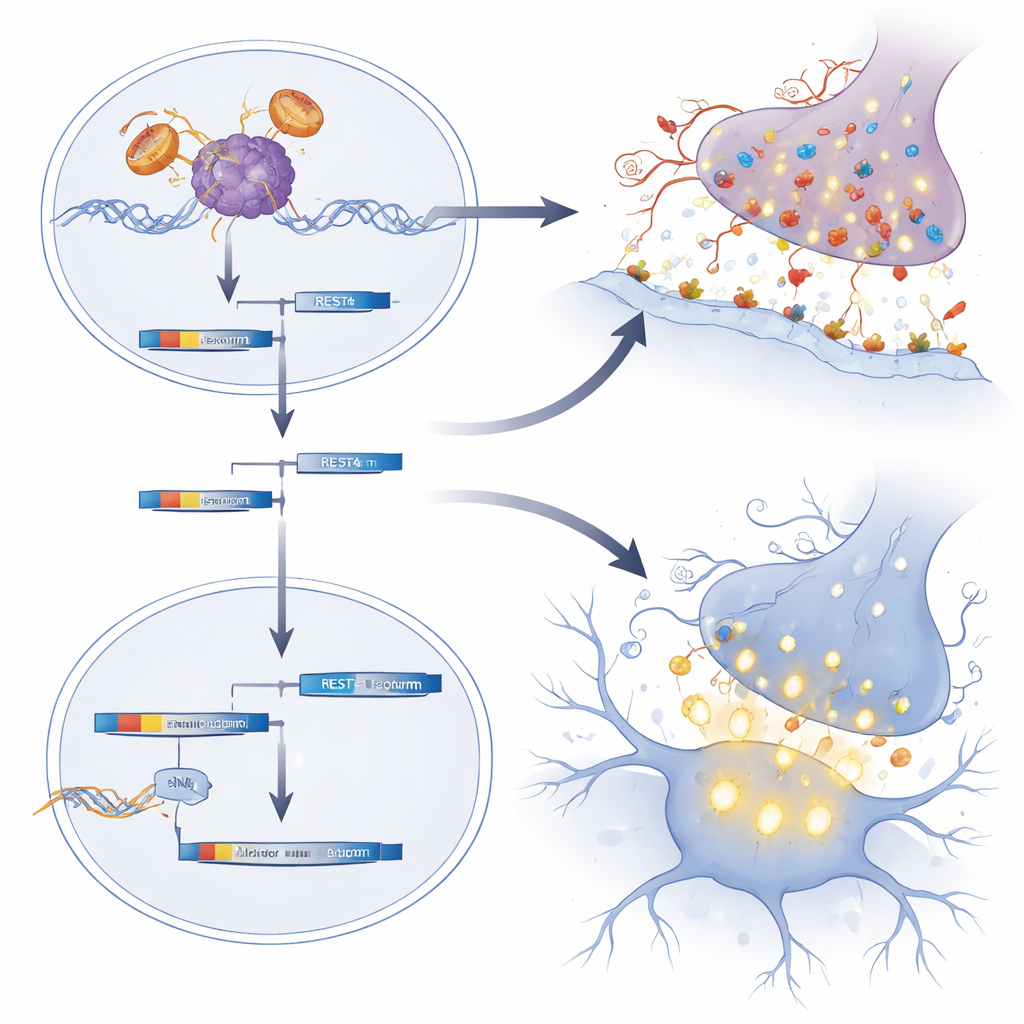
Mediante secuenciación de ARN a escala del genoma en médulas espinales de ratones recién nacidos, el equipo descubrió que muchos genes implicados en sinapsis excitatorias —los puntos de contacto donde las neuronas se comunican— estaban inusualmente activos. Muchos de esos genes codifican receptores de glutamato, que aumentan la probabilidad de que las neuronas se disparen. El grupo trazó este patrón a una alteración de REST, una proteína «freno» maestra que normalmente mantiene bajo estricto control esos genes sinápticos durante el desarrollo. En ratones con SBMA y en motoneuronas derivadas de células madre pluripotentes inducidas de pacientes, la actividad de REST se veía debilitada y se favorecía una forma acortada llamada REST4, levantando el freno y aumentando los genes de sinapsis glutamatérgicas. En consonancia con esto, las motoneuronas SBMA recién nacidas mostraron niveles más altos de c-Fos, un marcador de actividad reciente, y las motoneuronas humanas derivadas de pacientes exhibieron ráfagas de calcio más fuertes y más frecuentes, signos de hiperexcitabilidad.
Un tratamiento temprano y breve que cambia el curso vital
Los investigadores se preguntaron entonces si reducir el receptor mutante o restaurar el freno REST solo durante esta ventana neonatal podría modificar el curso a largo plazo de la enfermedad. Administraron oligonucleótidos antisentido —cadenas cortas de material genético modificado— en el fluido que rodea el cerebro y la médula espinal de ratones SBMA de un día de edad. Un tipo de oligonucleótido redujo de forma transitoria tanto el receptor de andrógenos mutante como el normal en el sistema nervioso central. Un segundo tipo modificó el empalme de REST alejado de REST4 y hacia REST de longitud completa, controlando así los genes sinápticos. De manera notable, aunque estos tratamientos se dieron solo una vez y sus efectos moleculares directos desaparecieron en unas semanas, los ratones vivieron más, se desempeñaron mejor en una barra rotatoria y mantuvieron una mayor fuerza de agarre en etapas posteriores de la vida. Sus motoneuronas y fibras musculares estaban menos atrofiadas, y los marcadores tempranos de hiperactividad neuronal y posteriores picos de neuropéptidos relacionados con el estrés se vieron atenuados.
Cómo las hormonas tempranas y la regulación génica moldean la vulnerabilidad
El trabajo también subraya la vulnerabilidad especial de las motoneuronas al breve estallido de testosterona que ocurre poco después del nacimiento. Cuando a los ratones SBMA recién nacidos se les administró testosterona adicional, su debilidad y pérdida de peso posteriores empeoraron, y los programas génicos vinculados a la maduración sana de las motoneuronas se vieron aún más alterados. Los ratones normales no mostraron este daño, lo que enfatiza que es la combinación del receptor mutante y el pico hormonal lo que resulta perjudicial. En conjunto, los hallazgos sugieren que en SBMA un exceso de sinapsis excitatorias y motoneuronas demasiado excitable temprano en la vida empuja lentamente el sistema hacia el fallo, aunque los síntomas evidentes no emerjan hasta la mediana edad.
Qué significa esto para las personas con SBMA
Para un público no especialista, el mensaje clave es que la SBMA puede ser, en parte, una enfermedad de sinapsis desincronizadas y mal conectadas durante los primeros días tras el nacimiento. Un sensor hormonal defectuoso empuja a las motoneuronas en desarrollo hacia un estado de sobreexcitación, y este estrés temprano contribuye con el tiempo a su degeneración años después. La noticia alentadora es que medicamentos genéticos diseñados con cuidado, administrados durante estas ventanas críticas, pueden reajustar el equilibrio de señales en las motoneuronas, calmar su sobreactividad y retrasar o reducir de forma significativa la pérdida neuronal posterior en animales. Aunque traducir tales intervenciones en la primera etapa de la vida a humanos requerirá mucha precaución y más investigación, estos resultados apuntan a nuevas estrategias que atacan las raíces de la SBMA mucho antes de que aparezca la debilidad.
Cita: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
Palabras clave: atrofia muscular espinal y bulbar, hiperexcitabilidad de las motoneuronas, receptor de andrógenos, regulación sináptica por REST, terapia con oligonucleótidos antisentido