Clear Sky Science · es
Selección de vía entre reacciones de 'click' y transferencia acilo impulsadas por aminoacilfosfatos
Por qué el tiempo importa en la química cotidiana
Dentro de cada célula, las moléculas importantes se construyen y modifican en un orden muy preciso, como los pasos de una receta. Ese orden determina si una proteína se activa, se desactiva o incluso cambia de forma. Los químicos buscan imitar este tipo de programación incorporada usando moléculas sencillas no vivas en agua, sin depender de enzimas ni de disparadores externos como luz o cambios bruscos de pH. Este artículo describe un sistema de reacción sintético que hace precisamente eso: emplea la estructura de pequeños péptidos y una reacción popular de formación de enlaces de la «química click» para decidir qué paso químico ocurre primero y cuál debe esperar.
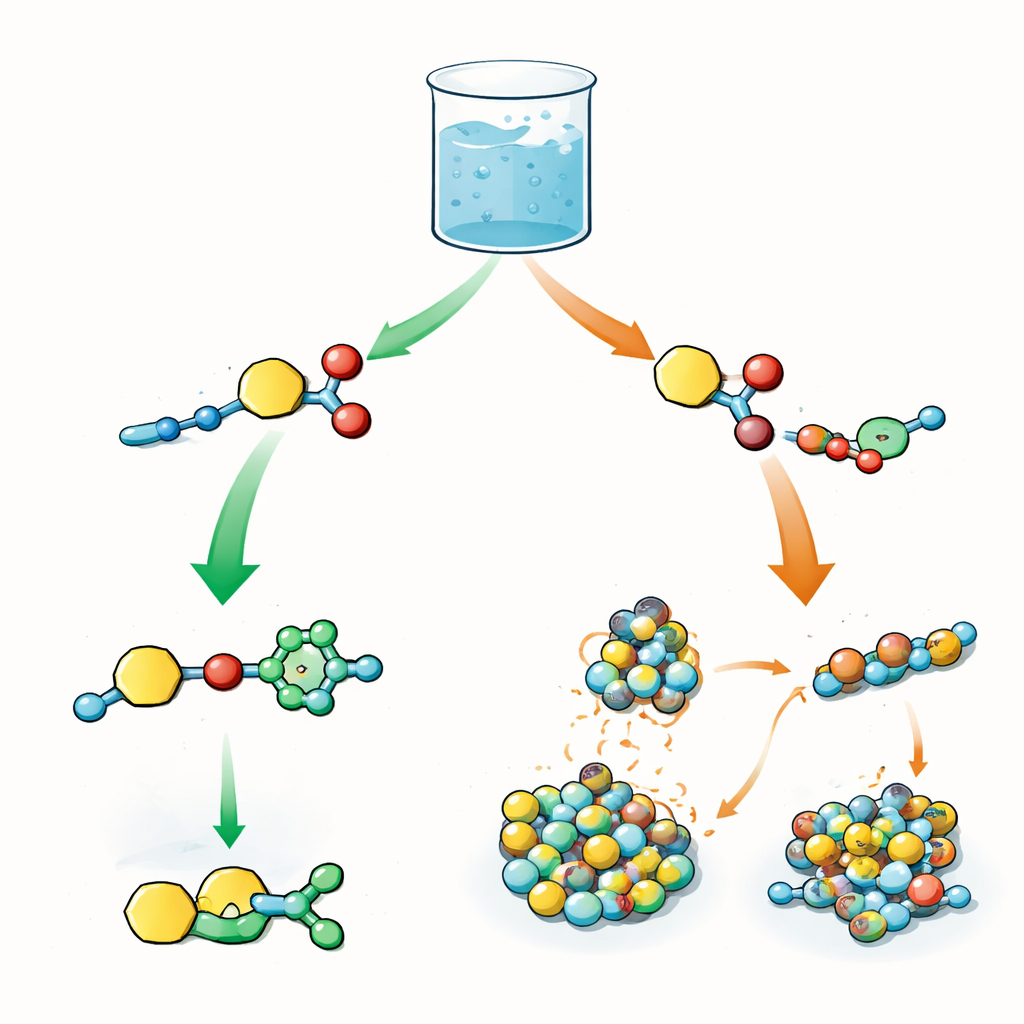
Dos reacciones rivales en un mismo vaso
Los autores diseñan un bloque de construcción central que lleva dos rasgos reactivos: uno que puede transferir un grupo acilo (un fragmento químico pequeño utilizado con frecuencia para modificar proteínas) y otro que puede sufrir una reacción click llamada cicloadición azida–alquino catalizada por cobre. En el mismo vaso de reacción, este bloque se mezcla con azidas y con péptidos cortos que actúan como nucleófilos, es decir, que capturan el grupo acilo. En biología, el orden de pasos como activación, transferencia y modificaciones posteriores controla el comportamiento de las proteínas. Aquí la pregunta es similar: cuando ambas reacciones son posibles a la vez, ¿el sistema elige primero la reacción click, primero la transferencia acilo, o alguna mezcla de ambas?
Oxígeno lento, azufre rápido
El equipo estudia primero péptidos que contienen tirosina, un aminoácido con una cadena lateral basada en oxígeno. Bajo condiciones ligeramente básicas, la reacción click corre por delante: el alquino y la azida se unen rápidamente, mientras que la transferencia acilo a la cadena lateral de tirosina es lenta y apenas forma intermedios detectables. Coexisten varios productos derivados del click y no hay una brecha temporal clara entre pasos. Cuando los investigadores cambian a cisteína, un aminoácido con una cadena lateral basada en azufre, la historia se invierte. La cisteína forma rápidamente tioésteres—productos acilados ligados al azufre—que aparecen en alto rendimiento mucho antes que cualquier producto de click. Solo tras muchas horas comienzan a aparecer productos de click. Este cambio se debe a que el azufre no solo reacciona con más facilidad sino que además se coordina con iones de cobre, secuestrando el catalizador y «pausando» temporalmente la vía del click.
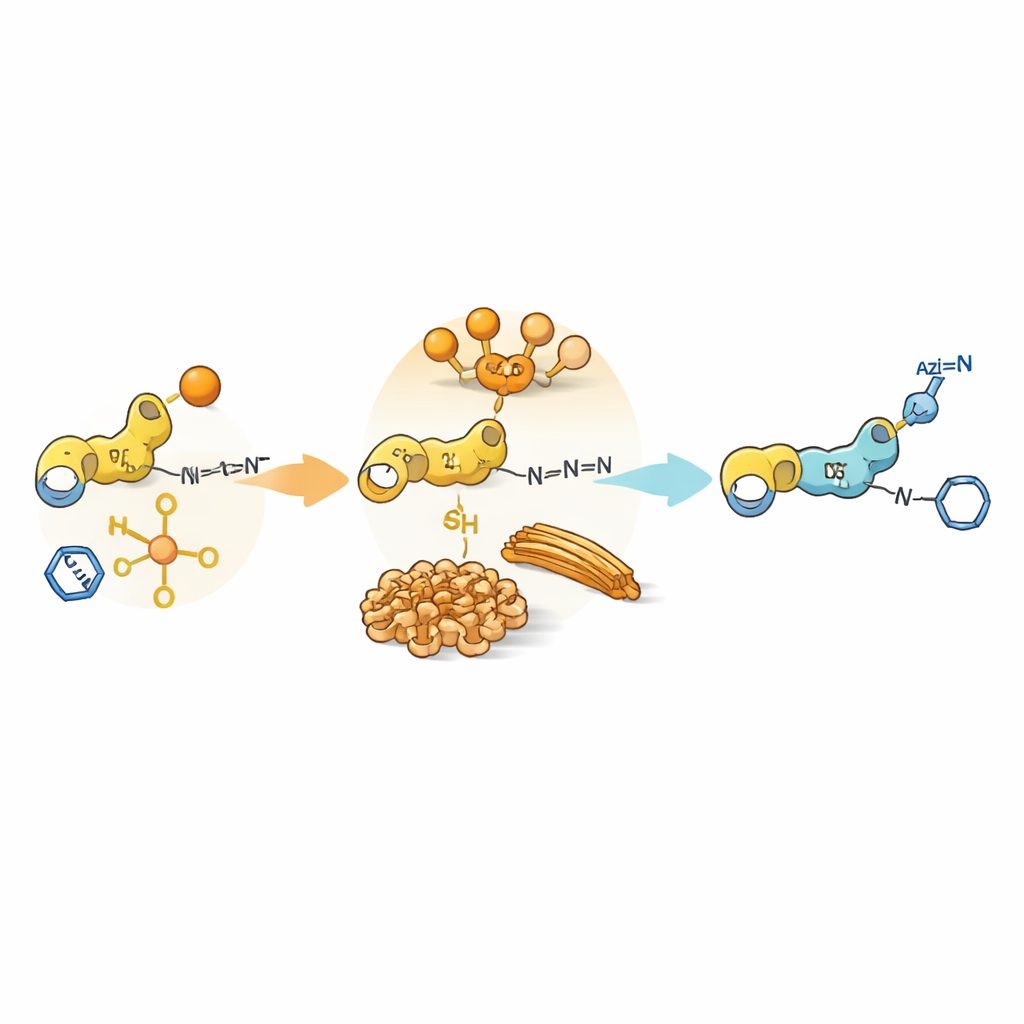
Autoensamblaje como compuerta química
Más allá de la reactividad simple, los propios péptidos pueden agruparse en estructuras mayores, formando geles suaves o fibras en agua. Estos ensamblajes crean dominios diminutos donde algunos componentes se concentran y otros quedan excluidos. Para ciertos dipeptidos que contienen tirosina o cisteína y que llevan grupos aromáticos adicionales, los intermedios se autoensamblan en fibrillas o partículas densas. Dentro de estas regiones compactas, la transferencia acilo resulta favorecida porque nucleófilo y donador de acilo quedan uno al lado del otro, mientras que la azida y el catalizador de cobre permanecen mayormente en la solución circundante. Como resultado, aunque la reacción click es intrínsecamente rápida en solución libre, se ralentiza porque debe alcanzar sitios reactivos ocultos. Este «desajuste de fase» entre dónde vive el catalizador y dónde se localizan los sustratos alarga la vida de los intermedios acilados y retrasa el inicio de la química click.
Programar cascadas y decisiones
Para probar hasta qué punto pueden empujar esta programación incorporada, los autores diseñan situaciones más complejas. En un caso, un único péptido contiene tanto cisteína como tirosina, ofreciendo dos sitios distintos de transferencia acilo. La reacción avanza como una cascada de tres pasos: primero se forma un tioéster en la cisteína, luego un segundo grupo acilo se traslada a la tirosina, y solo después de estos pasos aparecen los productos de click. En otro conjunto de experimentos, dos azidas diferentes—una flexible y alifática y otra rígida y aromática—compiten por el mismo centro reactivo. Sorprendentemente, el sistema prefiere consistentemente la azida alifática, lo que revela que incluso la forma y el carácter electrónico de la azida pueden sesgar qué productos dominan, mientras que el momento de la transferencia acilo sigue bajo control del péptido.
Qué significa esto para futuros materiales inteligentes
En términos sencillos, este trabajo muestra cómo es posible alojar múltiples reacciones potencialmente competitivas en la misma mezcla acuosa simple y aun así lograr que se sucedan en un orden prefijado—sin enzimas, bombas ni interruptores externos. Al elegir si un péptido porta oxígeno o azufre, al ajustar su tendencia al autoensamblaje y al modificar la naturaleza del compañero azida, los autores codifican una especie de reloj interno en una pequeña red química. Las transferencias acilo tempranas y reversibles crean intermedios de corta vida que determinan cuándo y cómo ocurre el paso robusto y casi irreversible del click. Tales secuencias programadas podrían sentar las bases de materiales inteligentes y redes de reacción sintéticas que “decidan” sus propias vías a lo largo del tiempo, de modo análogo a la química cuidadosamente cronometrada que opera en las células vivas.
Cita: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Palabras clave: química click, transferencia acilo, ensamblaje supramolecular, redes de reacción, química de péptidos