Clear Sky Science · es
Cartografía molecular en DNA-PAINT mediante un modelo de mezcla gaussiana modificado
Ver el mundo invisible de las moléculas
La biología moderna depende cada vez más de microscopios capaces de ver no solo células, sino moléculas individuales en su interior. Sin embargo, convertir la luz tenue y parpadeante procedente de esas moléculas en un “mapa” fiable de la posición de cada una resulta sorprendentemente difícil. Este estudio presenta un nuevo método computacional, llamado G5M, que hace estos mapas moleculares mucho más precisos y detallados, ayudando a los científicos a entender cómo se disponen y agrupan las proteínas en células reales, hasta escalas de solo unos pocos nanómetros.
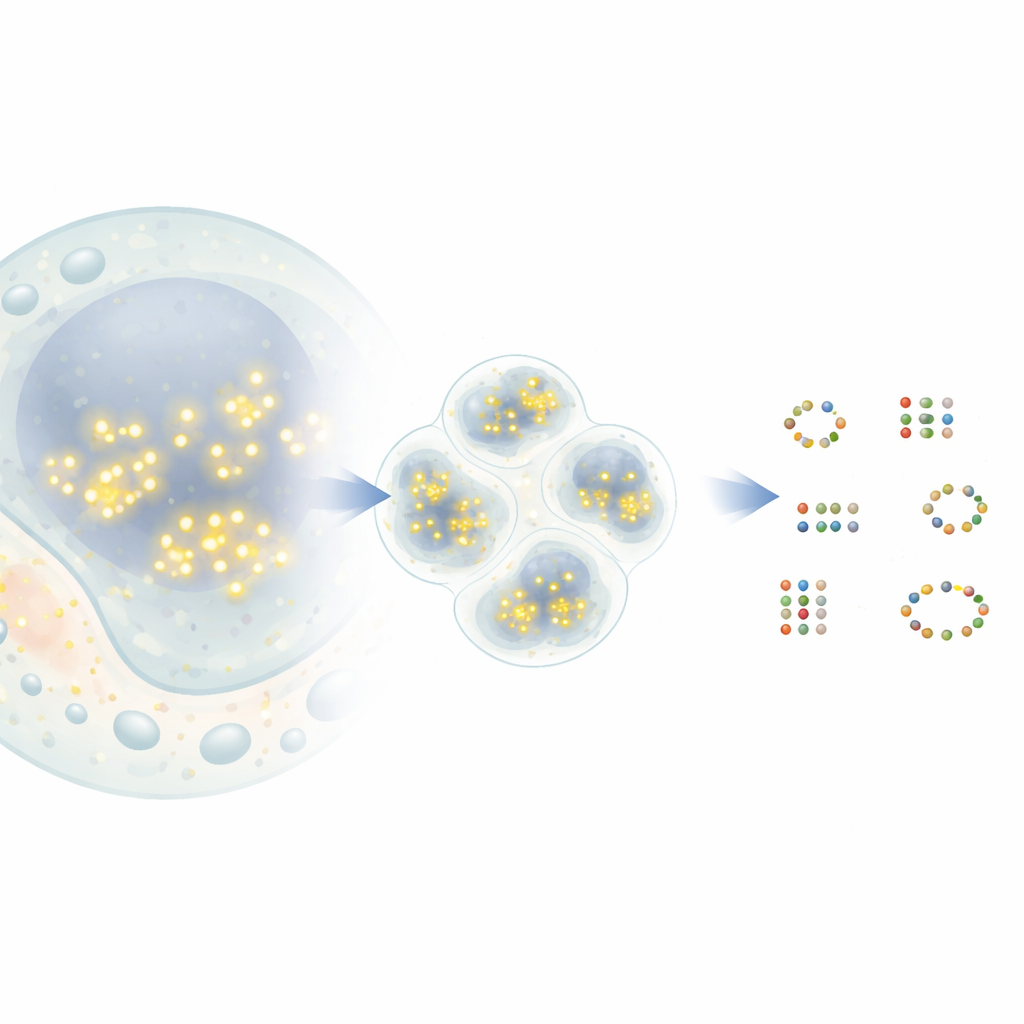
De puntos parpadeantes a mapas moleculares
En una técnica de superresolución popular llamada DNA-PAINT, breves hebras de ADN con tintes fluorescentes se unen y separan momentáneamente de etiquetas de ADN acopladas a proteínas diana. Cada vez que un tinte se une, aparece como un punto brillante en el microscopio antes de desaparecer. Con el tiempo, muchos de estos eventos crean una nube de puntos alrededor de cada proteína. En principio, el centro de cada nube marca la posición real de una proteína con precisión nanométrica. En la práctica, sin embargo, los puntos de proteínas cercanas pueden solaparse y algunos puntos proceden de señales de fondo aleatorias. Las herramientas de análisis existentes a menudo fusionan vecinos cercanos en una sola proteína o, por el contrario, inventan proteínas que no existen, lo que limita la cantidad de información biológica que se puede extraer.
Una forma más inteligente de encontrar moléculas reales
El nuevo método, G5M, trata el enjambre de puntos como una mezcla de nubes simples en forma de campana, cada una correspondiente a una molécula real. En lugar de agrupar puntos cercanos solo por densidad, G5M utiliza un modelo probabilístico que incorpora lo que ya se sabe sobre el experimento: qué precisión tiene la medida de posiciones, qué rapidez se unen y separan las hebras de ADN y cómo el microscopio difumina la luz en dos o tres dimensiones. Después evalúa distintas explicaciones posibles —diferentes números y formas de nubes— y selecciona automáticamente la que mejor equilibra ajuste y simplicidad. Salvaguardas adicionales rechazan soluciones sospechosas, como nubes demasiado estrechas, demasiado anchas, basadas en muy pocos puntos o no claramente separadas entre sí.
Demostrando su potencia en simulaciones y nanoestructuras de ADN
Para probar G5M, los autores primero usaron simulaciones informáticas realistas de escenas sencillas: pares de moléculas y pequeñas retículas de doce moléculas separadas apenas por unos nanómetros. En comparación con el método líder actual, conocido como Gradient Ascent, G5M detectó muchas más de las moléculas que deberían ser visibles en el límite teórico de resolución, mientras que casi nunca informó moléculas inexistentes. En casos clave, recuperó pares estrechamente separados veintisiete veces más a menudo que el método anterior y mejoró la resolución efectiva en más de la mitad. El equipo confirmó estos avances experimentalmente usando estructuras de origami de ADN —formas de ADN artificiales con sitios de acople colocados en posiciones precisamente conocidas— mostrando que G5M podía contar y localizar de forma fiable casi todos los sitios esperados en una variedad de condiciones de imagen.
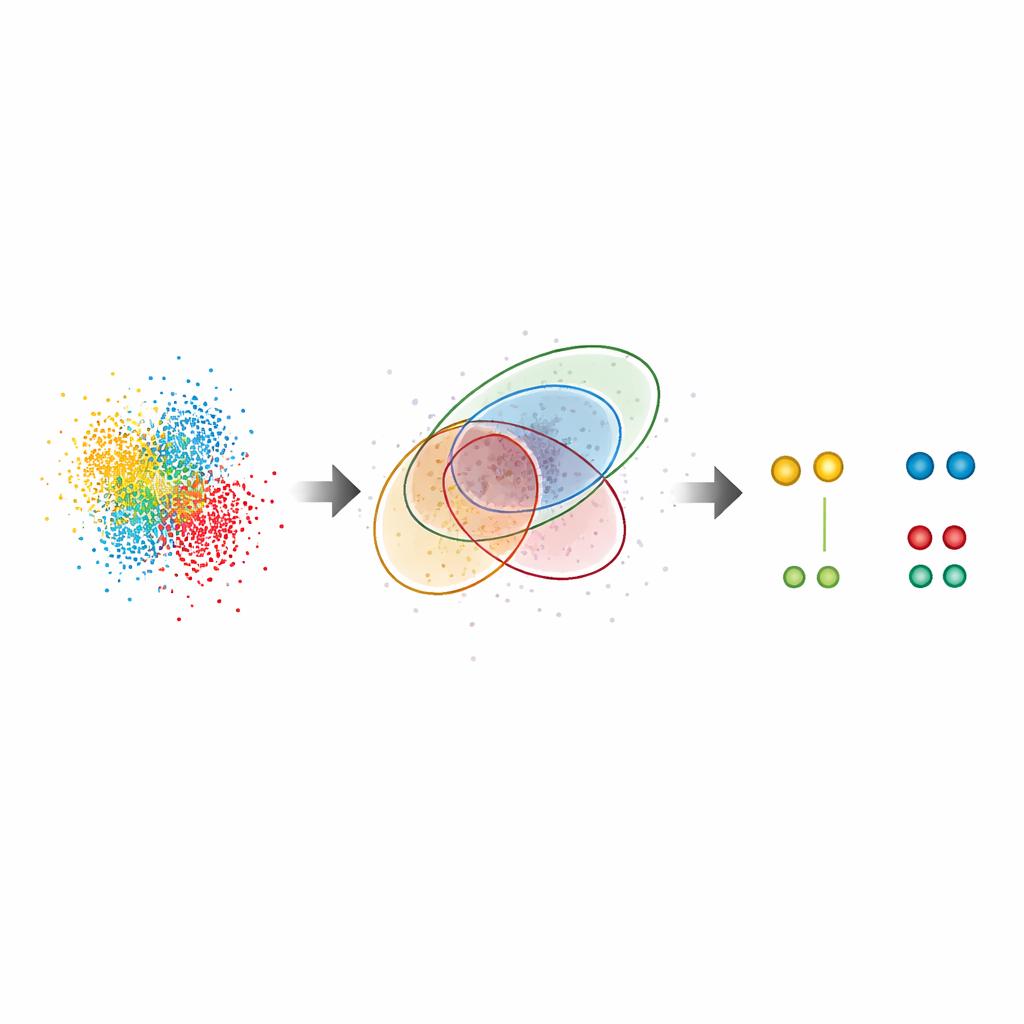
Revelando patrones ocultos en células reales
Más allá de las muestras de prueba, G5M se aplicó a sistemas biológicos complejos. En los complejos del poro nuclear, grandes puertas en el núcleo celular, el método recuperó la disposición conocida en forma de anillo de una proteína clave, Nup96, incluso donde las subunidades estaban separadas por solo unos diez nanómetros. Encontró casi el doble de pares de proteínas que el método estándar y reprodujo estimaciones independientes de la eficiencia de marcado, lo que sugiere que no pasa por alto muchas moléculas ni añade elementos espurios. Los autores también examinaron CD20, un receptor de superficie implicado en cánceres sanguíneos y objetivo de anticuerpos terapéuticos. Allí, G5M reveló un número significativamente mayor de pequeños conglomerados (dímeros, trímeros y tetrámeros) de CD20 en la membrana celular, clarificando cómo un anticuerpo anticáncer y formatos de fármacos relacionados reorganizan estos receptores. Incluso mejoró el rendimiento de un enfoque de ultraalta resolución llamado RESI, que se basa en separar señales a lo largo de múltiples rondas de imagen.
Qué significa esto para la microscopía futura
Al extraer información más fiable de datos existentes de DNA-PAINT, G5M demuestra que solo con mejor software se pueden desbloquear nuevos detalles biológicos, sin cambiar microscopios ni tintes. El algoritmo mantiene las detecciones falsas extremadamente bajas mientras resuelve moléculas que están casi en contacto, lo cual es esencial cuando se pregunta cuántas proteínas hay en un complejo, cómo están espaciadas o cómo un fármaco cambia su disposición. Integrado en la plataforma de código abierto Picasso y robusto frente a configuraciones típicas, G5M está preparado para convertirse en una herramienta estándar para convertir fluorescencia intermitente en mapas moleculares fiables, ayudando a los investigadores a cartografiar la organización a escala nanométrica de la vida dentro de las células.
Cita: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Palabras clave: microscopía de superresolución, DNA-PAINT, cartografía molecular, oligomerización de proteínas, algoritmos de análisis de imágenes