Clear Sky Science · es
La multiómica unicelular descubre un eje endotelial mecanosensible PIEZO1‑IL‑33 que impulsa la fibrosis pulmonar
Por qué importan los pulmones rígidos
La fibrosis pulmonar es una enfermedad devastadora en la que los sacos de aire que antes eran elásticos se transforman lentamente en tejido cicatricial rígido, de modo que cada respiración se vuelve un esfuerzo. Hoy por hoy los médicos solo pueden ralentizar la enfermedad, no detenerla ni revertirla. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones: ¿cómo perciben las células que recubren los vasos sanguíneos pulmonares que el tejido que las rodea se ha vuelto anormalmente rígido, y cómo se traduce esa percepción en más cicatrización? Al trazar esta cadena de eventos hasta la célula única y genes individuales, los investigadores descubren un “interruptor” mecánico en los vasos sanguíneos que podría ser modulable farmacológicamente.
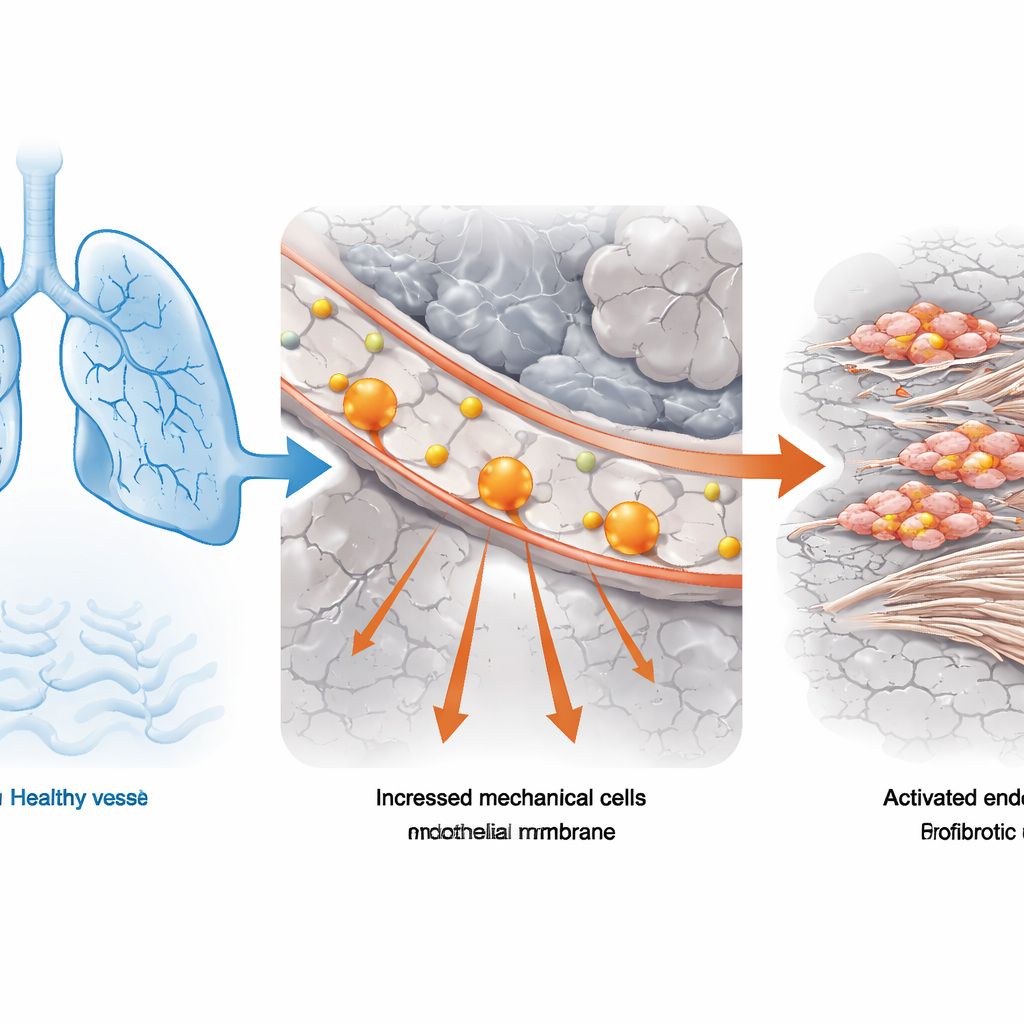
De las pruebas de función pulmonar a las células individuales
El equipo comenzó con tejido pulmonar de personas con fibrosis pulmonar idiopática, la forma más común de la enfermedad, y de donantes con pulmones normales. Combinaron las medidas estándar de función pulmonar (cuánto aire puede exhalar una persona con fuerza) con potentes análisis de ARN unicelular, que determinan qué genes están activos en miles de células individuales. Usando una herramienta computacional que vincula datos clínicos globales con perfiles unicelulares, identificaron qué tipos celulares se asociaban más estrechamente con una función pulmonar gravemente deteriorada. Las células endoteliales vasculares —las que forman el revestimiento interno de los vasos sanguíneos— destacaron por estar especialmente enriquecidas en pacientes cuya capacidad pulmonar era menos de la mitad de la normal. En estas células endoteliales, los programas génicos relacionados con el «estrés mecánico» estaban consistentemente activados, lo que sugiere que fuerzas físicas anómalas formaban parte del problema.
El estrés mecánico como un impulsor oculto
Para probar si este vínculo entre la detección del estrés y la enfermedad era general, los investigadores recurrieron a dos modelos murinos de cicatrización pulmonar: uno desencadenado por el fármaco quimioterápico bleomicina y otro por exposición a largo plazo a polvo de sílice, un riesgo laboral. Aplicando métodos unicelulares en estos pulmones experimentales, volvieron a encontrar que las células endoteliales mostraban firmas claras de estrés mecánico potenciado. En ambos modelos, a medida que el tejido pulmonar circundante se engrosaba y rigidizaba, el revestimiento de los vasos parecía pasar a un estado maladaptativo. Esta convergencia entre muestras humanas y modelos animales reforzó la idea de que las fuerzas físicas distorsionadas en el pulmón, más que solo la inflamación o la actividad inmune, son centrales en el desarrollo y la progresión de la fibrosis.
Un sensor de presión con un papel crítico
Indagando más, el equipo buscó «mecanorreceptores» específicos —proteínas que convierten la deformación física en señales bioquímicas— que estuvieran sobreactivados en las células endoteliales sometidas a estrés. Una proteína canal, llamada PIEZO1, emergió repetidamente como principal sospechosa. Tanto en ratones como en humanos con fibrosis, los niveles de PIEZO1 eran marcadamente más altos en células endoteliales vasculares que en controles sanos. Cuando los investigadores diseñaron ratones con eliminación de PIEZO1 únicamente en el endotelio, estos animales fueron mucho más resistentes a la cicatrización pulmonar inducida por bleomicina: presentaron menos acumulación de colágeno, menos células activadas formadoras de cicatriz y niveles más bajos de un marcador químico de fibrosis. El bloqueo farmacológico de PIEZO1 con un inhibidor peptídico también alivió la cicatrización, mientras que su activación la empeoró —a menos que el receptor faltara en las células endoteliales. En conjunto, estos experimentos mostraron que PIEZO1 en las células que recubren los vasos no es un mero espectador, sino un impulsor necesario de la enfermedad.
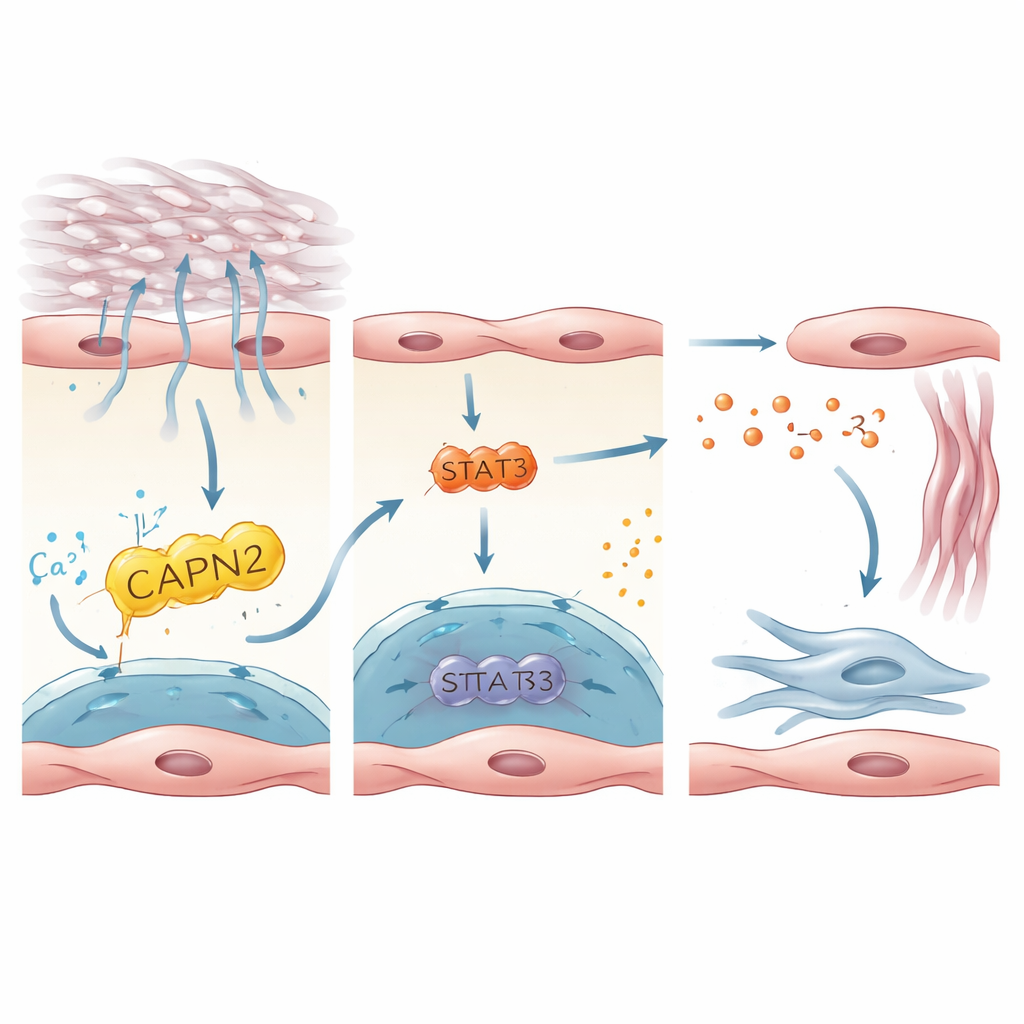
Una cadena de señalización que despierta a las células formadoras de cicatriz
El estudio trazó a continuación cómo la activación de PIEZO1 dentro de las células endoteliales se traduce en señales que despiertan a los fibroblastos, las células que depositan tejido cicatricial. Integrando conjuntos de datos humanos y murinos, los autores identificaron a la interleucina‑33 (IL‑33), una proteína pequeña liberada por células estresadas o dañadas, como un mensajero clave. IL‑33 se expresó de forma intensa en células endoteliales positivas para PIEZO1 y estaba elevada en pulmones de pacientes y ratones con fibrosis. En cultivos de células endoteliales humanas crecidas sobre sustratos rígidos o estiradas para imitar la respiración contra un pulmón rígido, la activación de PIEZO1 aumentó la producción de IL‑33. Esto dependía de una enzima aguas abajo, CAPN2, y de un factor de transcripción, STAT3, que en conjunto regulaban la actividad génica de IL‑33. En ratones, la eliminación específica de IL‑33 en células endoteliales protegió frente a la fibrosis, mientras que forzar a las células endoteliales a sobreproducir IL‑33 borró el efecto protector de la pérdida de PIEZO1. Estos resultados delinean un eje lineal: estrés mecánico → PIEZO1 → CAPN2/STAT3 → IL‑33 → activación de fibroblastos y cicatrización.
Qué significa esto para tratamientos futuros
Para los no especialistas, la conclusión es que la fibrosis pulmonar no la provocan únicamente células inmunes descontroladas; también es una enfermedad del “tacto” defectuoso en los vasos sanguíneos. Las células endoteliales perciben que su entorno se ha vuelto demasiado rígido, activan el interruptor PIEZO1 y, en respuesta, liberan IL‑33, una señal de peligro que insta a los fibroblastos cercanos a seguir depositando cicatriz. Al diseccionar esta cadena desde la fuerza mecánica hasta la expresión génica, el trabajo destaca varios objetivos prometedores —el propio PIEZO1, el relevo CAPN2‑STAT3 y la IL‑33— para terapias dirigidas a interrumpir el ciclo autorreforzante de rigidez y cicatrización. Aunque hacen falta más estudios para modular con seguridad estas vías en personas, este eje endotelial mecanosensible ofrece un nuevo enfoque, con base física, para abordar una enfermedad que durante mucho tiempo ha resistido tratamientos efectivos.
Cita: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Palabras clave: fibrosis pulmonar, células endoteliales, mecanotransducción, PIEZO1, IL-33