Clear Sky Science · es
Adaptaciones en la tubulina de Plasmodium determinan arquitecturas, mecánica y susceptibilidad a fármacos de microtúbulos distintas
Por qué importa el esqueleto de la malaria
Los parásitos de la malaria sobreviven dentro de los glóbulos rojos humanos, pero también deben abrevarse a través de los mosquitos y distintos tejidos. Para lograrlo, dependen de un andamiaje interno formado por tubos microscópicos llamados microtúbulos. Este estudio plantea una pregunta sencilla pero poderosa: ¿cómo pueden los microtúbulos del parásito ser tan especializados y resistentes cuando sus unidades básicas se parecen tanto a las de nuestras propias células? La respuesta revela no solo cómo el parásito mantiene su forma, sino también cómo podríamos diseñar fármacos que ataquen su armazón sin dañar el nuestro. 
Los tubos minúsculos que dan forma a un parásito letal
Los microtúbulos son tubos proteicos huecos que ayudan a las células a dividirse, moverse y conservar su forma. Se construyen a partir de unidades emparejadas de proteína llamadas tubulina. En animales, plantas y parásitos, la tubulina es sorprendentemente similar, lo que dificulta explicar por qué los microtúbulos pueden tener apariencias y comportamientos tan distintos según el organismo. En el parásito de la malaria Plasmodium falciparum, los microtúbulos forman arreglos diversos: algunos son dinámicos y participan en la división celular, mientras que otros son soportes largos y rígidos bajo la membrana exterior del parásito. Dado que estas estructuras son esenciales para el crecimiento y la transmisión del parásito, constituyen dianas atractivas para fármacos antipalúdicos, especialmente a medida que aumenta la resistencia a los tratamientos actuales.
Ver la tubulina del parásito en detalle atómico
Los investigadores purificaron tubulina directamente de parásitos de P. falciparum y utilizaron crio‑microscopía electrónica de alta resolución para ver cómo se ensamblaba en microtúbulos. Compararon estas estructuras con los microtúbulos bien estudiados del cerebro de mamífero. A primera vista, la tubulina del parásito parece casi idéntica a la versión humana y adopta el mismo pliegue global. Pero una comparación minuciosa reveló grupos de pequeños cambios en la secuencia alrededor de bolsillos clave donde se unen moléculas que intercambian energía (GTP y GDP) y donde interactúan ciertos fármacos. Estos desplazamientos sutiles alteran la posición de hélices y lazos cercanos, especialmente en la superficie del dímero de tubulina donde se fijan otras proteínas y fármacos. El trabajo sugiere que, aunque el plano general está conservado, afinamientos locales en el parásito remodelan de forma sutil esos sitios importantes.
Tubos más rígidos por enlaces laterales más fuertes
Los microtúbulos son polímeros: muchos dímeros de tubulina se apilan extremo con extremo formando protofilamentos, y varios protofilamentos se alinean lado a lado para formar la pared del tubo. El equipo encontró que, en los microtúbulos del parásito, los contactos longitudinales a lo largo de cada protofilamento son muy similares a los de los microtúbulos cerebrales. La diferencia aparece en los contactos laterales entre protofilamentos vecinos. Aunque el área de contacto es en realidad algo menor en el parásito, las simulaciones revelan que estas conexiones laterales son colectivamente más fuertes, lo que hace que la red sea más rígida. Modelos por ordenador de parches de la pared del microtúbulo mostraron que la tubulina del parásito se dobla y torsiona menos que la tubulina cerebral. La tomografía electrónica de extremos reales de microtúbulos confirmó que los microtúbulos del parásito tienen rizos de protofilamento más cortos y menos abiertos, una señal distintiva de un tubo más robusto. 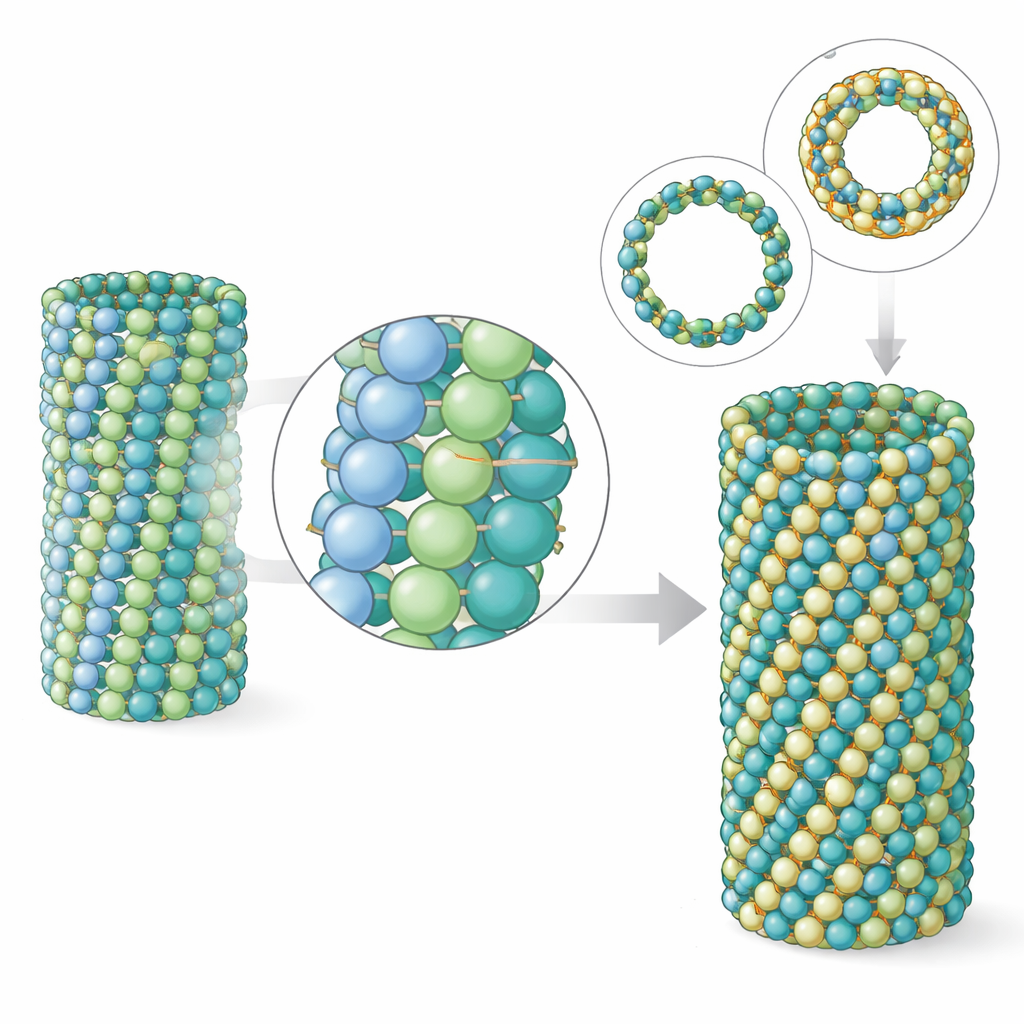
Tamaños de tubo inusuales que encajan con la vida del parásito
Otra característica llamativa de P. falciparum es que, en algunas etapas de su ciclo, sus microtúbulos contienen más unidades alrededor de la circunferencia que las 13 habituales en la mayoría de las células animales —con frecuencia 15 o incluso 17 hileras de protofilamentos. El equipo recreó este comportamiento en el laboratorio cambiando el nucleótido usado durante el ensamblaje. Con una molécula tipo GTP que estabiliza el estado de crecimiento, la tubulina del parásito mostró una preferencia natural por microtúbulos de 15 protofilamentos. Los autores resolvieron la estructura de estos tubos más gruesos y mostraron cómo acomodan los protofilamentos adicionales con un ligero sesgo de la red, sin dejar de ser casi perfectamente cilíndricos. Cuando compararon estos tubos de 15 protofilamentos hechos en el laboratorio con los observados dentro de células del parásito, la coincidencia en forma y dimensiones fue notablemente cercana, lo que indica que las propiedades intrínsecas de la tubulina —más que una multitud de proteínas ayudantes— son suficientes para generar las arquitecturas distintivas del parásito.
Pistas para fármacos futuros específicos del parásito
La conclusión del estudio es que la evolución ha afinado la tubulina del parásito mediante pequeños cambios dispersos en la secuencia que, en conjunto, modifican la mecánica, la arquitectura y la sensibilidad a fármacos de los microtúbulos. Estos ajustes hacen que los microtúbulos del parásito sean más rígidos y capaces de formar tamaños de tubo no estándar que se adaptan a su exigente ciclo vital, conservando al mismo tiempo el diseño básico de la tubulina. Importante para la medicina, algunos bolsillos de unión a fármacos parecen casi idénticos entre parásito y huésped (como ocurre con el fármaco contra el cáncer paclitaxel), lo que sugiere que son objetivos poco adecuados para antipalúdicos selectivos. Otros, como la región que se piensa que une al compuesto parecido a un herbicida orizalin, muestran tanto cambios en la secuencia como desplazamientos estructurales sutiles que podrían explicar por qué los microtúbulos del parásito son más vulnerables allí que los humanos. Cartografiar estas diferencias matizadas proporciona una hoja de ruta para diseñar fármacos futuros que alteren el armazón del parásito de la malaria dejando nuestras propias células en gran medida indemnes.
Cita: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Palabras clave: parásito de la malaria, microtúbulos, estructura de la tubulina, dirigido por fármacos, crio‑microscopía electrónica