Clear Sky Science · es
El ensamblaje del núcleo covalente en la biosíntesis de fostriecina implica malonilación-lactonización por una tioesterasa bifuncional y desmalonilación enzimática
Cómo la naturaleza construye un diminuto núcleo químico
Los medicamentos contra el cáncer y los antibióticos suelen depender de unos pocos átomos dispuestos de forma precisa: un diminuto “núcleo” que se ancla a una proteína y la inactiva. El compuesto natural fostriecina es una de esas moléculas, con potente actividad frente a enzimas implicadas en el crecimiento celular. Pero su estructura compleja dificulta su fabricación y modificación en el laboratorio. Este estudio desentraña, paso a paso, cómo las bacterias ensamblan el núcleo crucial de la fostriecina, revelando trucos enzimáticos que los químicos pueden ahora aprovechar para diseñar nuevos fármacos.
El gancho especial en fármacos naturales potentes
Muchos fármacos prometedores procedentes de bacterias del suelo pertenecen a una familia llamada poliquétidos. Dentro de esta familia, un subgrupo lleva un anillo reactivo, conocido por los químicos como una δ-lactona α,β-insaturada, que actúa como un anzuelo molecular. Puede formar un enlace permanente con ciertos aminoácidos en proteínas, apagando interruptores biológicos clave. En la fostriecina y moléculas relacionadas, este gancho se combina con un grupo fosfato que les ayuda a dirigirse a enzimas específicas que controlan la división celular. Estas características las convierten en candidatos atractivos contra el cáncer, pero la misma reactividad y complejidad estructural las hace difíciles de sintetizar y poco estables durante el almacenamiento.
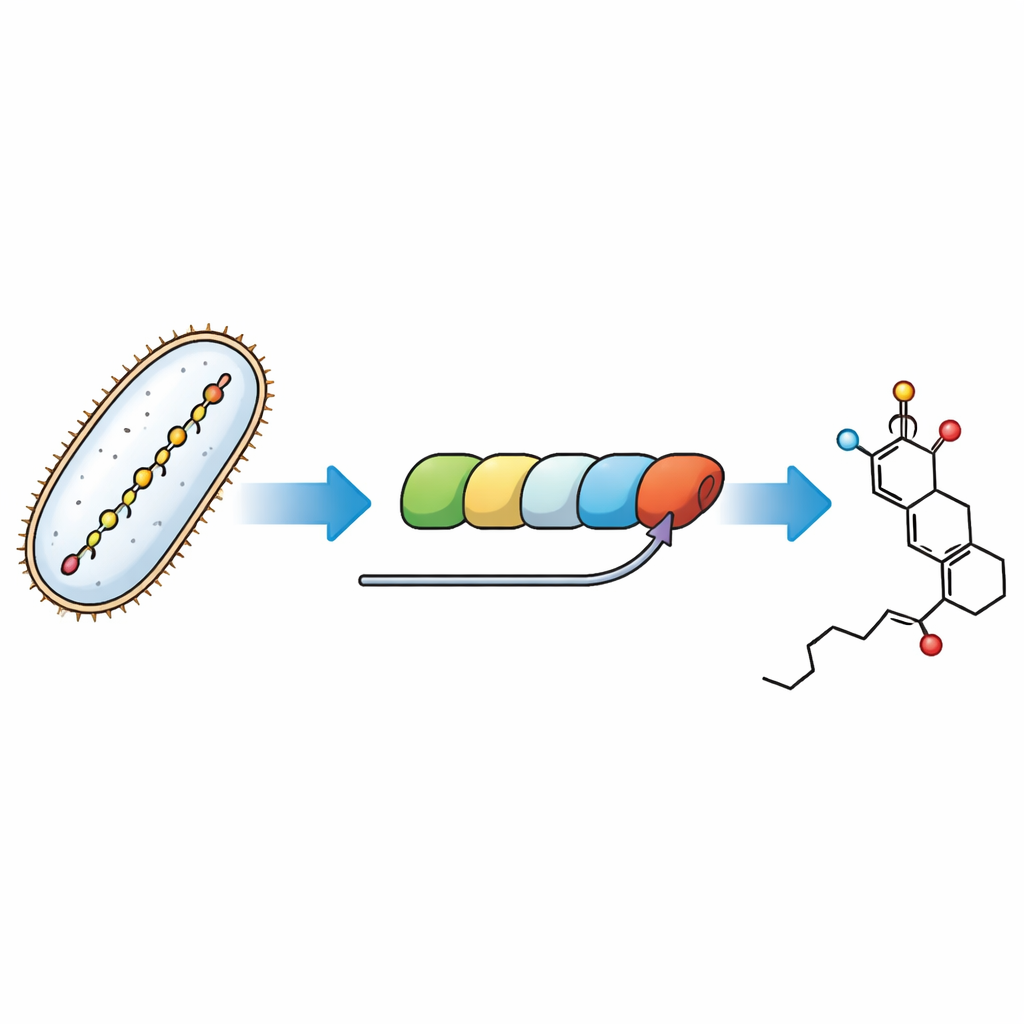
Rastreando los pasos finales de una línea de ensamblaje molecular
Las bacterias construyen la fostriecina usando una enorme máquina proteica modular llamada sintasa de poliquétidos: una línea de ensamblaje donde cada estación alarga y moldea una cadena carbonada en crecimiento. El enigma que aborda aquí es cómo el último módulo de esta máquina forja el anillo del núcleo y coloca un “asa” temporal llamada grupo malonilo que luego debe eliminarse. Recreando la vía en tubos de ensayo con enzimas purificadas y análogos pequeños diseñados para imitar los intermedios naturales, los investigadores pudieron observar pasos individuales y asignarlos a partes concretas de la línea de ensamblaje.
Una enzima multitarea con un talento inesperado
El equipo descubrió que la estación final de la línea de ensamblaje, un dominio denominado FosTE, actúa de una manera no vista hasta ahora. Las versiones típicas de este dominio simplemente liberan los productos terminados de la línea. FosTE, en cambio, primero toma un fragmento malonilo de un bloque celular común y lo transfiere a un oxígeno concreto de la cadena en crecimiento, y luego ayuda a que la cadena se pliegue para cerrarse formando el anillo del núcleo. La mutación de una sola serina reactiva en FosTE inactiva ambas actividades. Los modelos estructurales señalan a dos residuos de arginina con carga positiva en el sitio activo que acunan el fragmento malonilo y lo posicionan para la transferencia —funciones que normalmente desempeña otro tipo de enzima. Cambiar esas argininas por residuos neutros elimina el paso de transferencia del malonilo mientras que la formación básica del anillo queda en gran medida intacta, lo que confirma su papel crítico.
Fijar el núcleo y prevenir pérdidas
Una vez que el anillo se forma y porta su grupo malonilo temporal, otra enzima, FosM, debe eliminar ese grupo para revelar el núcleo plenamente armado. El estudio muestra que FosM trabaja con eficacia solo después de que otra enzima, una quinasa de amplia especificidad llamada FosH, añada un fosfato en una posición próxima de la molécula. Cuando los investigadores suministraron el anillo malonilado solo a FosM, la conversión fue modesta. Añadir primero a FosH condujo a la eliminación casi completa del malonilo y a la formación de la unidad reactiva final. Es importante que FosH también pueda fosforilar intermediarios “desvío” relacionados que surgen de reacciones laterales, rescatándolos para que puedan procesarse correctamente en lugar de perderse como productos sin salida.
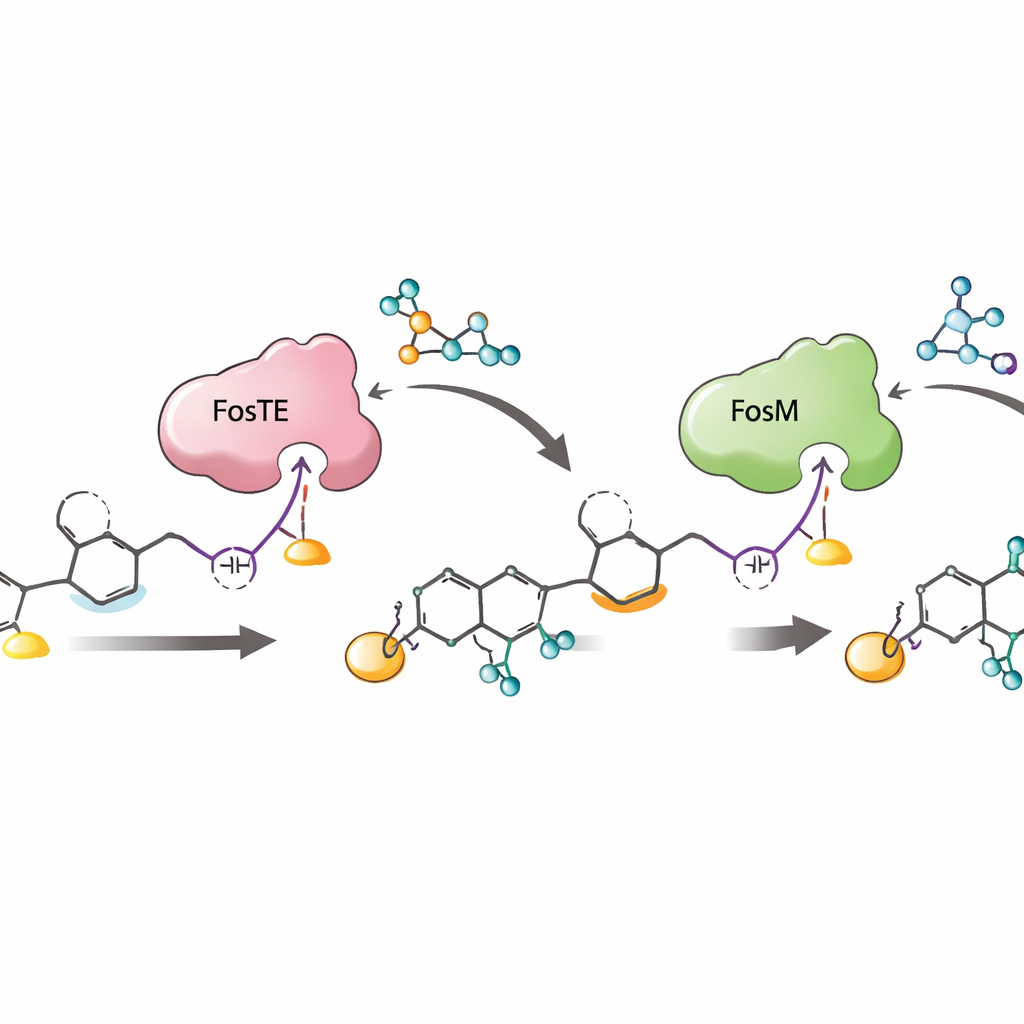
Por qué importa esta coreografía enzimática
En conjunto, el trabajo revela una secuencia cuidadosamente coreografiada: extensión de la cadena en la línea de ensamblaje, adición de malonilo y cierre del anillo impulsados por FosTE, fosforilación por FosH y, finalmente, la eliminación del malonilo promovida por FosM. Este orden no solo construye el delicado núcleo de forma eficiente, sino que también protege a los intermedios inestables de descomponerse y maximiza la producción de la forma fosforilada deseada, que es la más activa como candidato farmacológico. Al mostrar cómo un único dominio enzimático puede tanto decorar como liberar una molécula en crecimiento —y cómo enzimas asociadas afinan y rescatan intermedios reactivos— el estudio ofrece un plano para diseñar nuevos poliquétidos con núcleos reactivos y para construir rutas sintéticas más cortas y eficientes hacia agentes anticancerígenos complejos como la fostriecina.
Cita: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Palabras clave: fostriecina, biosíntesis de poliquétidos, ingeniería enzimática, núcleos reactivos de productos naturales, síntesis chemoenzimática