Clear Sky Science · es
Regulación de la traducción mediante desulfuración oxidativa de modificaciones en el ARNt
Cómo las células ajustan la producción de proteínas bajo estrés
Cada célula debe decidir qué proteínas producir, con qué rapidez y cuándo desacelerar. Este estudio revela un interruptor químico sutil en moléculas de ARN de transferencia (ARNt) que ayuda a las células a reducir la producción proteica cuando el entorno celular se vuelve más oxidante, como durante la inflamación o el estrés metabólico. Al observar cómo se comporta este interruptor en células de mamífero y en sistemas de tubo de ensayo, los investigadores descubren una nueva forma en que cambios similares al daño en el ARN pueden servir en realidad como una señal reguladora.
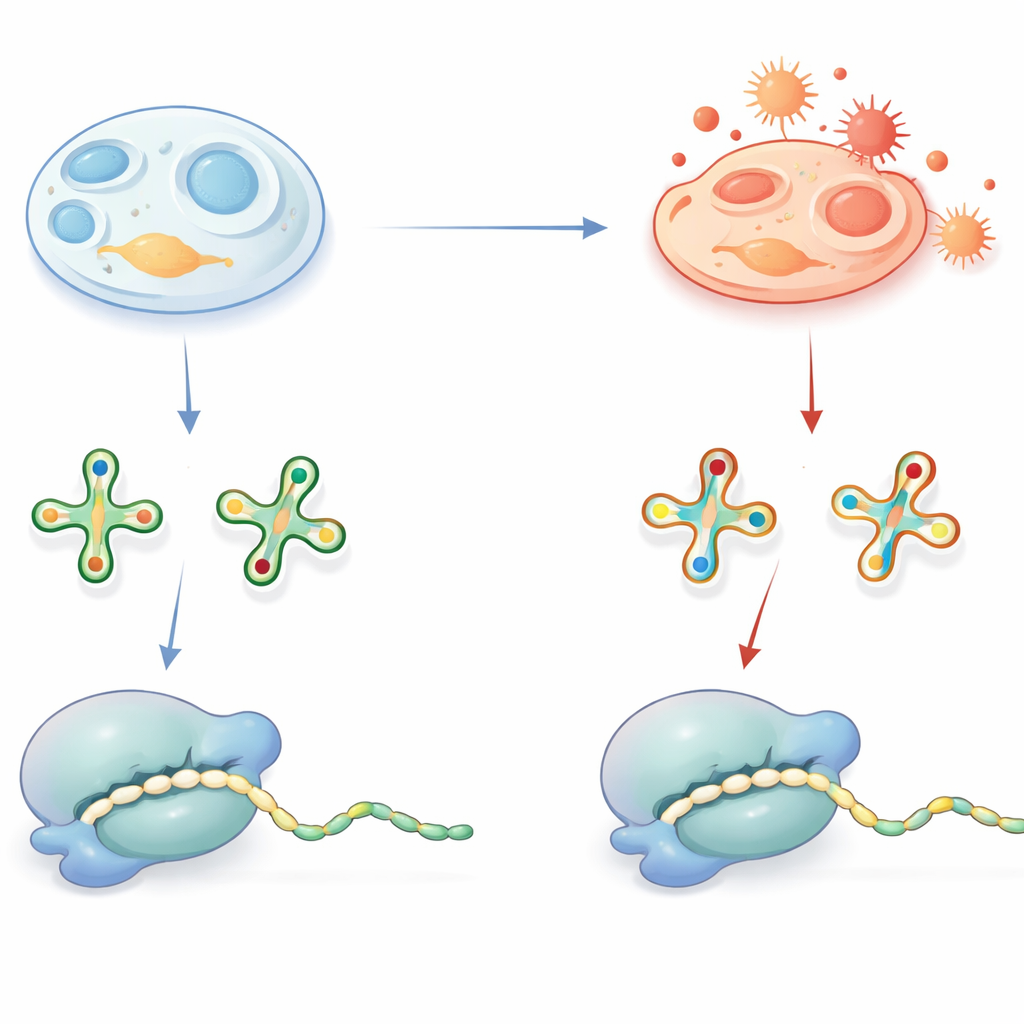
Marcas pequeñas en el ARNt con grandes consecuencias
Los ARNt actúan como adaptadores que leen “palabras” de tres letras en el ARNm y entregan los aminoácidos correspondientes durante la síntesis de proteínas. Para realizar este trabajo con precisión y eficiencia, muchos ARNt llevan decoraciones químicas especiales, sobre todo en una posición clave que contacta la tercera letra de cada codón. Una decoración extendida es un grupo que contiene azufre sobre una base uridina, a menudo escrito como una derivada de 2-tio-uridina. En condiciones saludables, este grupo de azufre ayuda al ARNt a reconocer los codones correctos que terminan en A o G y favorece una traducción rápida y sin errores. Ya se sabe que defectos en estas decoraciones causan enfermedades humanas, lo que subraya su importancia.
Cuando el estrés oxidativo reescribe el ARNt
El grupo de azufre que mejora la decodificación tiene un inconveniente: es químicamente vulnerable a la oxidación. El equipo se preguntó si, dentro de las células, este grupo se está realmente eliminando bajo condiciones oxidativas y qué significaría eso para la síntesis de proteínas. Empleando espectrometría de masas sensible, identificaron versiones oxidadas y sin azufre de estas bases de ARNt—llamadas derivadas h2U—en tejidos de ratón, mitocondrias de cerdo, bacterias, levaduras y una variedad de líneas celulares humanas. Un experimento ingenioso de spike-in con un trazador de ARNt bacteriano mostró que estas marcas h2U no son artefactos creados durante la preparación de muestras, sino que se forman dentro de las células vivas. Aunque las versiones oxidadas estaban presentes solo en una fracción de los ARNt, su abundancia varió entre tejidos y tipos celulares, lo que sugiere que el estado redox celular y la capacidad antioxidante influyen en la frecuencia de esta conversión.
Cómo los ARNt oxidados frenan la cadena de montaje
Los investigadores pusieron a prueba cómo rinden estos ARNt alterados durante la síntesis de proteínas. Convirtieron químicamente la forma que contiene azufre a la forma oxidada h2U en ARNt en masa y usaron un sistema de traducción humana completamente reconstituido in vitro. Una proteína reportera cuya producción depende en gran medida de estos ARNt modificados mostró una fuerte reducción de producción cuando los ARNt fueron desulfurizados, mientras que un reporte de control que evita los codones afectados se tradujo con normalidad. Ensayos bioquímicos revelaron la razón: los ARNt oxidados para lisina, glutamina y glutamato se cargaron con sus aminoácidos con mucha menos eficiencia, mientras que los ARNt correspondientes a arginina quedaron en gran medida preservados. Es importante que los ARNt portadores de h2U todavía aparecieron en fracciones ribosomales (polisomales) de células, lo que indica que sí participan en la traducción, pero lo hacen con poca eficacia.
Una visión estructural de la decodificación debilitada
Para ver exactamente cómo la oxidación cambia la decodificación, el equipo utilizó microscopía electrónica criogénica de alta resolución para obtener imágenes de ribosomas bacterianos programados con ARNt humano de lisina y codones específicos. En el estado normal con azufre, la base modificada en la posición de “cojeo” del ARNt formaba ya sea un par de bases estándar con un codón que termina en A o un par de cojeo especial con un codón que termina en G, ambos firmemente alojados en el centro de decodificación del ribosoma. Después de la desulfuración, la misma base pudo hacer solo un contacto débil con el codón que termina en A y formó un par de cojeo menos estable con el codón que termina en G. Experimentos de unión coincidieron con estas estructuras: el ARNt de lisina oxidado perdió esencialmente la capacidad de reconocer el codón AAA y reconoció el codón AAG con mucha menos eficiencia. En conjunto, estos hallazgos muestran que un ajuste químico aparentemente pequeño puede traducirse en desaceleraciones específicas de codones en la síntesis de proteínas.
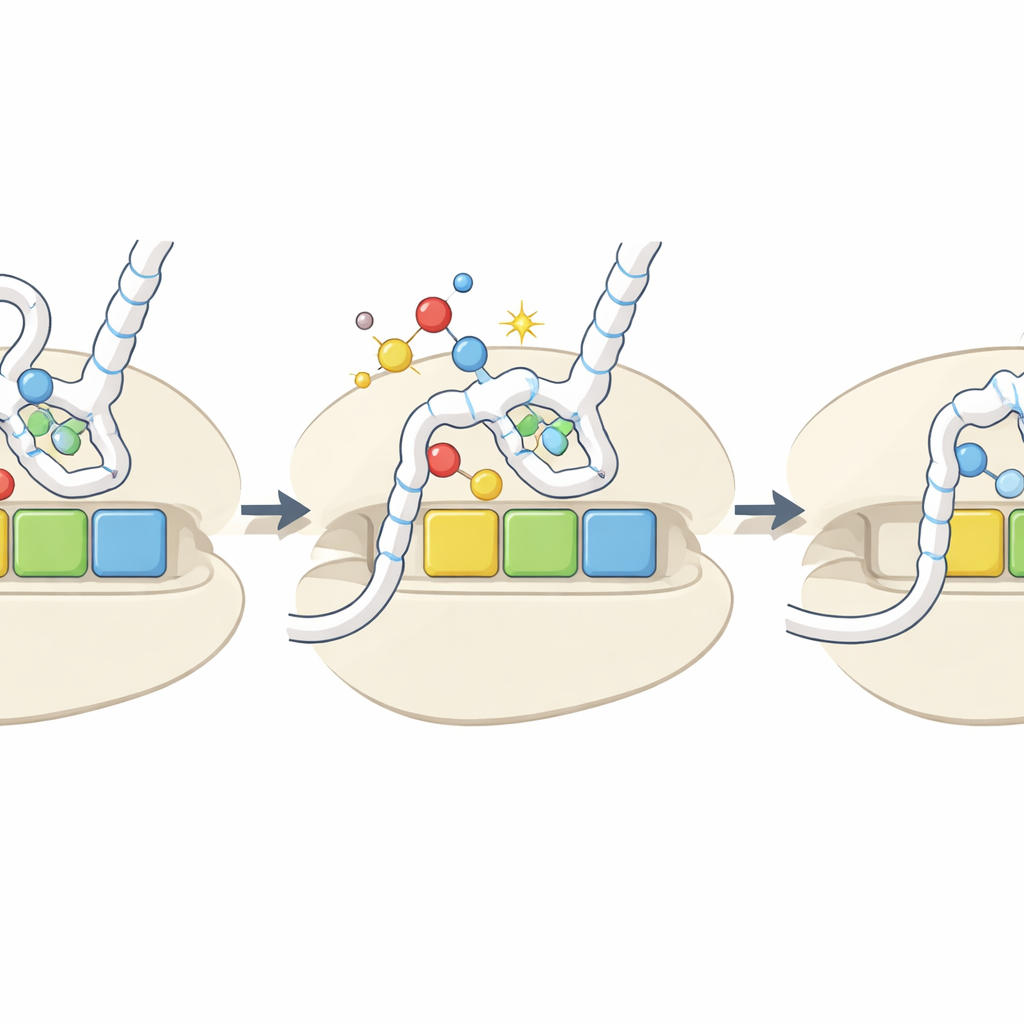
Una señal de daño que se convierte en un mando regulador
En conjunto, el estudio propone que la eliminación oxidativa del azufre de bases clave del ARNt actúa como un sensor integrado del entorno redox de la célula. Bajo estrés oxidativo, más ARNt se convierten a la forma h2U, que se cargan mal y se unen débilmente a ciertos codones. Esto ralentiza selectivamente la traducción en esos codones, lo que puede alterar la estabilidad de los ARNm afectados, cambiar el plegamiento de las proteínas y activar vías de respuesta al estrés cuando los ribosomas se paralizan. Aunque las marcas oxidadas son relativamente raras y sus niveles no siempre aumentan drásticamente bajo estrés experimental, sus efectos específicos por codón y por aminoácido significan que incluso cambios modestos podrían remodelar qué proteínas se sintetizan y a qué velocidad durante condiciones desafiantes.
Cita: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Palabras clave: modificación del ARNt, estrés oxidativo, síntesis de proteínas, regulación de la traducción, daño en el ARN