Clear Sky Science · es
Apuntar al uso de tirosina dependiente de ARNt revela una vulnerabilidad metabólica en el carcinoma hepatocelular
Privar a las células cancerosas de un bloque de construcción común
Las células del cáncer de hígado, como todas las células que se dividen rápidamente, necesitan un suministro constante de aminoácidos, los pequeños bloques que forman las proteínas. Este estudio revela que el carcinoma hepatocelular, la forma más común de cáncer de hígado, tiene una debilidad inesperada: depende en gran medida del aminoácido tirosina tanto para la producción de energía como para la supervivencia. Al limitar selectivamente cómo usan las células cancerosas la tirosina, los investigadores lograron ralentizar el crecimiento tumoral, dañar las centrales energéticas de las células cancerosas y desencadenar una forma de muerte celular que podría aprovecharse para nuevos tratamientos.
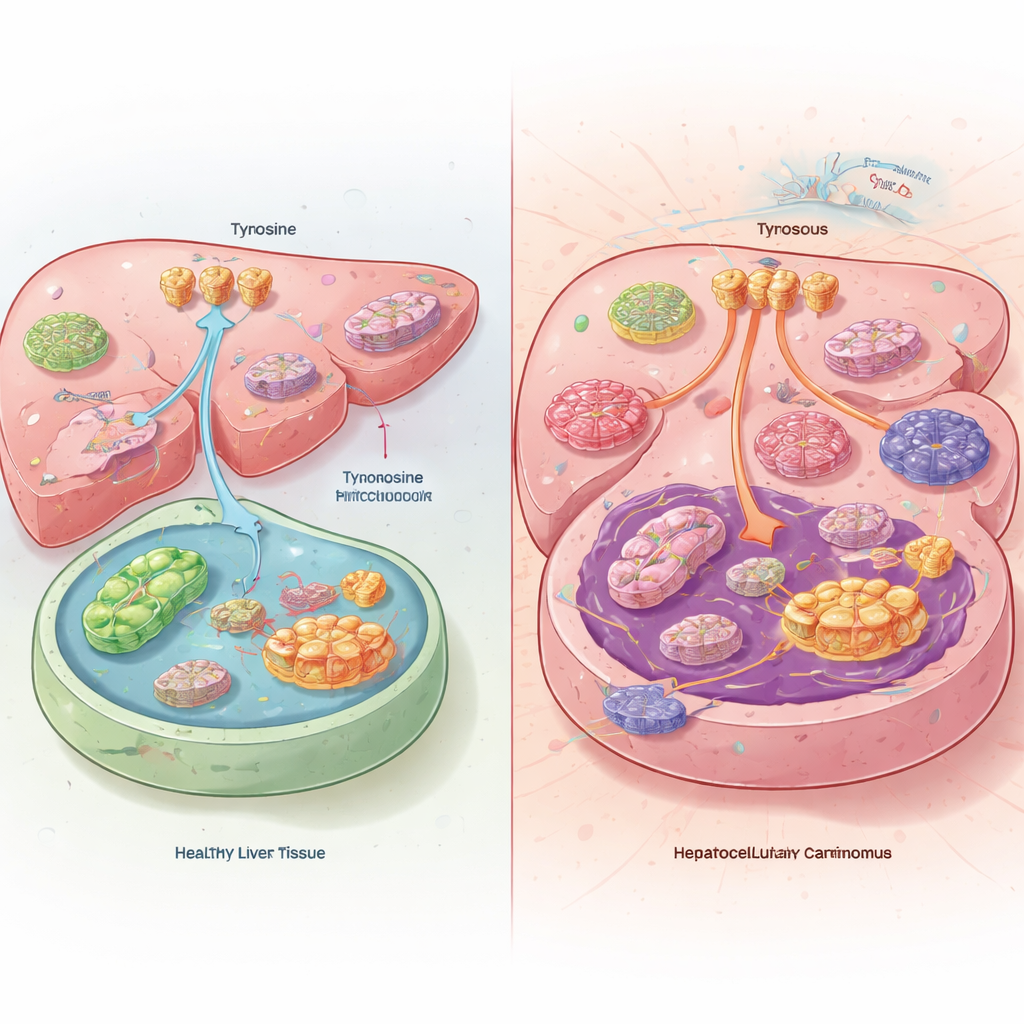
Un desequilibrio oculto en los tumores hepáticos
Cuando el equipo comparó tumores hepáticos con tejido hepático saludable de pacientes y ratones, encontraron algo desconcertante. Dentro de las células cancerosas, los niveles de tirosina eran en realidad bajos, a pesar de que los tumores captaban más tirosina desde el torrente sanguíneo y la degradaban menos. En lugar de quemar la tirosina como combustible, los tumores hepáticos la recondujeron hacia la producción de proteínas. Los cánceres lograron esto aumentando la actividad de los transportadores de tirosina en la superficie celular y reduciendo las enzimas que normalmente descomponen la tirosina en el hígado. Los ratones alimentados con una dieta sin tirosina desarrollaron tumores más pequeños y vivieron más tiempo, mientras que un exceso de tirosina en la dieta aceleró el crecimiento tumoral.
Cómo el cáncer reprograma la producción de proteínas
Los investigadores rastrearon este apetito por la tirosina hasta un potente gen impulsor del cáncer llamado MYC. En los tumores hepáticos, MYC activa una proteína denominada YARS1, que une la tirosina a un ARN de transferencia específico (tRNA-TyrGUA). Este ARNt cargado es lo que los ribosomas necesitan para construir proteínas ricas en tirosina. El estudio mostró que los cánceres de hígado aumentan tanto YARS1 como su ARNt correspondiente, asegurando una vía privilegiada de tirosina hacia la síntesis proteica. Interrumpir esta vía—ya sea reduciendo los niveles de tirosina, inhibiendo YARS1 o tRNA-TyrGUA, o bloqueando la carga de tirosina—redujo drásticamente la capacidad de las células de cáncer de hígado en cultivos y en ratones, revelando una vulnerabilidad metabólica estrechamente ligada a sus altas necesidades de producción proteica.
Paralizar las centrales energéticas y el equilibrio lipídico
Al combinar mediciones a escala genómica de ARN, producción proteica y metabolitos, el equipo identificó dos blancos especialmente sensibles a la restricción de tirosina. Uno, NDUFB8, es un componente del complejo I mitocondrial, una parte central de la maquinaria generadora de energía de la célula. El otro, SCD1, ayuda a convertir grasas saturadas en grasas monoinsaturadas que son más seguras para almacenar en membranas y en gotas lipídicas. Cuando se restringió la tirosina destinada a la traducción, la producción de NDUFB8 y SCD1 disminuyó, mientras que sus niveles de ARN se mantuvieron en gran medida sin cambios—evidencia clara de que lo que se veía afectado era la traducción, no la expresión génica. Esto condujo a un ensamblaje deficiente del complejo I, reducción de la respiración celular, exceso de especies reactivas de oxígeno y un cambio en los lípidos desde formas monoinsaturadas hacia formas poliinsaturadas más frágiles y fácilmente oxidadas.
Forzar a las células cancerosas hacia una muerte dependiente del hierro
El daño mitocondrial combinado y los lípidos inestables empujaron a las células del cáncer de hígado hacia la ferroptosis, una forma de muerte celular dependiente del hierro impulsada por la peroxidación lipídica. Los tumores intentaron defenderse aumentando bloqueadores naturales de la ferroptosis como GPX4 y moléculas relacionadas, pero una amplia pantalla CRISPR mostró que desactivar estos protectores hacía que la restricción de tirosina fuera aún más letal. En modelos celulares y en ratones, combinar estrategias de limitación de tirosina con fármacos que inhiben GPX4 o BCL2—o con fármacos ya usados en cáncer de hígado como sorafenib y venetoclax—produjo un mayor control tumoral, menores cargas tumorales y supervivencias más largas.
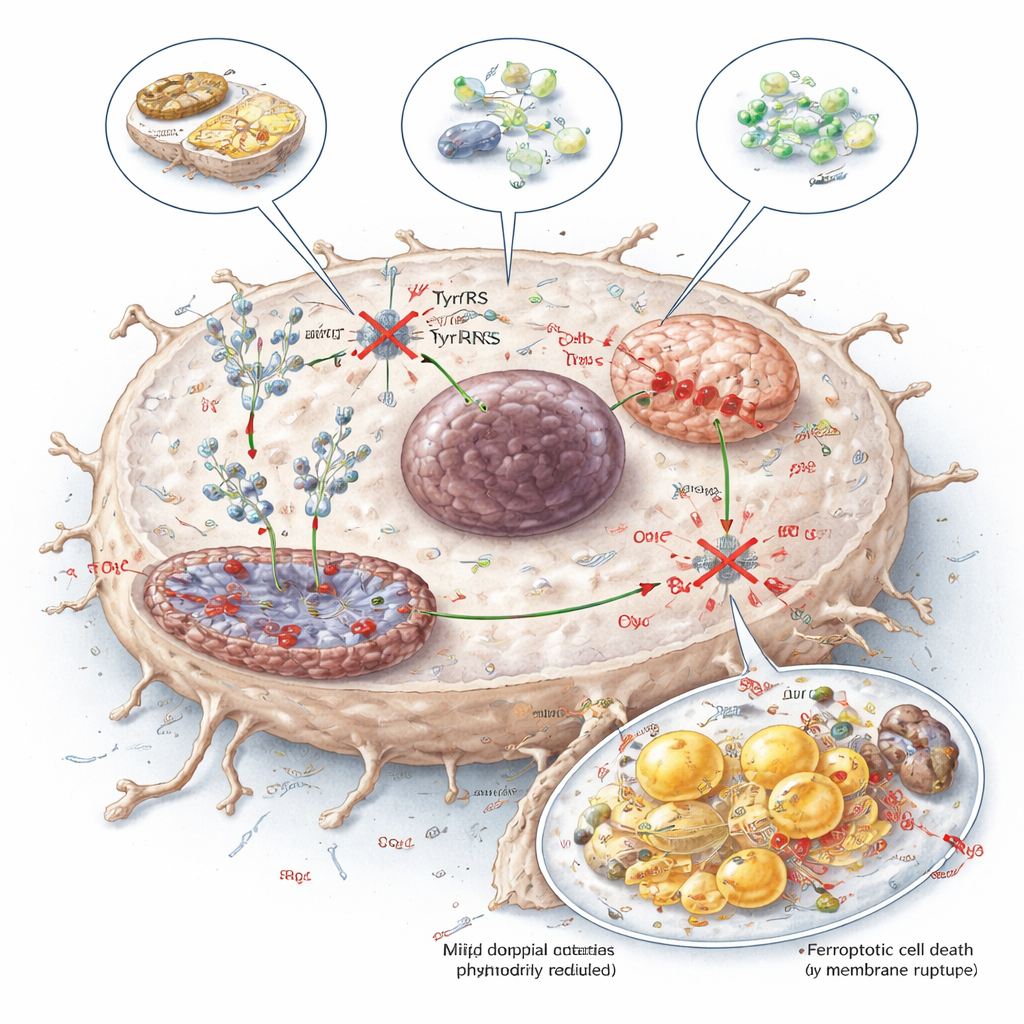
Convertir una debilidad metabólica en terapia
Para explorar formas prácticas de explotar esta debilidad, los investigadores probaron tres enfoques: una dieta restringida en tirosina, una enzima (TAL) que degrada enzimáticamente la tirosina, y una pequeña molécula llamada tirosinol que compite con la tirosina por la unión a YARS1. Los tres redujeron la disponibilidad de tirosina para la síntesis proteica, disminuyeron los niveles de NDUFB8 y SCD1, dañaron la función mitocondrial e incrementaron la ferroptosis en tumores hepáticos, mostrando al mismo tiempo efectos manejables sobre los tejidos normales en ratones. Para el público general, el mensaje es que los cánceres de hígado parecen depender de la tirosina no solo como nutriente, sino como un combustible preciso para su maquinaria de fabricación de proteínas. Dirigir esta dependencia—mediante dieta, enzimas o fármacos—ofrece una vía prometedora para debilitar los tumores y aumentar el efecto de los tratamientos existentes.
Cita: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Palabras clave: cáncer de hígado, metabolismo de aminoácidos, tirosina, mitocondrias, ferroptosis