Clear Sky Science · es
Identificación sistemática de interacciones entre pequeñas moléculas y estructuras de ARN específicas de variantes ejemplificada por los G-cuádruplex de ARN
Por qué importan los pequeños cambios en el ARN para las medicinas del futuro
La mayoría de nosotros heredamos pequeñas diferencias en nuestro ADN que nos hacen únicos. Estos minúsculos cambios pueden remodelar de forma sutil los pliegues de las moléculas de ARN dentro de nuestras células. El nuevo estudio presenta una forma de ver cómo esos ajustes genéticos alteran el agarre de fármacos experimentales que se dirigen al ARN. Esto es importante porque el mismo medicamento podría comportarse de manera muy distinta de una persona a otra, sobre todo en cánceres o enfermedades genéticas.
Nueva forma de ver dónde tocan los fármacos el ARN
Muchos desarrolladores de fármacos están ahora explorando el ARN, no solo las proteínas, como diana terapéutica. Las pequeñas moléculas pueden fijarse a formas especiales del ARN e influir en cómo se lee la información genética, pero hasta ahora la mayoría de los métodos solo funcionaban sobre una secuencia “de referencia”. En gran medida han ignorado los incontables cambios de una sola letra presentes en pacientes reales. Los autores crearon un enfoque de alto rendimiento llamado BIVID-MaP que puede evaluar simultáneamente miles de variantes de ARN y localizar dónde se une una pequeña molécula a cada una, con resolución de un solo nucleótido. 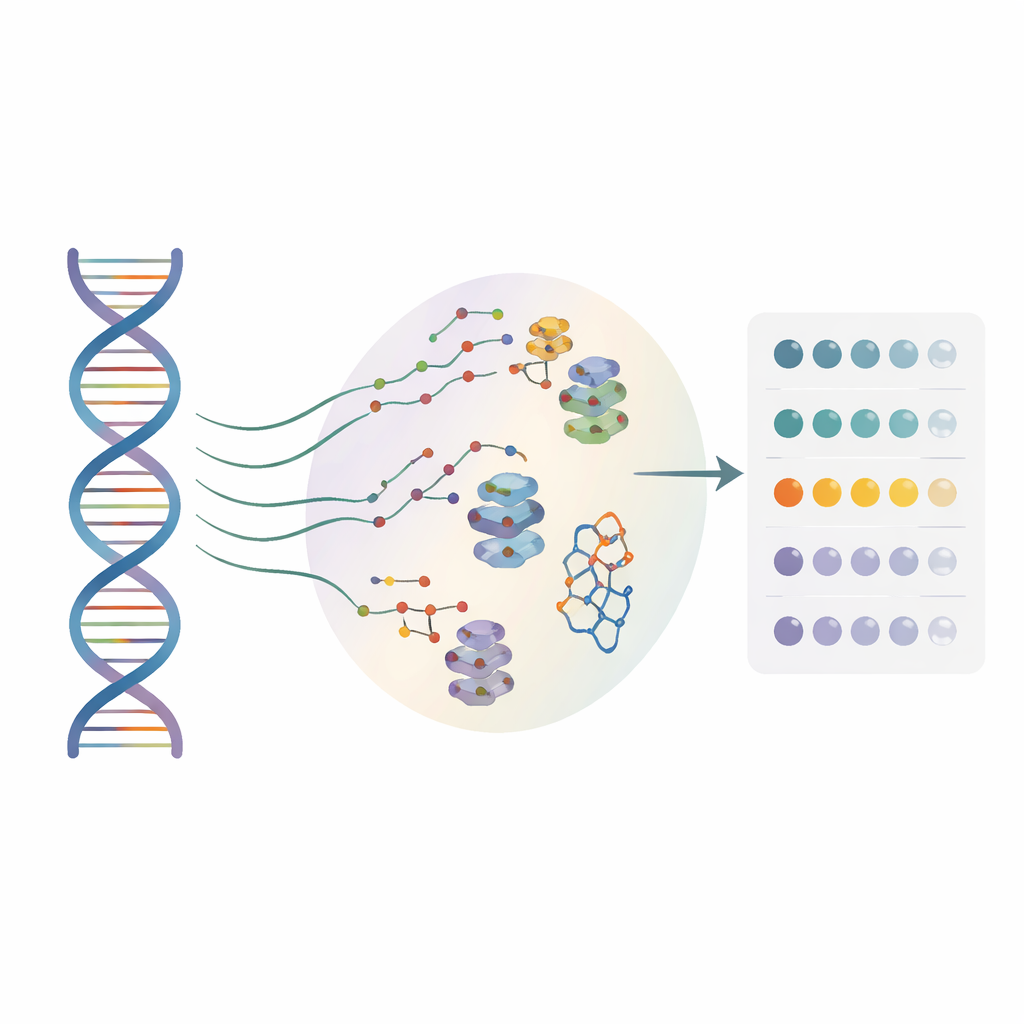
Convertir marcas químicas en una señal legible
BIVID-MaP funciona en tres pasos principales. Primero, el equipo añade una etiqueta reactiva a una pequeña molécula que se une al ARN. Cuando este compuesto etiquetado se acomoda en su estructura de ARN preferida, como un G-cuádruplex compacto formado por secuencias ricas en guanina, la etiqueta forma un enlace químico permanente con una base de ARN cercana. Segundo, una enzima especial copia el ARN modificado a ADN. Al encontrar una de estas marcas químicas, tiende a “saltar” una base, creando una pequeña deleción en la copia. Tercero, la secuenciación profunda lee estas firmas de deleción en millones de moléculas. Dado que casi toda la secuencia circundante se conserva, las deleciones pueden asignarse con precisión a variantes genéticas específicas en una mezcla.
Demostrar el método en un caso de control
Para confirmar que BIVID-MaP detecta verdaderamente la unión específica de variantes, los investigadores estudiaron un segmento de ARN del gen CD44 que normalmente forma un G-cuádruplex. Un único cambio de G a A interrumpe esta estructura. En una mezcla que contenía ambas versiones, solo la forma intacta mostró señales fuertes de deleción cerca de la región plegada cuando se expuso a una sonda basada en berberina, y ensayos independientes verificaron una unión más fuerte allí. El mutante, que no puede formar la misma estructura, produjo muchas menos deleciones y una unión más débil. Otras técnicas comunes de mapeo bien pasaron por alto esta diferencia o generaron ruido confuso, lo que subraya la mayor sensibilidad y especificidad del nuevo enfoque.
Explorar mutaciones vinculadas al cáncer en muchos genes
El equipo amplió luego el alcance. Construyeron una biblioteca de ARN de regiones no traducidas 5′ (5′ UTR) de 283 genes relacionados con el cáncer, cada una emparejada con mutaciones somáticas reales reportadas en tumores. Usando una sonda que reconoce estructuras tipo G-cuádruplex, BIVID-MaP reveló numerosas mutaciones que fortalecieron o debilitaron la unión de pequeñas moléculas. En genes como DAXX e ING2, cambios de una sola letra en tramos ricos en guanina alteraron notablemente la unión, en consonancia con pruebas biofísicas independientes de formación de G-cuádruplexes y mediciones directas de unión por espectrometría de masas. En algunos casos, mutaciones fuera de las tramas evidentes de G aún desplazaron la unión al cambiar sutilmente la probabilidad de apareamiento de bases cercanas, remodelando el “conjunto” estructural sin alterar gruesamente el plegamiento previsto en términos generales. 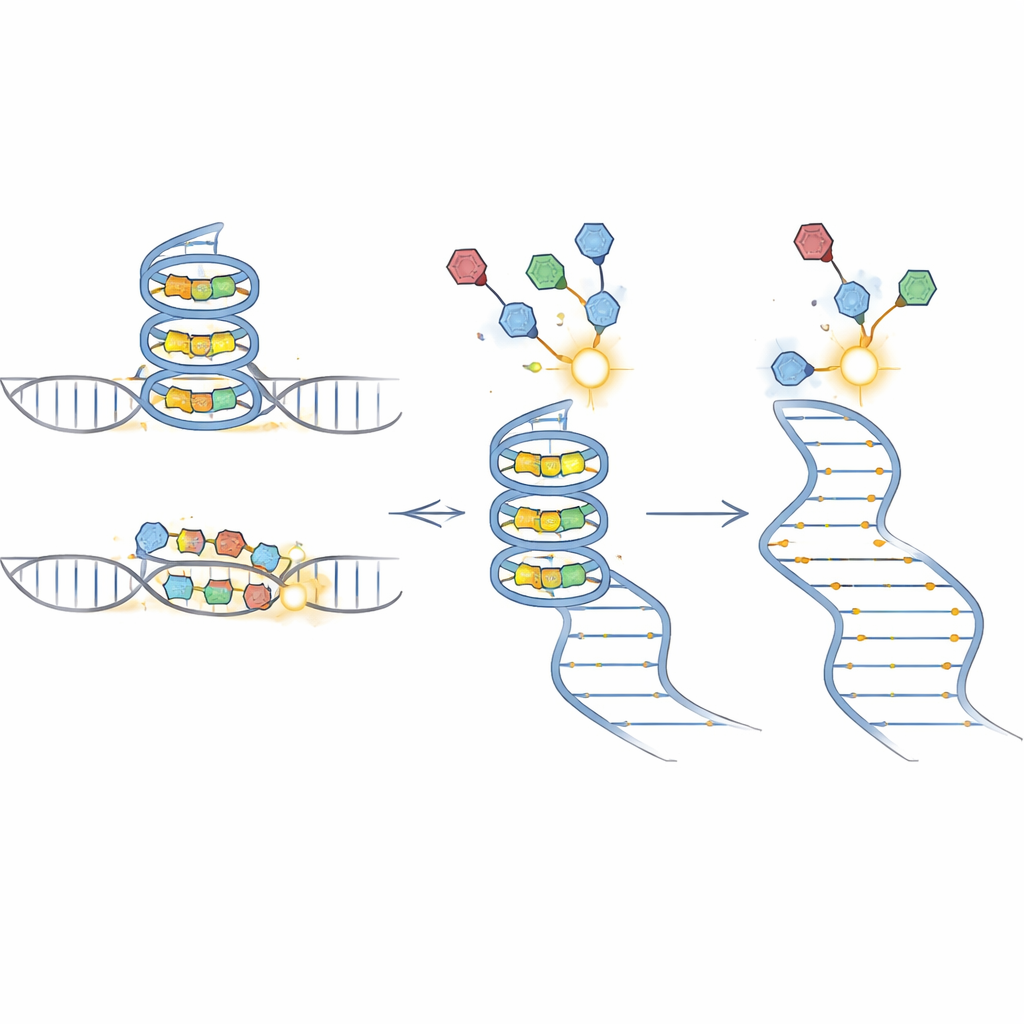
Ver lo que las predicciones por ordenador no detectan
Es importante señalar que las herramientas existentes de predicción de estructura de ARN y de G-cuádruplexes con frecuencia no previeron los cambios que BIVID-MaP puso de manifiesto. Algunas variantes que apenas modificaban las puntuaciones computacionales produjeron grandes diferencias reales en la unión. Otras parecían afectar la unión frente a una familia de compuestos que apuntan a G-cuádruplexes, mientras que ciertas mutaciones tuvieron efectos específicos para determinados fármacos. Esto demuestra que las variantes de un solo nucleótido pueden afinar el paisaje de los pliegues del ARN y los contactos con fármacos de maneras difíciles de inferir solo a partir de la secuencia.
Qué significa esto para los fármacos personalizados dirigidos al ARN
Los autores concluyen que BIVID-MaP ofrece una vía poderosa para mapear cómo las diferencias genéticas individuales remodelan las estructuras de ARN y sus interacciones con pequeñas moléculas farmacológicas. Al convertir modificaciones químicas locales en firmas precisas de deleción, el método puede sondear miles de variantes en paralelo y destacar aquellas que cambian de forma significativa la unión de fármacos. A largo plazo, tales mapas podrían guiar el diseño de medicinas dirigidas al ARN más eficaces y seguras en pacientes diversos, y revelar estructuras de ARN hasta ahora ocultas que podrían servir como nuevas dianas terapéuticas.
Cita: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Palabras clave: Fármacos dirigidos al ARN, G-cuádruplex, variantes genéticas, unión de pequeñas moléculas, mutaciones en el cáncer