Clear Sky Science · es
Optimización de la organización espacial de anillos FtsZ para una constricción a gran escala en células sintéticas
Por qué importan los anillos diminutos para construir células sintéticas
Imagínese construir una célula artificial y sencilla que pueda crecer y dividirse por sí sola. Para lograrlo, los científicos deben aprender a pellizcar una membrana blanda, similar a una burbuja de jabón, de forma controlada usando solo unas pocas piezas biológicas. Este estudio muestra cómo una proteína bacteriana puede ser ayudada a formar anillos grandes y estables sobre enormes gotículas lipídicas, permitiendo que estas «células» modelo se contraigan casi hasta la división. Revela qué tipo de arquitectura proteica se necesita para doblar y remodelar una membrana a la escala de una célula completa.
Tomando prestada la caja de herramientas de la división natural
Muchas bacterias se dividen usando una proteína llamada FtsZ, un pariente lejano de la tubulina que construye el esqueleto interno de nuestras propias células. FtsZ se ensambla en filamentos que se agrupan en un anillo en el punto medio de la célula, marcando dónde se separará. En bacterias vivas, una multitud de proteínas auxiliares anclan este anillo a la membrana interna, lo posicionan en el centro y lo conectan con enzimas que remodelan la pared celular. Intentos previos en laboratorio de recrear esta maquinaria dentro de vesículas de tamaño celular lograron formar anillos y provocar pequeñas hendiduras en la membrana, pero no una constricción suave y progresiva que remodelara una vesícula gigante en dos mitades casi separadas.
Un enfoque minimalista para una cáscara divisoria
Los autores se preguntaron si podían reducir este sistema a apenas dos piezas: una versión de FtsZ que puede adherirse directamente a membranas, y una cola corta con carga positiva de otra proteína de división, FtsN. Encapsularon estos componentes dentro de vesículas unilamelares gigantes —esferas huecas de lípido que asemejan células simplificadas— y les suministraron la molécula energética GTP y un análogo de GTP de acción lenta para ajustar la dinámica proteica. Sin la cola de FtsN, FtsZ formó muchos anillos diminutos y parches que solo causaban abolladuras locales. Con un exceso del fragmento de FtsN (llamado cytoFtsN), esos pequeños anillos se reorganizaron en un único anillo grande que rodeó la vesícula cerca del ecuador y pudo contraerse durante varias horas.
De una red enmarañada a un único anillo contráctil
Para entender cómo este pequeño péptido cambia tan drásticamente el comportamiento, el equipo observó filamentos de FtsZ sobre membranas soportadas planas mediante microscopía de alta resolución. Normalmente, FtsZ en esas superficies forma vórtices curvos y en espiral. Al añadir cantidades crecientes de cytoFtsN, esas espirales se borraron gradualmente y fueron reemplazadas por haces más rectos y alineados. El análisis cuantitativo de imágenes confirmó que la red se volvió más coherente y ordenada a medida que aumentaba la concentración del péptido. Experimentos de recuperación de fluorescencia mostraron que las subunidades dentro de esos haces se intercambiaban más lentamente, lo que indica que el péptido estabiliza los filamentos y reduce su dinámica de recambio.

“Velcro” electrostático que bloquea los filamentos entre sí
Mediciones bioquímicas revelaron que cytoFtsN y FtsZ interactúan principalmente mediante cargas eléctricas opuestas: FtsZ es netamente negativo, mientras que el péptido porta agrupaciones de cargas positivas. A niveles de sal más bajos, el péptido se unía con mayor fuerza, promovía la formación de haces más gruesos de FtsZ en solución y desaceleraba la descomposición de los filamentos al atenuar la actividad hidrolítica de GTP de la proteína. Cuando los investigadores cambiaron residuos clave cargados positivamente en el péptido, o aumentaron la concentración de sal para apantallar la atracción electrostática, los efectos de formación de haces y reorganización desaparecieron. Esto apunta a un mecanismo físico simple en el que el péptido cargado positivamente actúa como un “Velcro” molecular, reduciendo la repulsión entre filamentos de FtsZ para que puedan empaquetarse lado a lado en haces rígidos.
Cómo un único anillo remodela una vesícula gigante
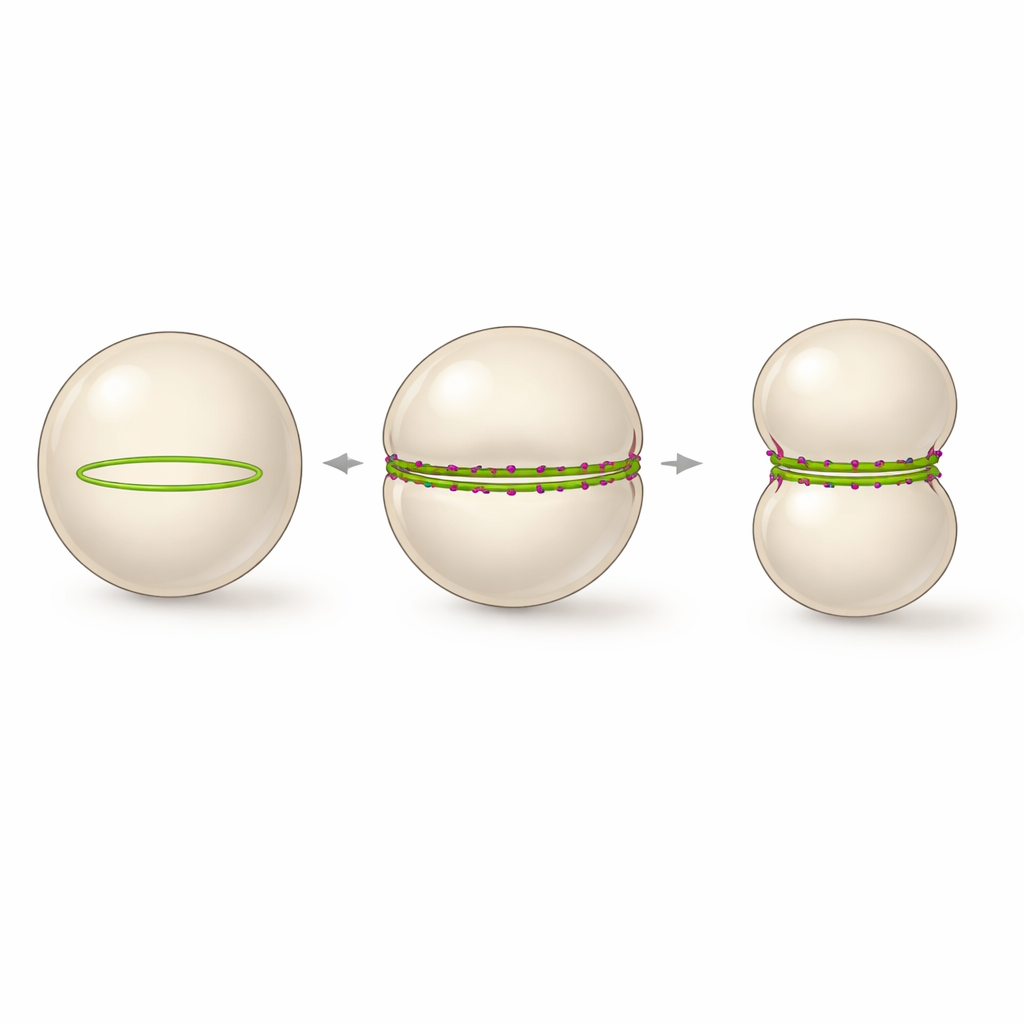
Dentro de las vesículas, este empaquetamiento estabilizado por el péptido tiene una consecuencia llamativa. En lugar de muchos pequeños anillos curvos, los haces rectificados de FtsZ se ven forzados a seguir la gran curvatura de la vesícula, ensamblándose en un único anillo continuo que abarca toda la circunferencia. Imágenes en lapso de tiempo mostraron que siempre que se formaba dicho anillo completamente cerrado, la vesícula se deformaba de forma fiable de una esfera a una forma de mancuerna, con una estrechez en la cintura donde se situaba el anillo. El proceso pudo seguirse en tiempo real mientras el diámetro de la vesícula se reducía y la constricción se profundizaba, casi dividiendo el compartimento en dos, aunque no se logró la escisión final. Los autores proponen que un anillo FtsZ estable que abarque el ecuador y con un recambio más lento pero aún activo es la arquitectura mínima necesaria para impulsar una constricción de membrana a gran escala en una célula sintética.
Qué significa esto para la vida sintética futura
Al mostrar que una variante de FtsZ anclada a la membrana más un péptido catiónico corto pueden remodelar vesículas lipídicas gigantes casi hasta la división, este trabajo define una regla de diseño clara para células artificiales: un único anillo proteico coherente que coincida con el tamaño de la célula y sea mecánicamente estable en el tiempo es suficiente para pellizcar un límite blando a escala celular. Pueden seguir siendo necesarios factores más complejos para cortar la membrana por completo, pero el estudio demuestra que una constricción controlada a gran escala no exige todo el elenco de proteínas de división bacterianas. En cambio, un ajuste cuidadoso de la organización y la dinámica de los filamentos puede convertir un andamiaje proteico simple en un anillo contráctil eficaz, acercando un paso más la posibilidad de células sintéticas que se dividan por sí mismas.
Cita: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Palabras clave: división de célula sintética, anillo FtsZ, constricción de membrana, divisoma mínimo, autoorganización del citoesqueleto</keyword:auto> <keyword>cytoskeletal self-organization