Clear Sky Science · es
El estilo de vida de Acinetobacter baumannii incluye la colonización en suelo de material vegetal en descomposición y la dispersión por aire
Por qué importa para usted el lado salvaje de este germen hospitalario
Acinetobacter baumannii es más conocido como un germen hospitalario difícil de eliminar que resiste muchos antibióticos. Este estudio muestra que el mismo microbio también lleva una vida activa al aire libre: en suelos, material vegetal en descomposición, animales e incluso en el aire. Al descubrir de dónde proviene y cómo se desplaza, el trabajo ayuda a explicar por qué esta bacteria es tan resistente y por qué con frecuencia aparece en hospitales de todo el mundo.

Vida oculta en campos, ríos y nidos de aves
Los investigadores comenzaron con una pista inesperada: los polluelos de cigüeña blanca en Polonia con frecuencia portaban A. baumannii en las vías respiratorias superiores, lejos de cualquier hospital. Siguiendo la dieta y el entorno de las aves, el equipo rastreó la bacteria no hasta insectos o peces, sino principalmente hasta pequeños mamíferos, lombrices de tierra y—lo más importante—suelos húmedos ricos en material vegetal en descomposición a lo largo de ríos y en montones de compost. Los suelos forestales, incluso junto a arroyos, raramente albergaban la bacteria, mientras que las riberas de ríos fuera de los bosques a veces actuaban como “puntos calientes” donde muchas cepas diferentes coexistían lado a lado.
De las plantas en descomposición al aire libre
Experimentos de campo cuidadosos mostraron que A. baumannii se siente atraída por el material vegetal en descomposición. Cuando los autores colocaron restos vegetales esterilizados en jardines, el material fue colonizado en pocas semanas, incluso cuando se elevó por encima del suelo y solo era accesible a través del aire. Trampas de aire situadas justo por encima de pilas de compost activas también captaron la bacteria. En trabajo de laboratorio, el equipo descubrió que A. baumannii se adhiere con facilidad a esporas de mohos comunes como Aspergillus y Penicillium. Las bacterias recubrían gradualmente las esporas e incluso ralentizaban su capacidad de germinar. Dado que las esporas fúngicas se vuelven fácilmente aerotransportadas desde composts y suelos, esta estrecha asociación ofrece una vía sencilla para que la bacteria se «suba» al aire.
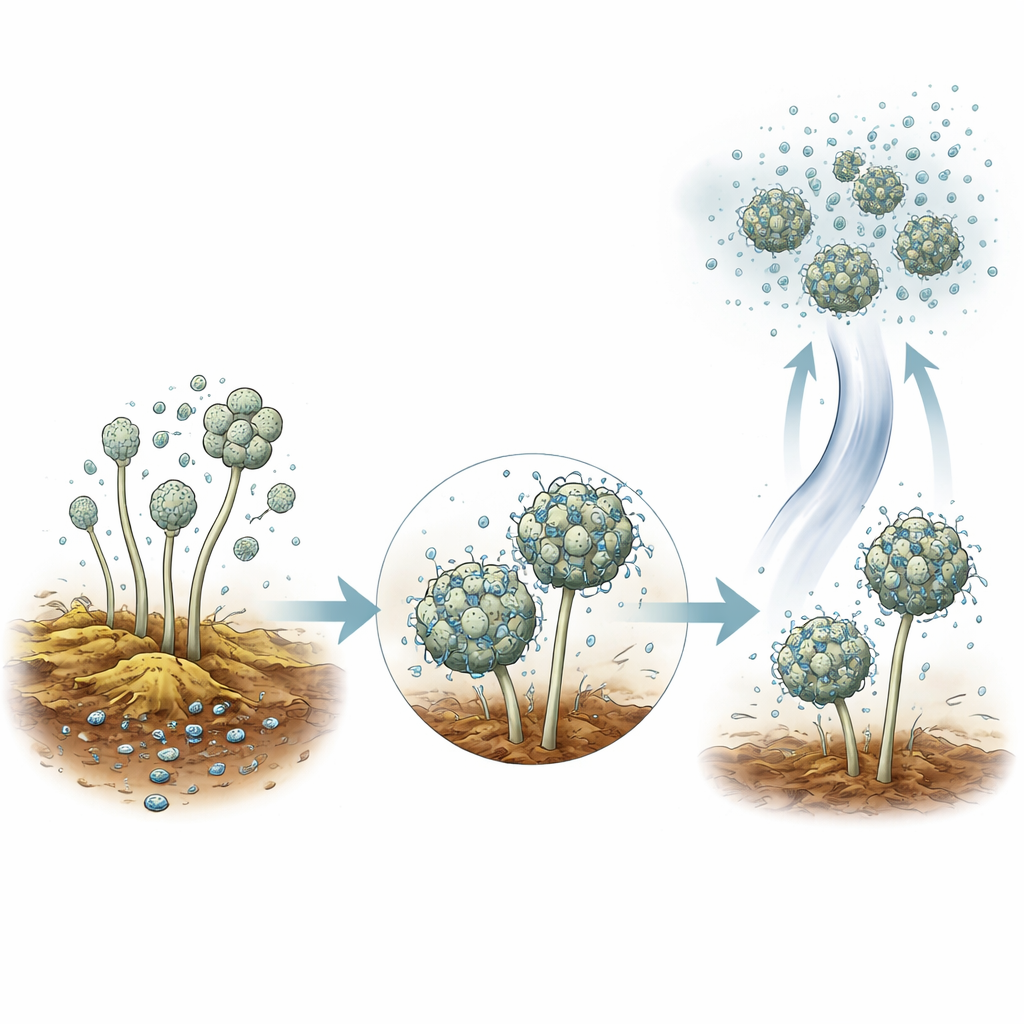
Viajeros globales con raíces antiguas
Para ver cómo se relacionan estas cepas silvestres con las hospitalarias, el equipo secuenció 401 genomas nuevos procedentes de cigüeñas, suelos, plantas, lombrices, roedores y otras fuentes, y los comparó con cientos de genomas disponibles públicamente. El árbol genealógico resultante reveló una dispersión notable: aislamientos ambientales, animales y clínicos humanos se distribuyeron a lo largo de las mismas ramas, a menudo diferenciándose por solo unos pocos cambios en el ADN. Algunos parientes casi idénticos se encontraron en distintos continentes, lo que implica que las mismas líneas habían cruzado océanos en solo unas pocas décadas. Según la tasa a la que se acumulan las mutaciones, los autores estiman que A. baumannii como especie es sorprendentemente joven—del orden de 15.000 años—y experimentó una rápida diversificación en la época en que los humanos comenzaron la agricultura a gran escala y la deforestación.
Un vasto conjunto de herramientas genéticas, pero poca huella humana en la naturaleza
Al combinar todos los genomas, los investigadores estimaron que el conjunto genético combinado de la especie—o pan-genoma—contiene aproximadamente 51.000 familias de genes distintas, más del doble de estimaciones previas. Esta enorme caja de herramientas genética probablemente subyace a su capacidad para adaptarse a la sequedad extrema, la radiación, los desinfectantes y los antibióticos. Sin embargo, la mayoría de los aislamientos de fauna y suelo solo portaban un pequeño número de genes de resistencia reconocidos y pocos elementos de ADN móvil, en contraste con las cepas hospitalarias que están cargadas de tales características. Ese patrón sugiere que las poblaciones naturales muestreadas aún están relativamente poco influenciadas por el uso moderno de antibióticos, ofreciendo una visión “de referencia” de la especie antes de su completa adaptación hospitalaria.
Qué significa esto para hospitales y salud pública
El estudio pinta a A. baumannii no como un problema puramente creado por el hombre, sino como una bacteria naturalmente aerotransportada y asociada a plantas y suelos que solo recientemente ha comenzado a explotar los hospitales y las instalaciones ganaderas como nuevos hábitats. Su asociación con hongos, su tolerancia a condiciones adversas y su inmensa diversidad genética la hacen apta para viajes atmosféricos de larga distancia y para una rápida evolución. Para el público en general, la conclusión es que el control de infecciones no puede centrarse únicamente en la transmisión de paciente a paciente dentro de los hospitales. Los picos estacionales, los ambientes interiores contaminados por moho, las instalaciones de compostaje y los cambios más amplios en el uso del suelo moldean cuándo y cómo este resistente germen llega a entornos humanos—y entender su estilo de vida al aire libre es clave para anticiparse a futuras cepas resistentes a los fármacos.
Cita: Wilharm, G., Skiebe, E., Michalska, A. et al. Acinetobacter baumannii’s lifestyle includes soil-dwelling colonization of decaying plant material and airborne spread. Nat Commun 17, 2316 (2026). https://doi.org/10.1038/s41467-026-70072-4
Palabras clave: Acinetobacter baumannii, bacterias aéreas, microbioma del suelo, resistencia a antibióticos, One Health