Clear Sky Science · es
La dinámica a nivel de una sola molécula revela que la unión de ATP por sí sola impulsa la translocación de sustrato en un transportador ABC
Por qué importan las bombas celulares diminutas
Cada célula de su cuerpo depende de máquinas microscópicas que mueven moléculas a través de membranas, determinando desde la absorción de nutrientes hasta la defensa inmunitaria. Una clase principal de estas máquinas, llamadas transportadores ABC, utiliza el combustible químico de la célula, ATP, para empujar cargas en contra de gradientes naturales. Sin embargo, durante décadas los científicos han debatido una cuestión fundamental: ¿la simple unión de ATP impulsa el paso de transporte, o la energía sólo se libera cuando el ATP se descompone? Este estudio se centra en un único transportador, molécula por molécula, para dirimir ese debate.
Vigilar un transportador a la vez
En lugar de medir el comportamiento combinado de millones de moléculas, los investigadores construyeron un montaje que les permite seguir eventos de transporte individuales en tiempo real. Se centraron en TmrAB, un pariente bacteriano del transportador humano TAP que carga péptidos inmunitarios para su presentación a células T citotóxicas. TmrAB se integra en una membrana y transporta fragmentos cortos de proteínas (péptidos) de un lado al otro usando ATP. Para ver cada paso de transporte, el equipo atrapó una sola molécula de TmrAB en una burbuja de membrana artificial (un lipoosoma) e incluyó dentro de esa burbuja una proteína “sensor” especialmente diseñada que cambia su fluorescencia cuando captura un péptido. Usando un microscopio de alta sensibilidad, pudieron entonces observar, como saltos breves en la señal luminosa, los momentos exactos en que un péptido tras otro llegaba al interior de la burbuja.
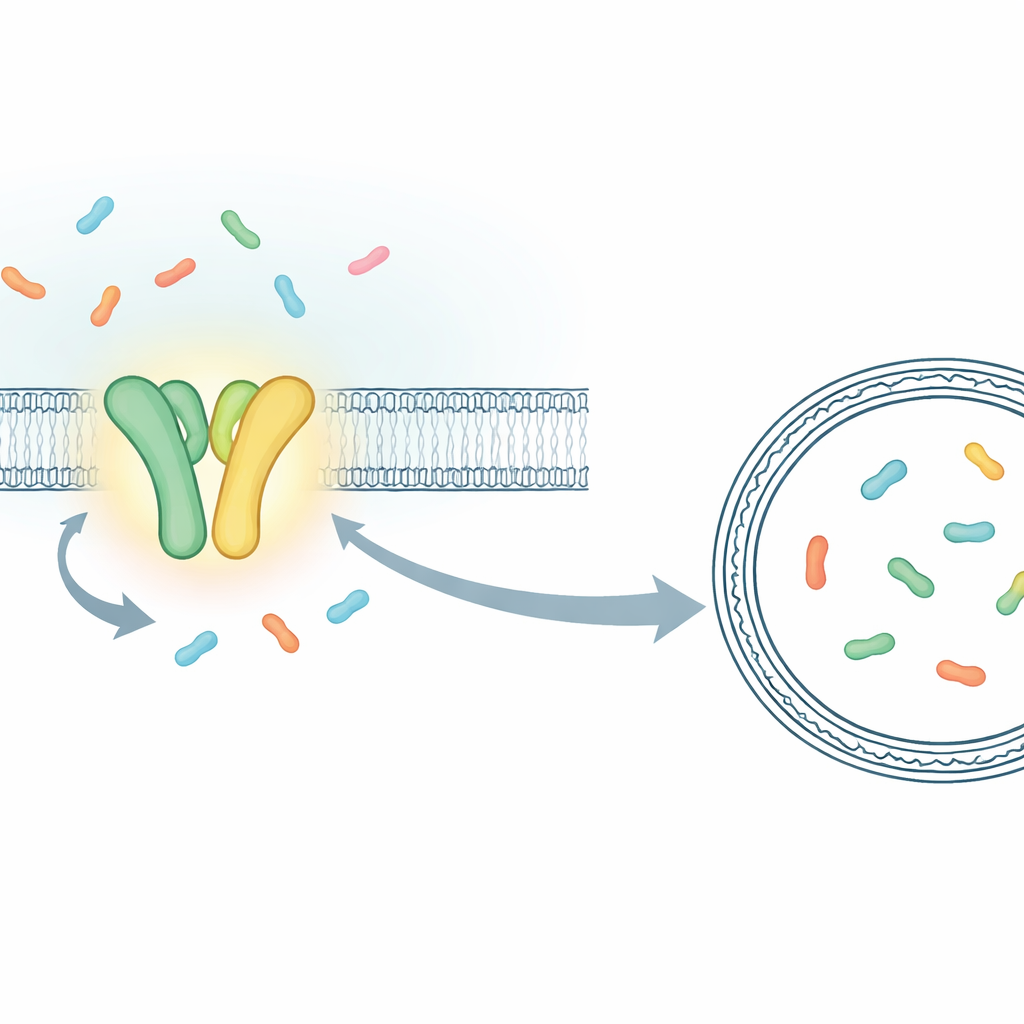
Demostrar que una unión de ATP mueve un péptido
Con este ensayo de una sola molécula en mano, los investigadores compararon el TmrAB normal con una versión modificada de baja velocidad cuyo ciclo se prolonga en el tiempo. La variante lenta hizo posible distinguir eventos individuales que de otro modo se mezclarían. Mostraron que cuando ATP y péptidos estaban presentes a la vez, el sensor dentro del lipoosoma pasaba de su estado “vacío” al estado “cargado” en pasos discretos, cada uno compatible con el transporte de un único péptido. Al analizar la rapidez con que el sensor se cerraba alrededor de los péptidos y estimar el diminuto volumen dentro de cada lipoosoma, pudieron incluso traducir esos cambios de luz en concentraciones aproximadas de péptido. Los números coincidían con lo que cabría esperar si uno y luego dos péptidos se acumulaban en burbujas de unos 100 nanómetros de diámetro, confirmando que estaban contando eventos de transporte uno por uno.
La unión de ATP por sí sola activa el interruptor molecular
La controversia clave concierne a los iones magnesio (Mg2+), que normalmente acompañan al ATP en las células y son necesarios para la hidrólisis eficiente del ATP. Algunos modelos sugerían que el Mg2+ también podría ser necesario para que el ATP se una o para que el transportador se cierre. Para separar estos roles, los investigadores eliminaron el Mg2+ usando un agente quelante pero suministraron ATP. En estas condiciones, tanto el transportador normal como el lento pudieron llevar a cabo exactamente un paso de transporte de péptido por molécula, pero luego se detuvieron. Ese comportamiento indica que el ATP puede aun así unirse y forzar que el transportador cambie de una conformación orientada hacia el interior a otra orientada hacia el exterior y mueva un péptido, incluso sin Mg2+. Sin embargo, sin Mg2+ el transportador no puede escindir ATP de manera eficiente y, por tanto, no puede reiniciarse para otra ronda.
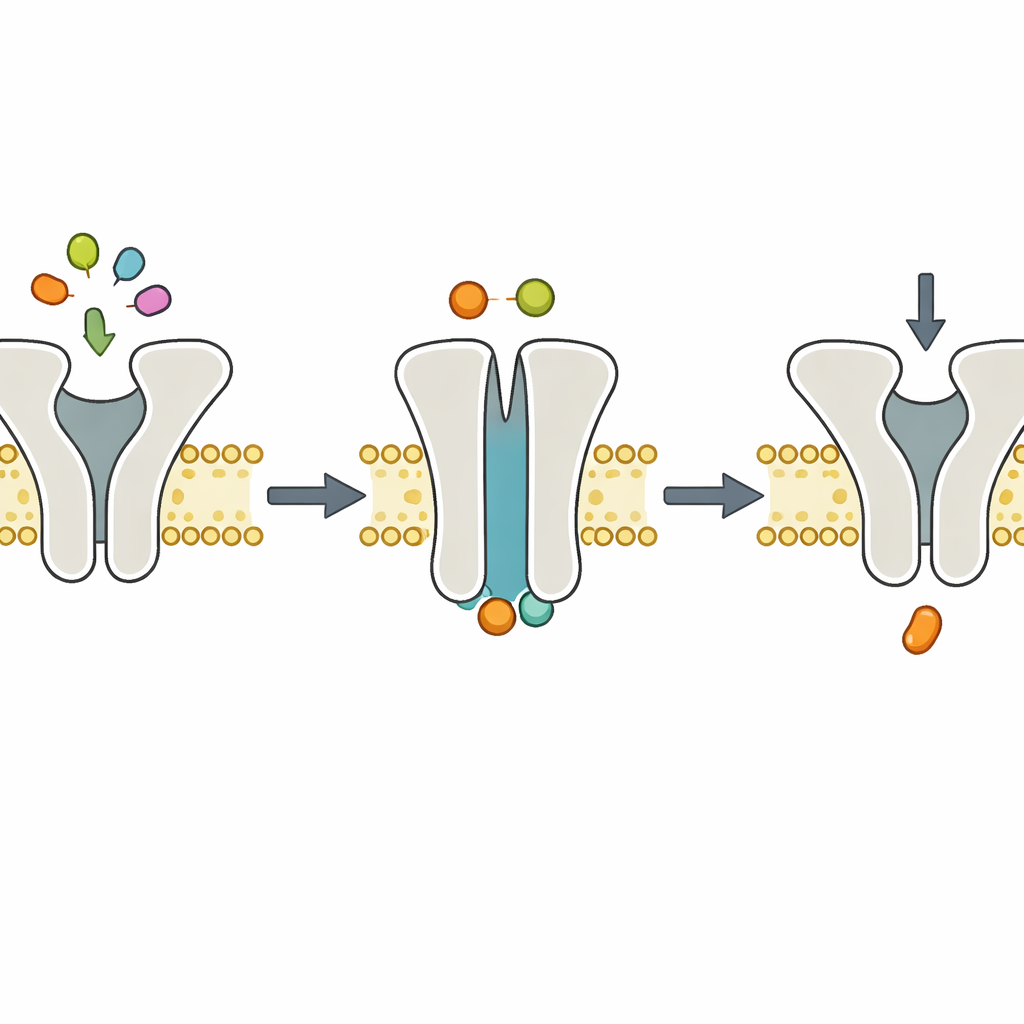
Instantáneas estructurales respaldan la dinámica
Para ver cómo se ve la máquina durante este paso sin Mg2+, el equipo recurrió a la criomicroscopía electrónica, que imagen moléculas vitrificadas con detalle cercano al atómico. Reconstituyeron TmrAB en nanodiscos lipídicos, añadieron ATP sin Mg2+ y congelaron los complejos. Las estructuras resultantes mostraron a TmrAB en una conformación orientada hacia el exterior, “ocluida”, con ATP encajado en ambos de sus sitios de unión internos, pero sin Mg2+ visible. Estas instantáneas eran esencialmente indistinguibles de estructuras anteriores obtenidas con ATP y Mg2+ presentes. Junto con ensayos bioquímicos que muestran que la hidrólisis de ATP se detiene por completo sin Mg2+, las imágenes apoyan una división simple del trabajo: la unión de ATP impulsa el cambio conformacional que mueve el péptido, mientras que la hidrólisis de ATP dependiente de Mg2+ realiza el paso de recuperación.
Una imagen más clara de cómo funcionan las bombas celulares
Al observar transportadores individuales y resolver sus estructuras, este trabajo resuelve una pregunta de larga data sobre los transportadores ABC: la carrera de potencia mecánica que mueve un péptido es desencadenada por la propia unión de ATP, no por la posterior descomposición química del ATP. El Mg2+ entra en la escena principalmente para permitir que el ATP se escinda, lo que a su vez reinicia el transportador para que pueda volver a funcionar. Más allá de aclarar una pieza fundamental de la biología celular, este enfoque de una sola molécula ofrece un modelo para diseccionar otras máquinas de membrana que sustentan la inmunidad, la resistencia a fármacos y muchas enfermedades—una molécula y un paso de transporte a la vez.
Cita: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Palabras clave: Transportadores ABC, Unión de ATP, FRET de una sola molécula, transporte de membrana, TAP y TmrAB