Clear Sky Science · es
Nanopartículas de azul de Prusia dirigidas a múltiples PANoptosomas mediadores de PANoptosis para la terapia de la lesión por isquemia-reperfusión miocárdica
Por qué importa proteger el corazón en reparación
Cuando una persona sufre un infarto, los médicos se apresuran a reabrir la arteria bloqueada y restaurar el flujo sanguíneo. Este paso que salva vidas, sin embargo, tiene un coste oculto: el regreso repentino de oxígeno puede dañar el corazón por sí mismo, provocando la muerte celular y preparando el terreno para la insuficiencia cardíaca. Este estudio explora una nanomedicina ingeniosa que pretende proteger el corazón durante esa ventana vulnerable bloqueando a la vez varias vías entrelazadas de muerte celular, lo que podría conducir a recuperaciones más suaves tras los infartos.
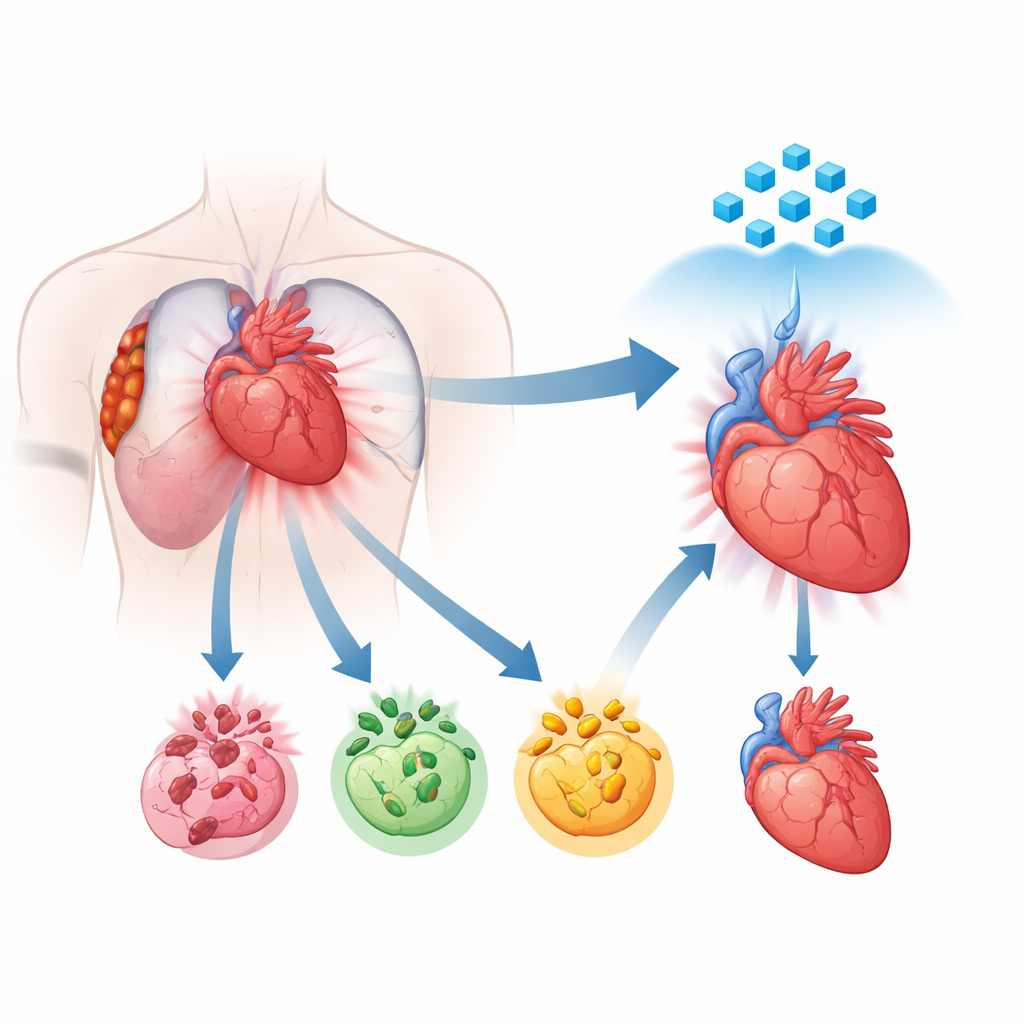
Una nueva visión de cómo mueren las células cardíacas
Durante años, los científicos han sabido que las células cardíacas dañadas pueden morir por distintas rutas programadas, incluidas la apoptosis, la necroptosis y la piroptosis. Cada una sigue su propio guion molecular, pero crece la evidencia de que estas rutas no operan de forma aislada. En cambio, se comunican entre sí y pueden unirse en un proceso combinado y descontrolado llamado PANoptosis. En este estado, varios programas de muerte se activan a la vez, lo que hace que las terapias que bloquean solo una vía resulten frustrantemente débiles. Los autores emplearon secuenciación de ARN de núcleo único en tejido cardíaco humano de pacientes con infartos recientes para mapear dónde y con qué intensidad se activan estos programas de muerte. Encontraron que en las regiones más dañadas, las células musculares cardíacas mostraban un cambio potente hacia este modo de muerte combinado, señalando a la PANoptosis como un impulsor central de la lesión.
Diseñando una multiherramienta diminuta para el corazón lesionado
Para abordar un proceso tan complejo, el equipo se centró en el azul de Prusia, un compuesto médico aprobado desde hace tiempo, conocido sobre todo como antídoto para ciertos envenenamientos por metales. A escala nanométrica, las partículas de azul de Prusia actúan como pequeños robots catalíticos que pueden eliminar moléculas nocivas e influir en el comportamiento celular. Mediante simulaciones por ordenador, los investigadores mostraron que estas nanopartículas podrían unirse directamente a tres nodos proteicos clave—RIPK1, ZBP1 y AIM2—que ayudan a ensamblar la maquinaria molecular de la PANoptosis. Al unirse a estos nodos de diferentes maneras, se predijo que las partículas interferirían con la construcción de los complejos inductores de muerte que coordinan las tres vías de muerte celular.
Guiando las nanopartículas directamente al tejido cardíaco dañado
Las nanopartículas solo funcionan si llegan al lugar correcto, así que el equipo recubrió las partículas de azul de Prusia con membranas naturales extraídas de plaquetas, las células sanguíneas que se dirigen a los vasos lesionados. Este recubrimiento creó PB@PM, un transportador biomimético que circula como una plaqueta pero entrega una carga terapéutica. En ratones sometidos a un infarto controlado y reapertura de la arteria, las imágenes mostraron que PB@PM se acumuló con mucha más intensidad en la región cardíaca lesionada que las partículas sin recubrimiento, evitando en gran medida los órganos sanos. Es importante destacar que las partículas recubiertas fueron bien toleradas: análisis de sangre y estudios de tejidos no revelaron toxicidad evidente, lo que respalda su potencial para un desarrollo posterior.
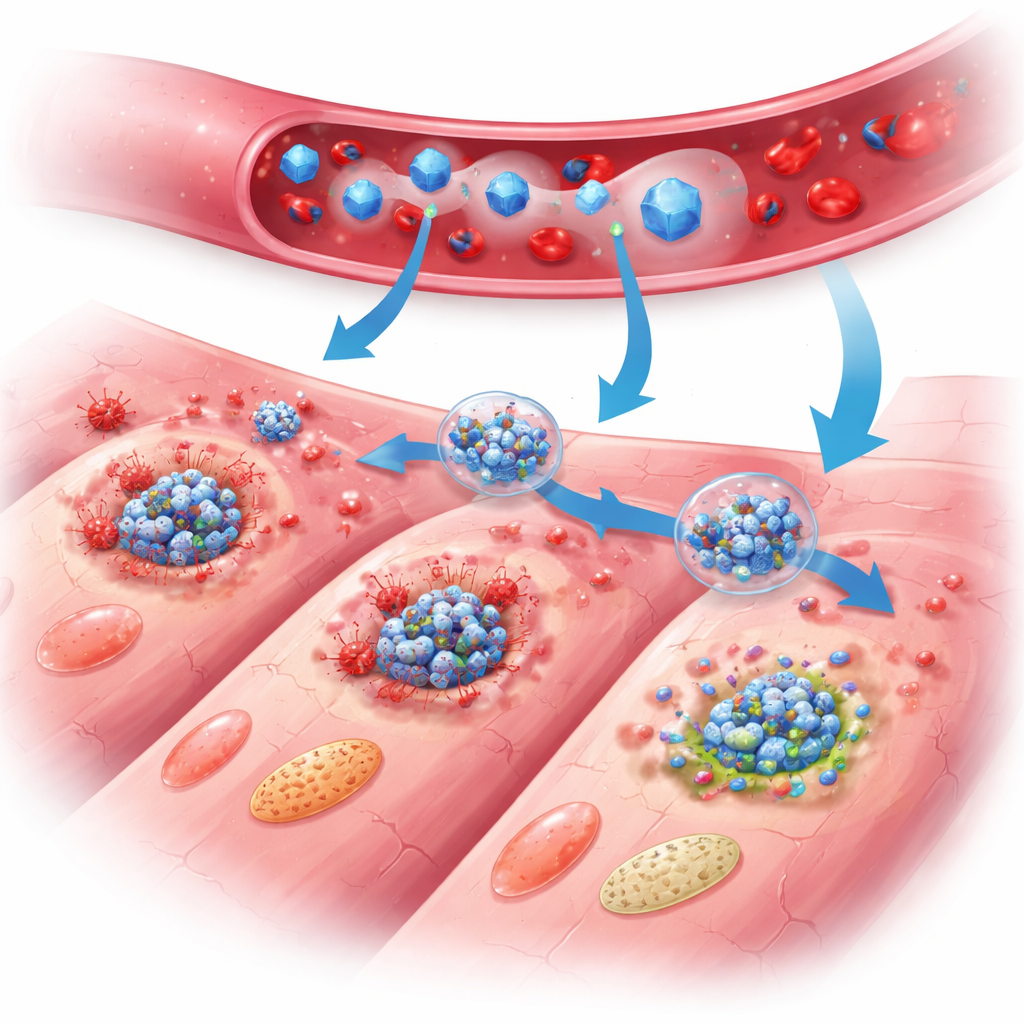
Cómo el nano-escudo protege el corazón
En los ratones tratados, los beneficios de PB@PM se hicieron evidentes durante días y semanas. La función de bombeo del corazón mejoró, el tamaño de la cicatriz se redujo y el engrosamiento de la pared cardíaca fue menor en comparación con los animales no tratados. Estudios tisulares detallados revelaron menos células cardíacas moribundas, células inflamatorias más calmadas y tejido de reparación mejor estructurado con un crecimiento vascular más sano y menos hipertrofia anómala de las células supervivientes. A nivel molecular, perfiles amplios de expresión génica y medidas proteicas mostraron que PB@PM silenciaba a la vez las tres principales vías de muerte programada, interrumpía el ensamblaje de los complejos multiproteicos de PANoptosis y reducía los niveles de moléculas de señalización que alimentan la inflamación. Las partículas también eliminaron especies reactivas de oxígeno dañinas, estabilizaron las mitocondrias—las centrales energéticas de la célula—y restauraron un metabolismo energético más normal, suprimiendo desencadenantes clave que de otro modo empujarían a las células hacia la autodestrucción.
Qué podría significar esto para el cuidado futuro del infarto
En pocas palabras, este trabajo muestra que una nanopartícula inteligentemente diseñada puede actuar como un escudo multifrontal para el corazón, amortiguando un enredo de señales mortales destructivas en lugar de perseguir una vía tras otra. Al dirigirse al tejido cardíaco lesionado, unirse a proteínas de control centrales y aliviar el estrés oxidativo e inflamatorio, PB@PM redujo drásticamente la reacción en cadena de pérdida celular y cicatrización que a menudo sigue a la reapertura de una arteria bloqueada. Aunque hacen falta muchas pruebas antes de que esta estrategia pueda llegar a los pacientes, el estudio ofrece una prueba de concepto de que atacar la PANoptosis en su conjunto—y hacerlo con partículas inteligentes e inspiradas en la biología—podría abrir un nuevo capítulo en la protección del corazón tras un infarto.
Cita: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Palabras clave: isquemia-reperfusión miocárdica, terapia con nanopartículas, muerte celular programada, inflamación cardíaca, protección mitocondrial