Clear Sky Science · es
RPA estimula directamente la procesividad de la helicasa Mer3 para asegurar la formación normal de cruzamientos en la meiosis
Cómo las células barajan el ADN para producir óvulos y espermatozoides sanos
Cada vez que una planta, un animal o un humano produce óvulos o espermatozoides, sus células deben reordenar los cromosomas para que cada descendiente reciba una mezcla nueva del ADN parental. Este remezclado genético depende de intercambios de ADN cuidadosamente situados, o cruzamientos, entre pares de cromosomas. El estudio que se presenta desvela cómo dos proteínas clave, Mer3 y RPA, trabajan juntas como una máquina microscópica para garantizar que estos cruzamientos se formen de manera eficiente y segura; un proceso con implicaciones para la fertilidad, la evolución y, posiblemente, también el cáncer.
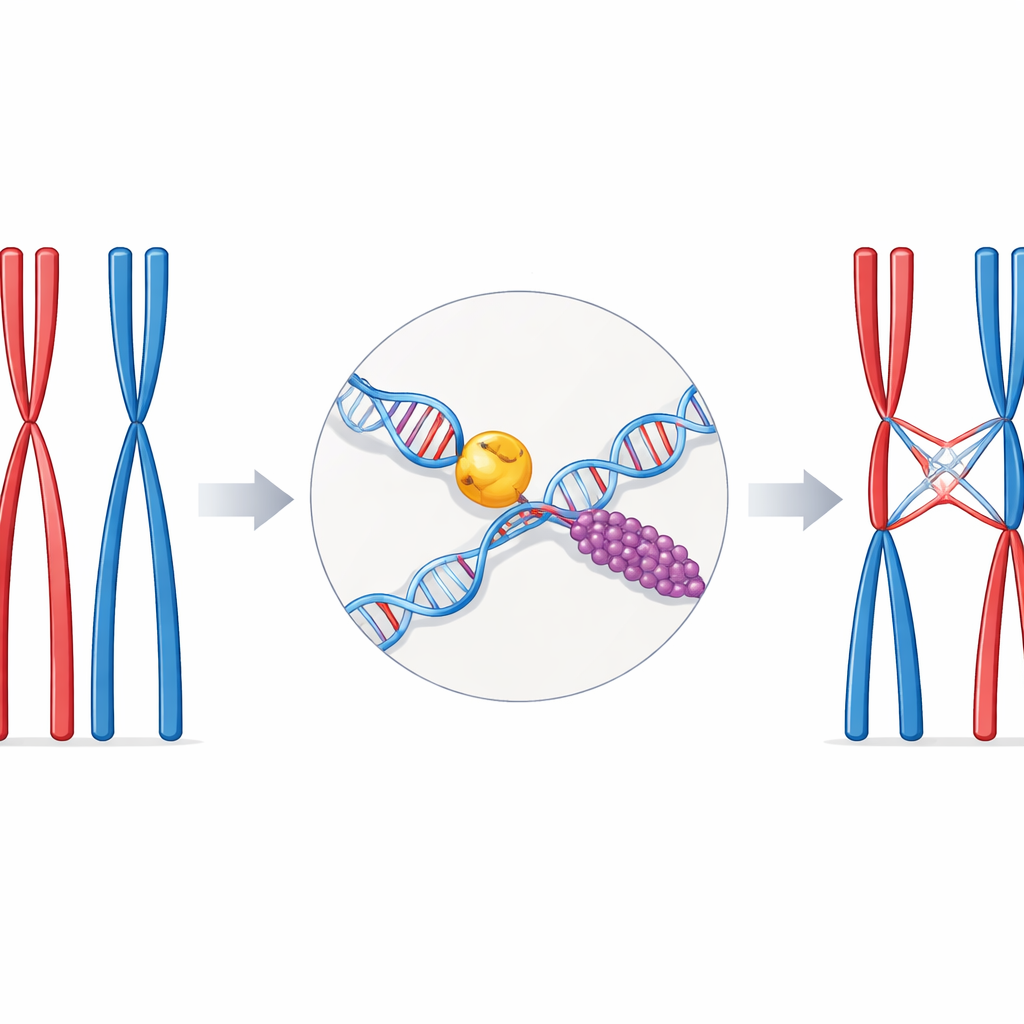
Un delicado acto de equilibrio en la reproducción sexual
Durante la división celular especial llamada meiosis, los cromosomas aparecen en pares coincidentes, uno de cada progenitor. Para que estos pares se separen correctamente, deben quedar físicamente unidos en algunos puntos bien elegidos a lo largo de su extensión. Estos enlaces son los cruzamientos: secciones donde las hebras de ADN de un cromosoma se intercambian con las de su pareja. Tener muy pocos cruzamientos aumenta el riesgo de mala segregación cromosómica e infertilidad; tener demasiados o mal situados puede dañar el genoma. Por eso las células recurren a vías de reparación especializadas y proteínas auxiliares para convertir una rotura peligrosa de ADN en un cruzamiento controlado correctamente.
Conozca a Mer3 y RPA, un equipo que desenrolla ADN
Los investigadores se centraron en Mer3, un motor molecular que desenrolla el ADN y favorece la formación de cruzamientos. Su equivalente humano, HFM1, es conocido por ser importante para la fertilidad. Descubrieron que Mer3 se une directamente a RPA, un complejo proteico que normalmente recubre el ADN monocatenario expuesto para protegerlo y reclutar otros factores de reparación. Mediante ensayos bioquímicos, modelado estructural y ensayos de interacción, el equipo localizó un sitio de acoplamiento específico donde una cola corta de Mer3 encaja en una hendidura de una subunidad de RPA. Esta interfaz está conservada desde levaduras hasta mamíferos, lo que sugiere que es una solución antigua que la evolución ha reutilizado para controlar la reparación del ADN durante la meiosis.
Observando un motor de ADN individual en acción
Para ver qué hace realmente esta asociación, los científicos usaron pinzas magnéticas a nivel de molécula única —un instrumento que mantiene un horquilla de ADN como un pequeño resorte y mide cómo una sola molécula de Mer3 la desenrolla con el tiempo. Encontraron que Mer3 se desplaza por el ADN a una velocidad constante incluso por sí solo. Pero en condiciones que imitan la tensión física relativamente baja dentro de las células, Mer3 tiende a soltarse del ADN tras desenrollar solo un tramo corto. Cuando hay una pequeña cantidad de RPA presente, Mer3 se vuelve de repente mucho más persistente: puede desenrollar tramos mucho más largos de ADN sin caerse, especialmente cuando el ADN tiende a plegarse sobre sí mismo. Una versión mutante de Mer3 diseñada para interrumpir la cola que se une a RPA no consigue esa mayor capacidad de permanencia, lo que revela que el contacto directo con RPA es lo que aumenta la procesividad de Mer3.
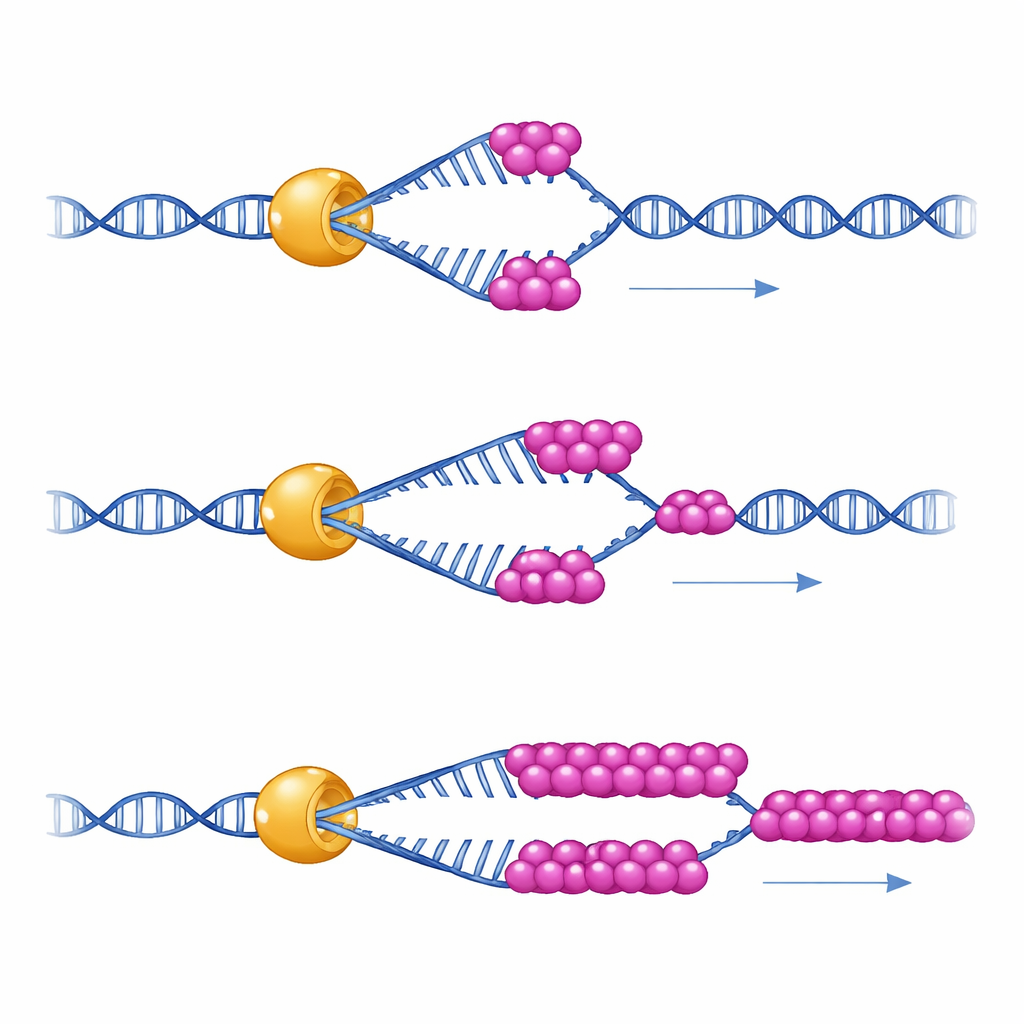
Consecuencias para los cruzamientos en células vivas
El equipo preguntó entonces qué ocurre en células de levadura reales cuando Mer3 no puede agarrar bien a RPA. Sustituyeron el gen MER3 normal por la versión mutante que no se une a RPA y monitorizaron la meiosis. Estas células aún podían dividirse y formar esporas, pero su fertilidad disminuyó y el número global de cruzamientos a lo largo de ciertas regiones cromosómicas se redujo. Un análisis detallado del ADN mostró más eventos de reparación que terminaban como no‑cruzamientos y una acumulación de intermedios de recombinación sin resolver. El mapeo a escala del genoma de la localización de Mer3 reveló que la proteína mutante estaba reclutada de manera menos estable en los sitios donde se producen roturas de ADN programadas, aunque su asociación temprana con los ejes cromosómicos parecía normal. En otras palabras, sin una unión fuerte a RPA, Mer3 no permanece el tiempo suficiente en los sitios de rotura para conducirlos con fiabilidad hacia resultados de cruzamiento.
Qué implica esto para la fertilidad y la estabilidad del genoma
En conjunto, el estudio muestra que RPA hace algo más que simplemente recubrir el ADN suelto; ajusta directamente el comportamiento de una helicasa meiótica clave. Al acoplarse a RPA, Mer3 se convierte en un desenrollador de ADN más decidido, capaz de extender y estabilizar las estructuras de ADN conjuntas que maduran hasta convertirse en cruzamientos. Cuando esta interacción se debilita, las células se orientan hacia resultados de reparación más seguros pero menos útiles y dejan más intermedios sin resolver, socavando de forma sutil la segregación cromosómica. Dado que los mismos jugadores moleculares existen en humanos —y que las mutaciones en HFM1 se han relacionado con la infertilidad—, este trabajo proporciona un marco mecanístico de cómo pequeños cambios en una interfaz proteica pueden tener efectos en cascada sobre la salud reproductiva y la diversidad genética de las futuras generaciones.
Cita: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Palabras clave: meiosis, recombinación genética, helicasa de ADN, fertilidad, intercambio cromosómico