Clear Sky Science · es
Desregulación de la respuesta al daño del ADN por oligonucleótidos antisentido fosforotioatos
Cuando terapias génicas útiles engañan al equipo de reparación de la célula
Los oligonucleótidos antisentido, o ASO, son una clase emergente de fármacos de precisión diseñados para activar o silenciar genes concretos. Ya se utilizan para tratar algunos trastornos genéticos raros y se están probando en muchas más enfermedades. Este estudio revela un inconveniente inesperado de una modificación química habitual usada para estabilizar estos fármacos: en ciertas condiciones, puede engañar a la célula haciéndole creer que su ADN está dañado, bloqueando la maquinaria de reparación y poniendo en riesgo la integridad del genoma a largo plazo.
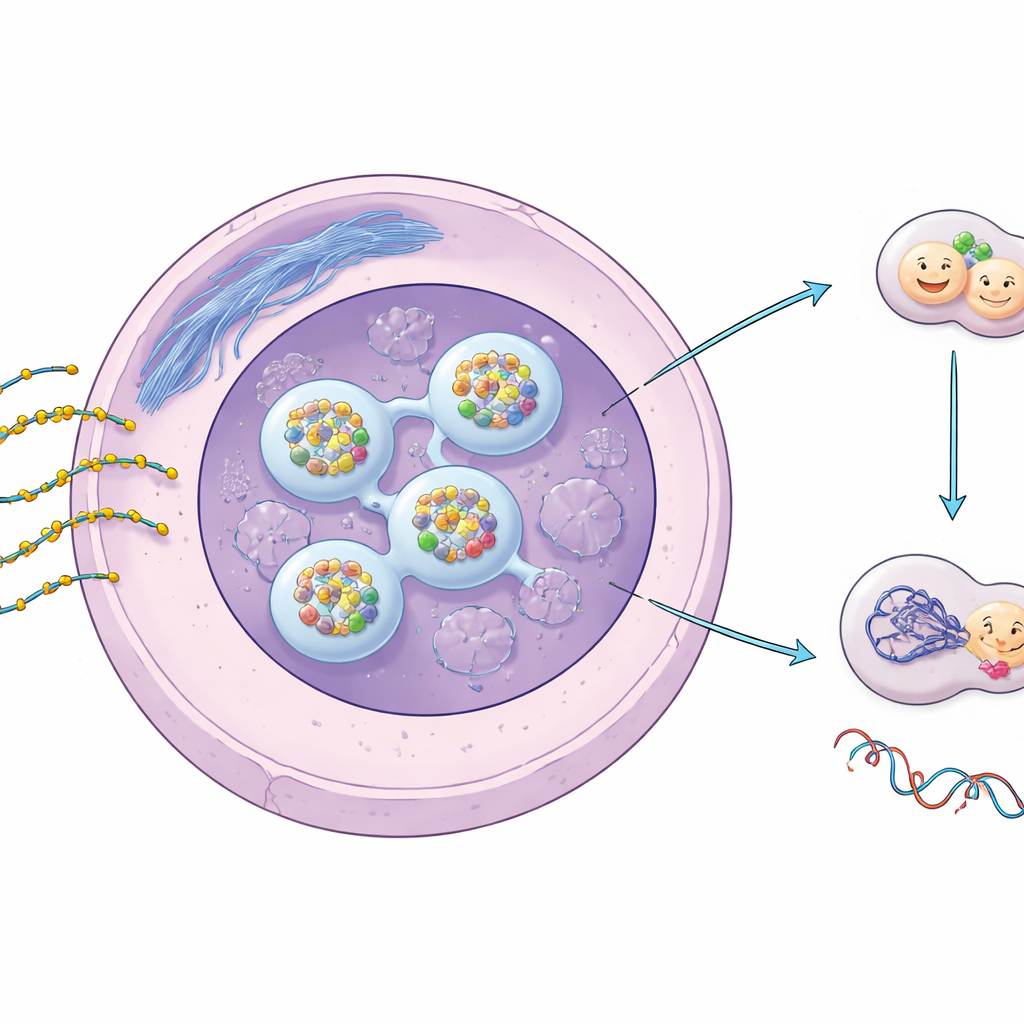
Interruptores génicos diseñados y su mejora química
Los ASO son cadenas cortas y sencillas de material genético creadas para reconocer y unirse a mensajes de ARN específicos dentro de nuestras células, silenciándolos o modificándolos. Para sobrevivir en el organismo y entrar eficientemente en las células, la mayoría de los ASO terapéuticos llevan una modificación de fosforotioato (PS), en la que un átomo de azufre sustituye a un átomo de oxígeno en la columna vertebral de la cadena. Este pequeño cambio aumenta drásticamente su estabilidad y su tendencia a interactuar con proteínas. Trabajos previos mostraron que los PS‑ASO se acumulan en puntos distintos en el núcleo celular y pueden estresar ciertas estructuras nucleares, pero quedaba por aclarar qué implicaciones tiene esto para la reparación del ADN y la seguridad a largo plazo.
Gotas artificiales que imitan sitios reales de reparación del ADN
Los autores siguieron PS‑ASO marcados con fluorescencia en células humanas y encontraron que, a dosis experimentales comúnmente usadas, se acumulan rápidamente en el núcleo y originan nuevas estructuras esféricas denominadas cuerpos PS. Estos cuerpos se forman de manera dependiente de la concentración y se comportan como gotas líquidas que se fusionan, se disuelven y dependen de fuerzas moleculares débiles—rasgos característicos de la separación de fase líquido–líquido. Crucialmente, no se localizan donde ocurren roturas reales del ADN ni contienen los marcadores habituales de ADN roto. En lugar de eso, el estudio muestra que enzimas clave de reparación del ADN—incluyendo DNA‑PKcs, ATM, ATR y PARP1—se unen directamente a los PS‑ASO y se enriquecen considerablemente dentro de estas gotas artificiales, pese a que el ADN subyacente está intacto.
Falsas alarmas que activan las señales de daño celular
Una vez formadas, las gotas iniciadas por ASO hacen más que atrapar proteínas pasivamente: activan las enzimas de reparación. En la primera hora tras la entrada de ASO, las enzimas en estas gotas se activan y comienzan a modificar la cromatina cercana, marcando histonas con señales químicas que normalmente aparecen tras daño genuino del ADN. Esto desencadena la respuesta completa al daño del ADN—reclutando factores de reparación adicionales, activando la señalización de puntos de control y reduciendo la actividad de los motores del ciclo celular llamados CDK. Como resultado, las células ralentizan o detienen su progresión por fases clave del ciclo celular, particularmente en el punto donde habitualmente comprueban que su ADN está intacto antes de dividirse. En cerebros de ratón expuestos a una administración de ASO clínicamente relevante, los investigadores también observaron una mayor señalización de daño en regiones con mayor captación de ASO, lo que indica que estos efectos no se limitan a cultivos celulares.
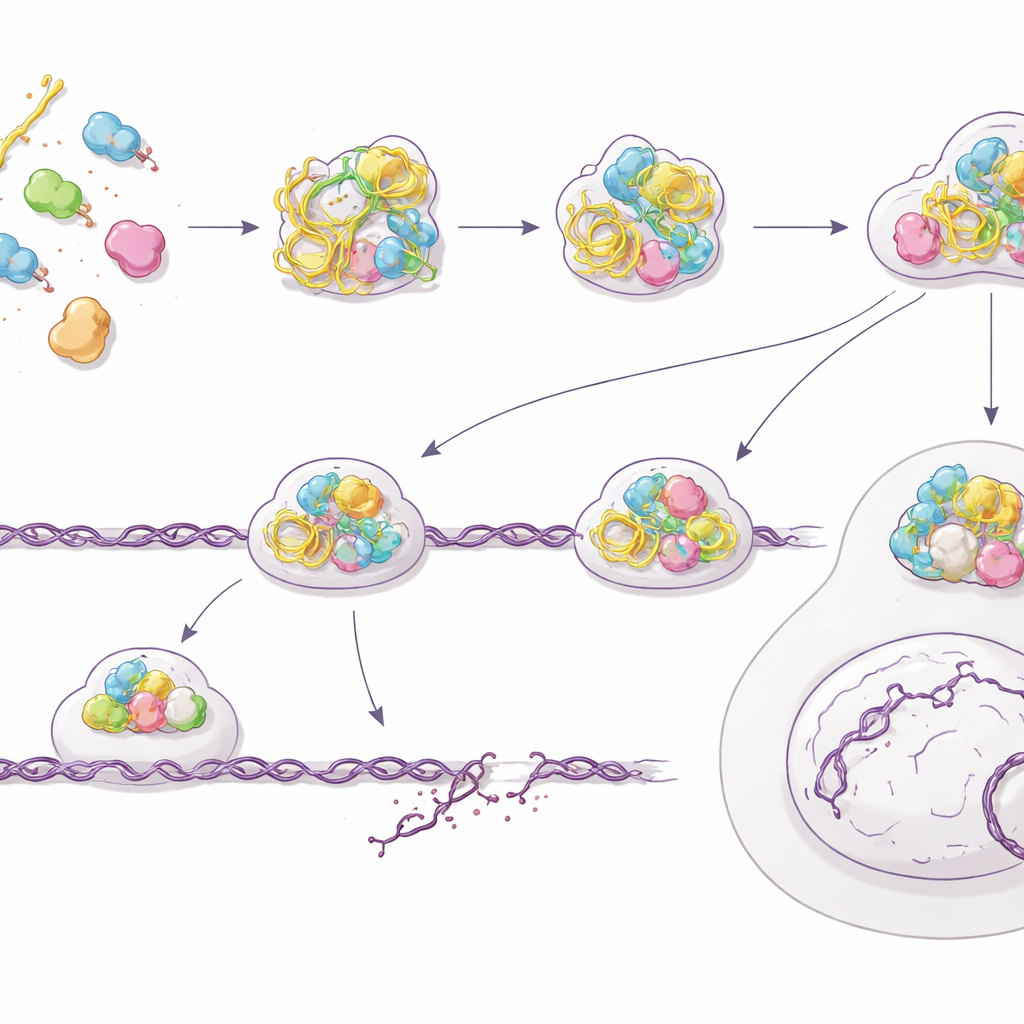
Reparación equivocada y una creciente carga de roturas de ADN
Paradójicamente, mientras suena la alarma celular, la capacidad real para reparar roturas peligrosas del ADN empeora. El equipo demostró que las células pretratadas con PS‑ASO tienen dificultades para eliminar daños tras irradiación e incluso acumulan más roturas espontáneas, medidas por ensayos de cometa y focos de reparación persistentes. Un examen más detallado de una de las vías de reparación más precisas de la célula—la recombinación homóloga—reveló el problema: actores clave como BRCA2 y RAD51 no logran ensamblarse correctamente en los extremos rotos del ADN, mientras que marcadores tempranos de procesado en esos extremos aún aparecen. Usando un sistema genético reportero, los autores cuantificaron una caída de alrededor del 60% en la eficiencia de la recombinación homóloga tras la exposición a PS‑ASO. Las células se vuelven menos viables en general y claramente más sensibles a la radiación, coherente con un sistema de reparación que está siendo activado pero no desplegado correctamente.
Qué significa esto para el futuro de los fármacos dirigidos a genes
En conjunto, el estudio sugiere que los ASO modificados con PS pueden nucleizar gotas líquidas artificiales en el núcleo que concentran y activan enzimas de reparación del ADN incluso cuando no hay daño que arreglar. Esta falsa alarma crónica perturba las decisiones normales de reparación, en particular la recombinación homóloga precisa, conduciendo a lesiones persistentes en el ADN, activación de puntos de control y muerte celular. Aunque los efectos más intensos se observan a niveles nucleares altos de ASO, típicos de experimentos de transfección, una activación sutil de la señalización de daño es detectable incluso a dosis más bajas, similares a las de fármaco. Para pacientes y desarrolladores de medicamentos, el mensaje es claro: las mismas características químicas que hacen a los ASO fármacos eficaces pueden, en algunos contextos, interferir con la salvaguarda más fundamental de la célula—su capacidad para mantener un genoma estable—subrayando la necesidad de diseñar respaldos más seguros y monitorizar las vías de reparación del ADN durante la terapia.
Cita: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Palabras clave: oligonucleótidos antisentido, respuesta al daño del ADN, separación de fase líquida, recombinación homóloga, estabilidad genómica