Clear Sky Science · es
Análogos quirales del peptidoglicano apuntan a la biosíntesis de la pared bacteriana para la intervención frente a patógenos
Una nueva forma de cazar gérmenes dañinos
Las infecciones resistentes a los antibióticos están aumentando en todo el mundo, pero los médicos aún carecen de herramientas que puedan detectar y atacar con precisión las bacterias peligrosas sin dañar nuestras propias células. Este estudio presenta un ingenioso "cebo" molecular que imita un componente clave de la pared celular bacteriana. Estas moléculas diseñadas pueden tanto iluminar las infecciones para su imagen como transportar antibióticos directamente a los microbios, ofreciendo una estrategia novedosa para combatir patógenos difíciles de tratar.
Imitando la armadura bacteriana
Las bacterias están envueltas en una malla resistente llamada pared celular, construida a partir de azúcares y aminoácidos en forma de imagen especular que nuestras propias células apenas usan. Los investigadores aprovecharon esta diferencia creando largas cadenas a base de azúcares decoradas con una forma especular específica de alanina, un aminoácido común. Estas cadenas, denominadas imitadores quirales del peptidoglicano, están diseñadas para asemejarse estrechamente a los ingredientes naturales que las bacterias usan para construir sus paredes, pero están ausentes en los tejidos de mamíferos. Al ajustar la cantidad de alanina en configuración D que se añadió, el equipo produjo versiones que favorecían claramente a las bacterias frente a las células humanas.
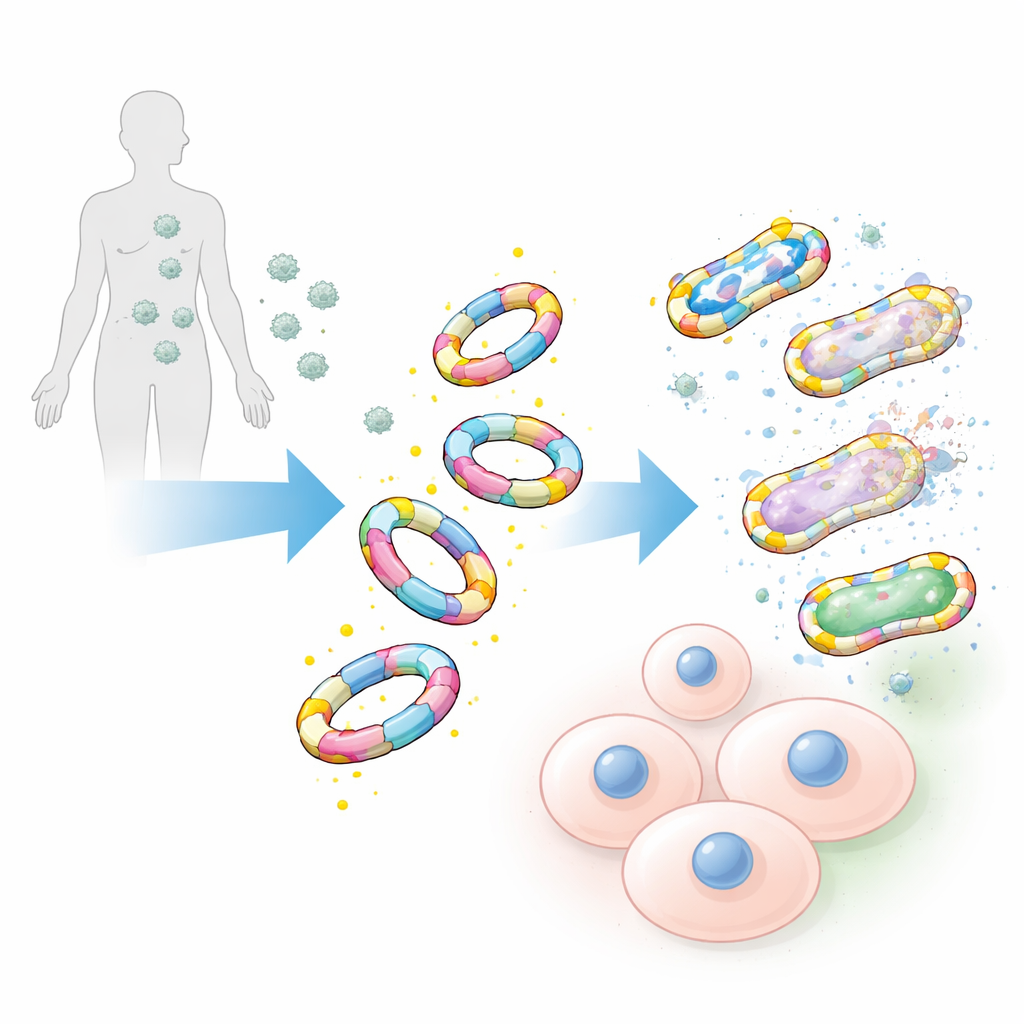
Adherirse a las bacterias, no a nuestras células
Al probarse frente a una amplia gama de patógenos, incluidas cepas hospitalarias notorias como Staphylococcus aureus resistente a meticilina y otras bacterias ESKAPE, los imitadores decorados con D-alanina se unieron a las superficies bacterianas con una eficiencia llamativa. Sus equivalentes imagen especular construidos con la forma L de la alanina, así como las cadenas azucaradas sin modificar, mostraron una unión débil o despreciable. El equipo también comparó estos grandes imitadores con sondas químicas tradicionales de pequeño tamaño basadas en moléculas individuales de D-alanina. Incluso cuando las sondas pequeñas se hicieron extremadamente brillantes, todavía marcaron a muchas menos bacterias y dieron señales más débiles, subrayando la fuerza del diseño más grande y más realista.
Secuestrando la cadena de montaje de la pared celular
Para entender cómo la reconocibilidad se hace tan fuerte, los científicos examinaron cómo interactúan los imitadores con la maquinaria que construye la pared bacteriana. Descubrieron que las cadenas basadas en D-alanina no solo se adhieren al exterior; son incorporadas como si fuesen auténticos bloques de construcción y alimentadas en los mismos pasos enzimáticos que normalmente unen los componentes de la pared. El análisis químico detectó nuevos intermediarios que surgen solo cuando estos imitadores están presentes, y las simulaciones por ordenador mostraron que enzimas clave de construcción de la pared agarran a los imitadores incluso con más firmeza que a los sustratos naturales. Tras varias rondas de crecimiento bacteriano, los imitadores se acumularon en la pared, distorsionando gradualmente su estructura y haciéndola permeable.
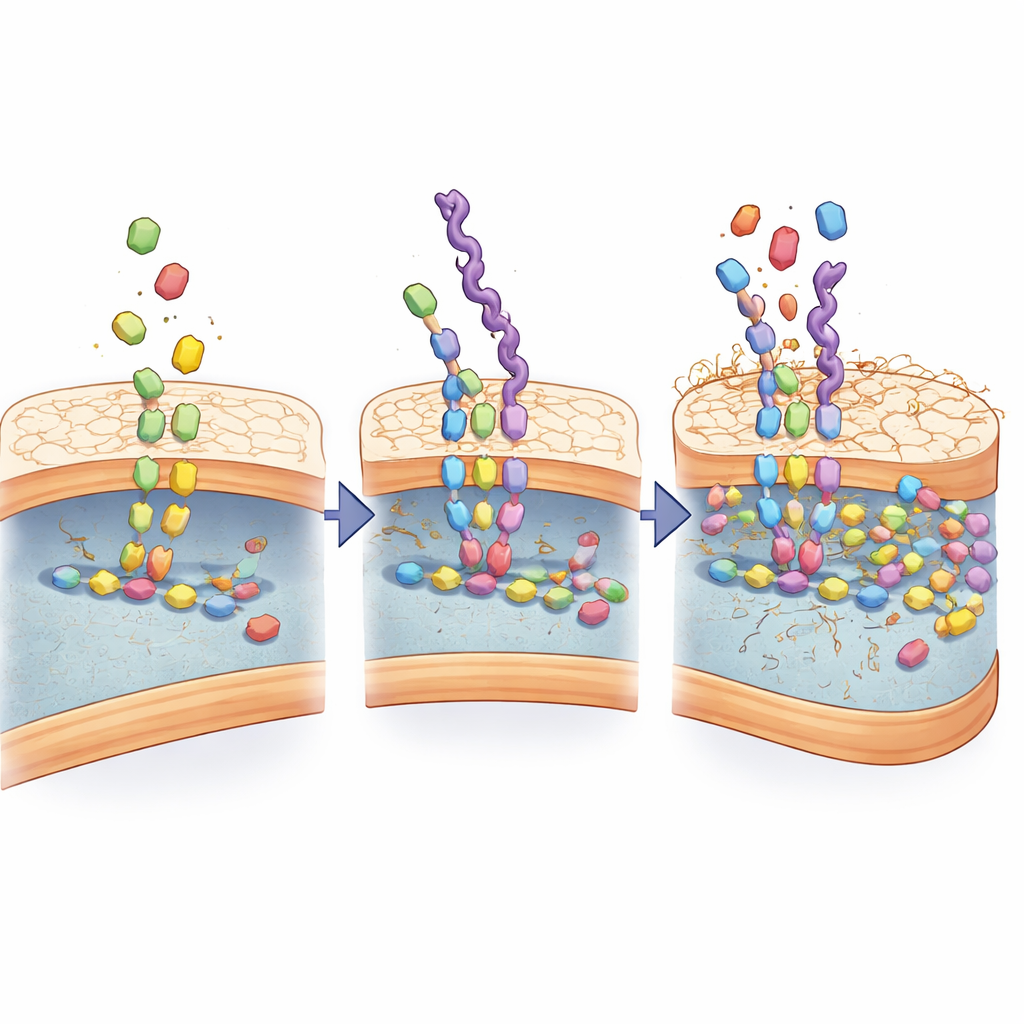
Convertir los imitadores en portadores inteligentes de fármacos
Puesto que estas cadenas se agrupan de forma natural en partículas diminutas en agua y contienen numerosos puntos de anclaje químicos, el equipo las utilizó como andamiaje para colorantes de imagen y antibióticos. Las versiones fluorescentes delinearon claramente las bacterias en cultivos celulares, mientras interactuaban muy poco con las células de mamífero cultivadas junto a ellas. Los investigadores cargaron entonces el antibiótico tetraciclina en las partículas basadas en los imitadores. En ensayos de laboratorio, este encapsulado hizo que la tetraciclina fuera varias veces más eficaz, matando incluso a cepas resistentes con dosis mucho más bajas que el fármaco libre. La microscopía reveló que los imitadores cargados con antibiótico se agolpaban sobre las bacterias, penetraban sus envolturas y provocaban una muerte celular extensa en comparación con formulaciones no dirigidas.
Luchando contra infecciones dentro del cuerpo
Las pruebas más exigentes tuvieron lugar en modelos murinos de heridas cutáneas localizadas e infecciones abdominales potencialmente mortales. En heridas infectadas, los imitadores fluorescentes se dirigieron a las bacterias profundas en el tejido y, al portar tetraciclina, eliminaron casi por completo los microbios. Esto condujo a una curación más rápida, piel nueva más gruesa, una deposición de colágeno más ordenada y un mayor desarrollo de pequeños vasos sanguíneos. En modelos de infección sistémica, los imitadores se acumularon específicamente en órganos infectados como el bazo y los pulmones, donde redujeron drásticamente los recuentos bacterianos cuando estaban cargados con antibiótico. Es importante destacar que dosis elevadas de los imitadores por sí solas mostraron buena seguridad, sin daños evidentes en órganos principales o en la química sanguínea.
Qué podría significar esto para tratamientos futuros
Al construir un análogo químico muy parecido a los propios ingredientes de la pared bacteriana, este trabajo demuestra una nueva manera de "camuflarse" en el metabolismo del patógeno en lugar de limitarse a atacar desde fuera. Estos imitadores quirales actúan tanto como balizas de alta precisión para la imagen como vehículos inteligentes que dirigen antibióticos directamente hacia sus objetivos microbianos, incluidas cepas resistentes, al tiempo que preservan las células de mamíferos. Si se traducen en herramientas clínicas, estas plataformas biomiméticas podrían ayudar a los médicos a ver exactamente dónde se ocultan las infecciones y tratarlas de forma más eficaz con dosis de fármacos más bajas, ofreciendo un arma prometedora contra el creciente desafío de la resistencia antimicrobiana.
Cita: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Palabras clave: resistencia a los antibióticos, pared celular bacteriana, administración dirigida de fármacos, imagen molecular, nanomedicina