Clear Sky Science · es
Desfluorinación completa de los PFAS mediante reducción fotocatalítica en agua
Por qué por fin parece posible romper las "sustancias químicas para siempre"
Durante décadas, una clase de contaminantes conocida como PFAS —a menudo llamadas “sustancias químicas para siempre”— se ha acumulado en el agua potable, la fauna e incluso la sangre humana porque apenas se descomponen en la naturaleza. Este estudio describe un nuevo material impulsado por la luz que puede casi eliminar por completo los átomos de flúor de algunos de los PFAS más persistentes en agua, transformándolos en pequeñas moléculas inocuas sin necesidad de productos químicos agresivos ni de costes energéticos elevados. Eso lo convierte en un esquema prometedor para una limpieza más segura y práctica de abastecimientos de agua contaminada.
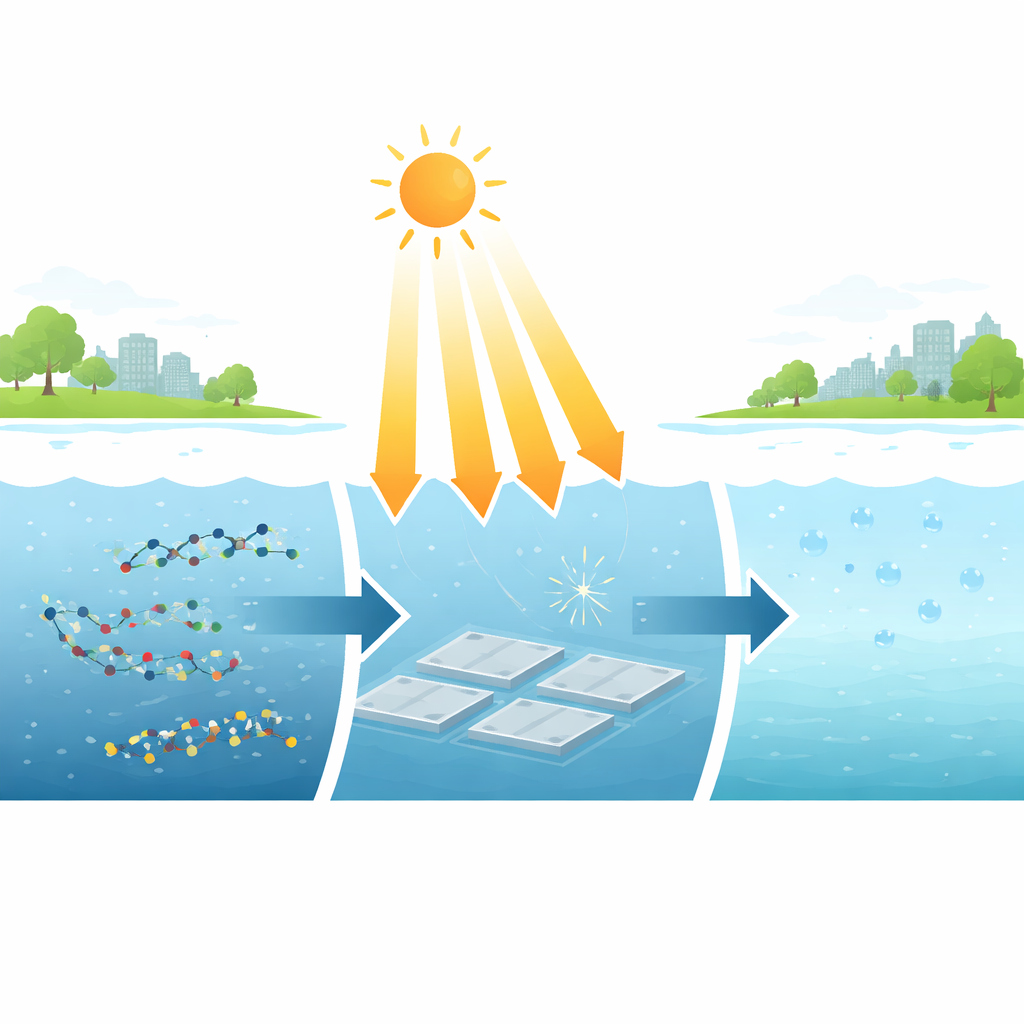
El problema de los contaminantes fluorados persistentes
Los PFAS (sustancias per- y polifluoroalquílicas) se usan en sartenes antiadherentes, espumas contra incendios y recubrimientos resistentes a manchas. Sus enlaces carbono–flúor están entre los más resistentes de la química, por eso los PFAS perduran en el medio ambiente y se bioacumulan en los seres vivos. Dos de los PFAS más difundidos, PFOA y PFOS, ahora se clasifican como riesgos cancerígenos para el ser humano, y varios países han establecido límites en el agua potable en el rango de partes por trillón. Desafortunadamente, la mayoría de los métodos existentes capaces de destruir realmente los PFAS —como ultrasonido intenso, tratamiento a alta temperatura o aditivos químicos fuertes— funcionan solo a concentraciones altas y requieren mucha energía, lo que dificulta su escalado para el tratamiento de agua en el mundo real.
Un nuevo catalizador impulsado por la luz diseñado para enlaces extremos
Los investigadores diseñaron un material orgánico especial llamado TAPP, que se autoensambla en pilas ordenadas de moléculas planas. Cuando se ilumina con luz visible, estas pilas forman un estado radicalario de larga vida —una versión de la molécula con un electrón no apareado— que permanece estable durante más de una semana en aire. Debido a que la carga eléctrica se distribuye por la molécula y sus grupos amino unidos, este radical puede absorber una segunda dosis de luz y empujar electrones a energías extremadamente altas. Esos electrones energizados son lo bastante fuertes para atacar los enlaces carbono–flúor ultrastables en los PFAS, algo que los catalizadores ordinarios basados en luz no pueden lograr.
Cómo el catalizador captura y desmantela los PFAS
Las partículas de TAPP están cargadas positivamente en agua, mientras que el PFOS y PFAS relacionados presentan cargas negativas en un extremo y colas fluoradas en el otro. Este contraste atrae a los contaminantes hacia la superficie del catalizador: los grupos cabeza cargados negativamente interactúan con sitios amino protonados, y la cola fluorada se dispone a lo largo de la superficie aromática plana mediante fuerzas de atracción suaves. Tras este paso de “preconcentración”, la luz visible excita repetidamente al TAPP. Su forma radicalaria envía electrones de alta energía directamente a las regiones antienlazantes de los enlaces carbono–flúor del PFAS. Ese electrón adicional desestabiliza la estructura helicoidal rígida de la cadena PFAS, estira la columna vertebral de carbono y facilita que enlaces C–F individuales se rompan.
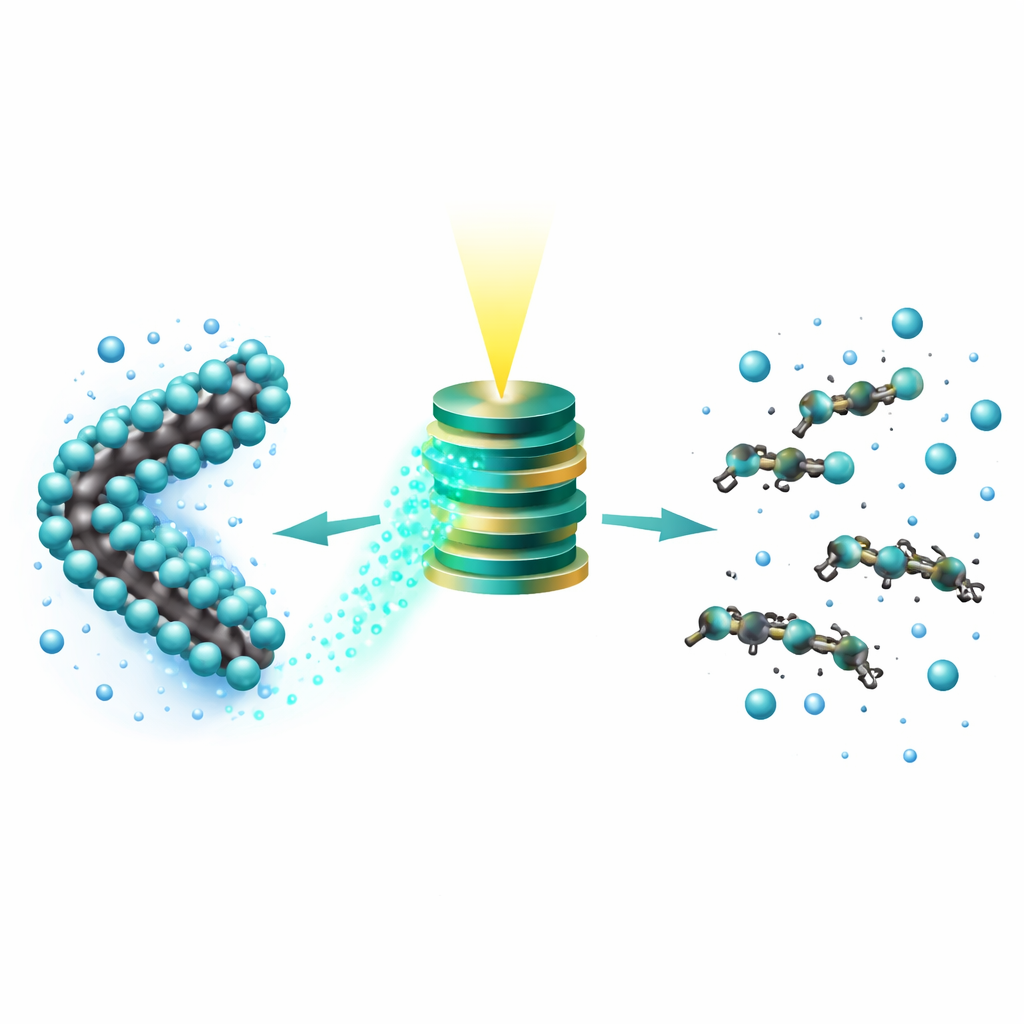
De cadenas letales a fragmentos inocuos
En experimentos de agua controlados con niveles de contaminante realistas (alrededor de 0,1 partes por millón), el TAPP eliminó el PFOS de la solución y, bajo luz, convirtió casi todo su flúor en iones fluoruro libres en aproximadamente dos días. El análisis químico detallado mostró que la señal original de PFOS desapareció y fue reemplazada por ácidos orgánicos simples como formiato, oxalato y lactato, sin PFOS residual en la superficie del catalizador. Al inicio de la reacción, el equipo detectó una serie de fragmentos fluorados más cortos, lo que apoya un mecanismo en el que los electrones primero arrancan el flúor de la cadena y luego el esqueleto de carbono debilitado se fragmenta en piezas más pequeñas que se oxidan adicionalmente hasta productos finales benignos.
Rendimiento en agua real y ahorro energético
Para probar la practicidad, los científicos construyeron un pequeño reactor al aire libre que imitaba una unidad de tratamiento en una planta de aguas residuales. Solo con luz solar natural, su sistema basado en TAPP desfluorinó completamente agua con PFOS en tres días. El catalizador funcionó bien incluso en presencia de materia orgánica natural e iones comunes, aunque algunas sales ralentizaron el proceso al competir por sitios superficiales. En comparación con otros tratamientos de PFAS impulsados por luz, este enfoque consumió alrededor de un 90–98 % menos energía por volumen de agua y evitó metales tóxicos o agentes oxidantes añadidos. El catalizador también se mantuvo activo al menos durante cinco ciclos repetidos con una pérdida mínima de eficiencia.
Qué significa esto para limpiar las "sustancias químicas para siempre"
Este trabajo demuestra que materiales orgánicos cuidadosamente diseñados pueden usar luz visible ordinaria para generar electrones lo bastante energéticos como para romper los enlaces carbono–flúor más resistentes en PFAS, todo ello operando en agua simple y sin químicos sacrificatorios. Al combinar una fuerte adsorción de contaminantes, un estado radical de larga vida y fotoexcitación en múltiples pasos, el catalizador TAPP transforma PFAS persistentes en fluoruro y pequeñas moléculas orgánicas inocuas. Aunque escalar la tecnología y abordar la amplia variedad de PFAS llevará tiempo, este estudio ofrece una vía realista hacia la destrucción con energía solar y bajo coste de las "sustancias químicas para siempre" en sistemas de agua potable y aguas residuales.
Cita: Chong, M., Zhou, Q., Xu, J. et al. Complete defluorination of PFASs via photocatalytic reduction in water. Nat Commun 17, 3081 (2026). https://doi.org/10.1038/s41467-026-69933-9
Palabras clave: Remediación de PFAS, fotocatálisis, tratamiento de agua, desfluorinación, química ambiental