Clear Sky Science · es
Las células Th17 requieren el sensor de reparación del ADN xeroderma pigmentosum complementación del Grupo C para controlar el daño oxidativo del ADN en un modelo murino
Guardianes de nuestros defensores inmunitarios
Las células T helper 17, o células Th17, son un tipo especial de glóbulo blanco que patrulla las barreras del cuerpo, como el intestino y la piel, para defendernos frente a bacterias y hongos. Pero también participan en enfermedades autoinmunes cuando sus respuestas se descontrolan. Este estudio plantea una pregunta aparentemente simple: ¿cómo protegen estas células tan activas su propio ADN del estrés químico que generan al combatir infecciones? La respuesta se centra en un sensor de daño del ADN llamado XPC, conocido sobre todo por proteger las células de la piel frente a la luz solar. Aquí, los investigadores muestran que XPC también es crucial para mantener las células Th17 saludables, enérgicas y eficaces.
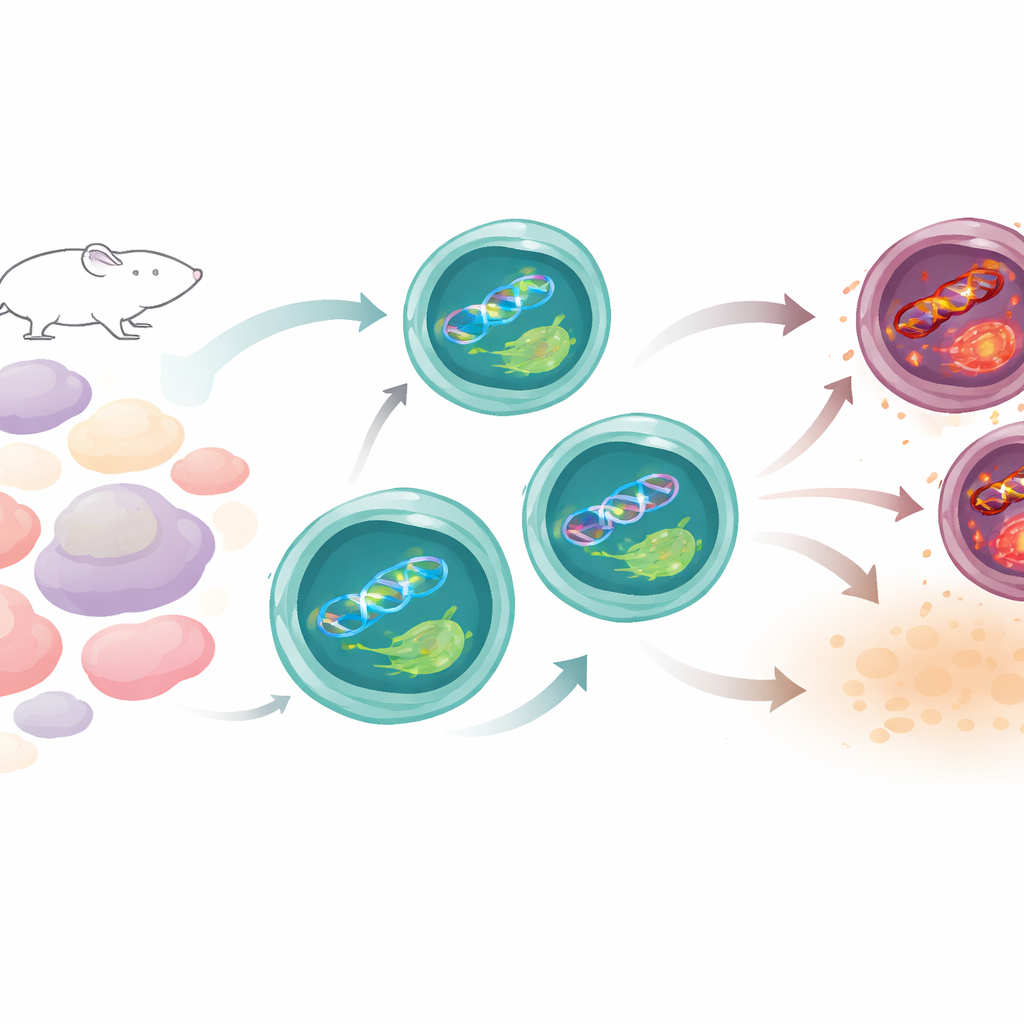
Cómo mantienen el equilibrio las células Th17
Las células Th17 llevan una vida peligrosa. Para funcionar, aumentan su metabolismo y producen especies reactivas de oxígeno—moléculas químicamente reactivas que pueden dañar el ADN. El equipo comparó las células Th17 con otros tipos de células T en ratones y encontró que, pese a su intensa actividad, las Th17 acumulan menos daño en el ADN que muchas de sus parientes. Una pista clave fue que los genes implicados en la reparación del ADN, especialmente los de una vía que normalmente corrige lesiones inducidas por el sol, estaban más activados en las Th17. Entre ellos estaba XPC, una proteína que detecta daños estructurales en el ADN. A medida que las Th17 maduraban, los niveles de XPC aumentaban y se localizaban en sitios dañados del núcleo, lo que sugiere que estaba en patrulla constante para mantener su integridad genética.
Qué ocurre cuando falta el sensor del ADN
Para evaluar la importancia real de XPC, los investigadores usaron ratones modificados para carecer de esta proteína. A primera vista, sus sistemas inmunitarios parecían mayormente normales: el número total de células T y muchos subtipos no cambiaron. Pero cuando el equipo se centró en las células Th17 surgió un defecto llamativo. Sin XPC, muchas menos células producían la molécula característica de las Th17, IL-17, y marcadores de identidad y conmutadores de señalización clave que impulsan el programa Th17 estaban disminuidos. En cultivos, las células T naïve de estos ratones tuvieron dificultades para convertirse en Th17 plenamente diferenciadas. En un modelo estándar en el que la transferencia de células T provoca inflamación intestinal, las células T deficientes en XPC no indujeron colitis, reflejando una capacidad inflamatoria atenuada. Al mismo tiempo, las células T reguladoras, que moderan las respuestas inmunitarias, se hicieron más abundantes, lo que sugiere un cambio en el equilibrio entre agresión y contención.
Daño en el ADN, fábricas de energía y estrés químico
Profundizando más, el equipo halló que las Th17 sin XPC tenían más roturas en las hebras de ADN y más bases de ADN oxidizadas, una firma del ataque por especies reactivas de oxígeno. Los genes que normalmente detectan el daño del ADN y detienen el ciclo celular también estaban reducidos, lo que sugiere un sistema de alarma debilitado. El metabolismo energético de las células se reconfiguró: perdieron parte de su capacidad para emplear vías rápidas de uso de glucosa y se volvieron más dependientes de sus mitocondrias, las pequeñas centrales energéticas de la célula. Sin embargo, estas mitocondrias filtraban más especies reactivas de oxígeno y mostraban signos de estrés, creando un ciclo vicioso de aumento del estrés químico y acumulación de daño en el ADN. De forma notable, tratar las células con un antioxidante restauró la producción de IL-17 y redujo el daño en el ADN, vinculando directamente el estrés oxidativo con el defecto funcional observado.
Un esfuerzo conjunto para reparar el ADN dañado
Más allá de su papel clásico, XPC también trabajó mano a mano con otra proteína reparadora llamada OGG1, que reconoce una base de ADN comúnmente oxidada. Los investigadores demostraron que estas dos proteínas se asocian físicamente en las Th17, ayudando a coordinar la eliminación de bases dañadas. Cuando faltaba XPC, la actividad cortante de OGG1 aumentó, como si intentara compensar el daño excesivo. Pero esta sobreactividad se produjo en un contexto de alto estrés oxidativo y redes de reparación perturbadas, y no fue suficiente para restaurar la función normal de las Th17. Análisis genéticos y estructurales sugirieron que XPC actúa como un nodo que conecta diferentes vías de reparación y el control redox, asegurando que el daño no solo se detecte sino que se procese de modo que la célula pueda seguir dividiéndose y produciendo moléculas protectoras.
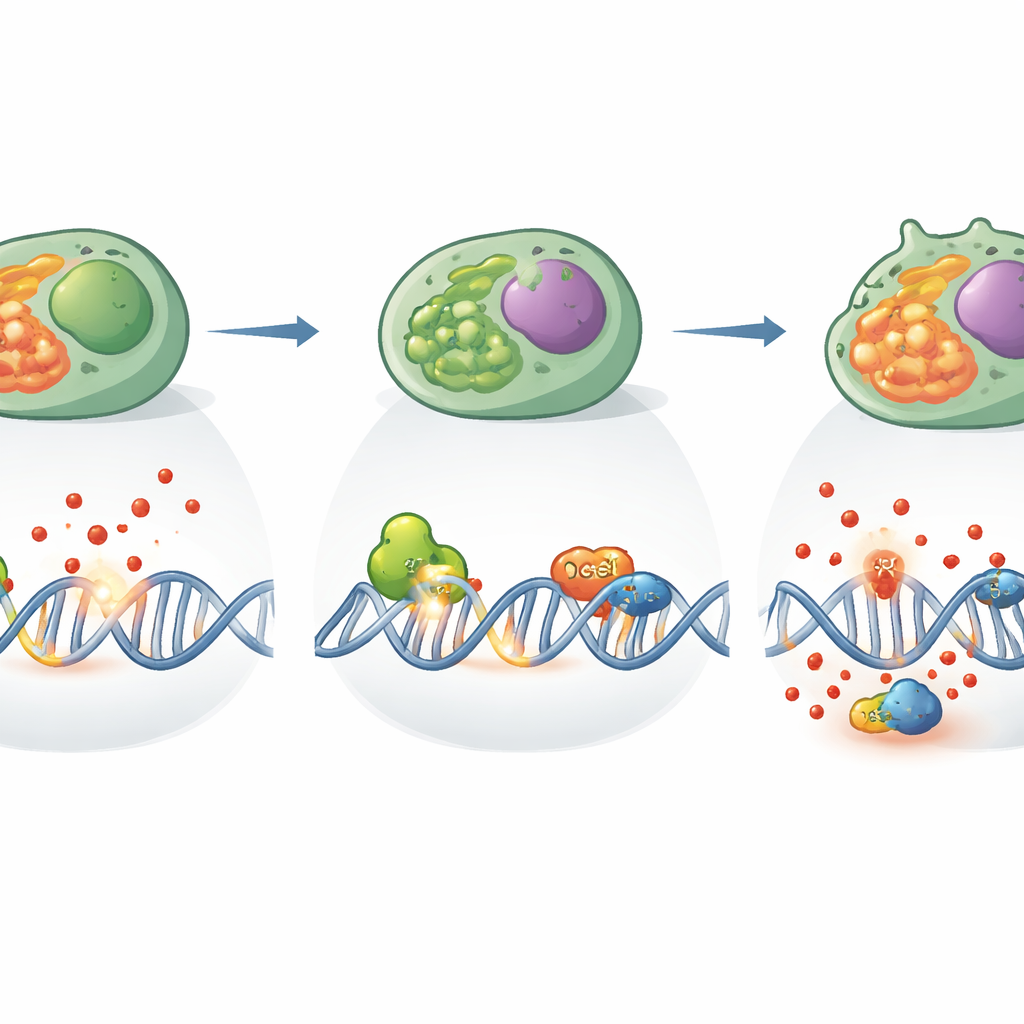
Por qué esto importa para la enfermedad y la terapia
Para un lector general, el mensaje clave es que las células inmunitarias necesitan sus propios guardias internos para mantenerse en forma mientras nos protegen. Este estudio revela que XPC, antes famoso por proteger las células de la piel frente a la radiación UV, es también un guardián vital de las Th17, manteniendo su ADN intacto y sus sistemas energéticos equilibrados bajo estrés oxidativo. Cuando falta XPC, las Th17 se vuelven frágiles desde el punto de vista genético y metabólico, producen menos respuestas inflamatorias y pueden desplazar el balance inmunitario hacia la regulación en lugar del ataque. Dado que las Th17 son centrales en afecciones como la enfermedad inflamatoria intestinal, la psoriasis y la esclerosis múltiple, las vías controladas por XPC podrían convertirse en nuevos objetivos para modular las respuestas inmunitarias—ya sea calmando la inflamación perjudicial o potenciando la defensa donde es insuficiente—al ajustar cómo estas células reparan su ADN y manejan el estrés oxidativo.
Cita: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Palabras clave: células Th17, reparación del ADN, estrés oxidativo, proteína XPC, enfermedad autoinmune