Clear Sky Science · es
La secreción endosomal tardía dependiente de VAMP7 de proteínas del RE y mitocondriales impacta el microambiente tumoral y la implicación de macrófagos
Cómo las células estresadas piden ayuda
Las células cancerosas llevan una vida dura. Privadas de oxígeno y nutrientes, acumulan daños en las pequeñas centrales energéticas (mitocondrias) y en las fábricas de proteínas (retículo endoplásmico, o RE) que contienen. Este estudio revela una forma inesperada en que las células bajo presión expulsan fragmentos dañados de estas estructuras internas al exterior. En tumores cerebrales llamados glioblastomas, este sistema celular de “exportación de desechos”, impulsado por una proteína denominada VAMP7, resulta influir en cómo las células inmunes detectan y penetran en el tumor.
Rutas de envío ocultas dentro de las células
La mayoría de las proteínas que salen de una célula usan una vía clásica: entran en el RE, pasan por una estación central de clasificación llamada aparato de Golgi y luego se empaquetan en pequeñas burbujas que se fusionan con la superficie celular. Pero las células también recurren a rutas no convencionales que evitan el Golgi. Una de esas rutas emplea endosomas tardíos—sacos internos que pueden fusionarse con la membrana y liberar su contenido al exterior. Los autores se centran en una proteína molecular tipo “cremallera”, VAMP7, ya conocida por ayudar a que los endosomas tardíos se fusionen con la membrana externa y liberen pequeñas vesículas extracelulares, paquetes diminutos que transportan mercancía entre células.
Trasladando las piezas desgastadas hacia la salida
Utilizando células de riñón de rata y de glioma modificadas y carentes de VAMP7, los investigadores siguieron qué sucede con proteínas que normalmente se encuentran en el RE y las mitocondrias. Mostraron que sin VAMP7, las células liberaban mucho menos de una forma corta de una proteína modeladora del RE llamada RTN3 y de VDAC, un canal en la superficie mitocondrial. Al mismo tiempo, los endosomas tardíos quedaron mal posicionados y las pequeñas vesículas ricas en el marcador CD63 se secretaron deficientemente. Imágenes de alta resolución y ensayos de proximidad revelaron que RTN3 y material mitocondrial se asocian físicamente con endosomas tardíos positivos para CD63 antes de ser liberados, y que esta transferencia depende de VAMP7 y sus proteínas asociadas de fusión. Estos hallazgos apoyan un modelo en el que el RE y las mitocondrias estresadas forman pequeñas vesículas que brotan y se fusionan con endosomas tardíos, que a su vez exportan su carga fuera de la célula. 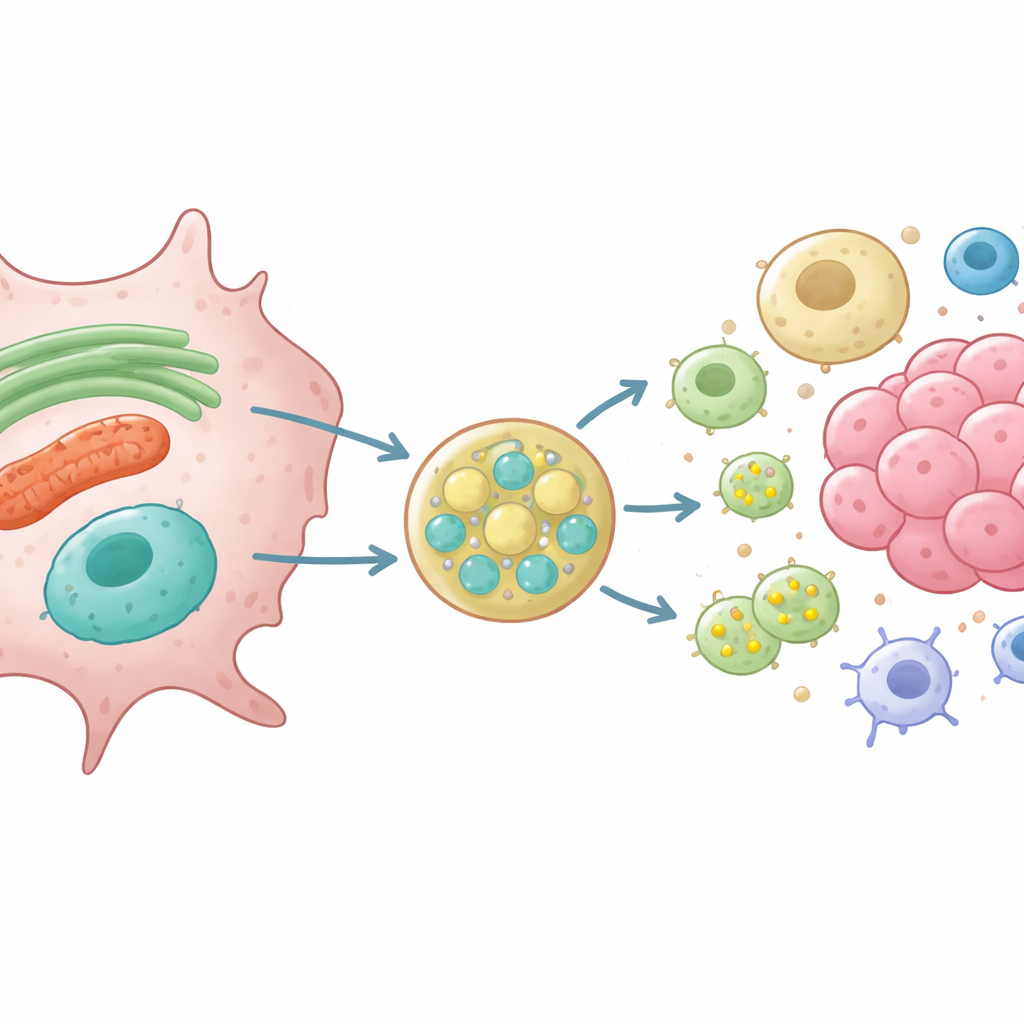
Alivio del estrés y control de calidad
Las células sin VAMP7 no perdieron la vía general de reciclaje conocida como autófagia, pero sí mostraron claros signos de tensión. Los patrones de actividad génica apuntaron a la activación de respuestas al estrés en el RE y a cambios en genes relacionados con mitocondrias. La microscopía reveló “remolinos” anormales de membrana del RE y mitocondrias excesivamente fusionadas y alargadas, ambas señales de orgánulos que luchan por mantener el equilibrio. Las mediciones del consumo de oxígeno mostraron que, pese a tener más masa mitocondrial, las células sin VAMP7 o sin una proteína clave de la autófagia (ATG5) presentaban una producción de energía más débil. Cuando los científicos provocaron deliberadamente estrés en el RE o en las mitocondrias con fármacos, las células con VAMP7 intacto aumentaron la secreción de RTN3 o VDAC, respectivamente. Este aumento se perdió cuando VAMP7 fue eliminado, lo que sugiere que la secreción endosomal tardía actúa como una válvula de alivio para ayudar a desechar componentes dañados y difundir el estado interno de la célula.
Moldeando el vecindario tumoral
Para evaluar la importancia de esta vía en la enfermedad, el equipo recurrió a un modelo de rata de glioblastoma, un tumor cerebral muy agresivo. Implataron células de glioma normales, carentes de VAMP7 o carentes de ATG5 en cerebros de rata. Los tumores originados a partir de células sin VAMP7 crecieron mucho y contenían más tejido muerto, pero presentaron menor infiltración de macrófagos—las células inmunes que engullen desechos y pueden influir en si un tumor progresa o se detiene. En contraste, los tumores sin ATG5 fueron más pequeños en conjunto pero no mostraron la misma caída selectiva en la entrada de macrófagos al núcleo tumoral. Análisis de conjuntos de datos de tumores cerebrales humanos revelaron además que una menor expresión de VAMP7 (y de RTN3) se asocia con una supervivencia peor del paciente, lo que sugiere que esta vía de secreción ligada al estrés puede actuar de forma natural para frenar la progresión tumoral al moldear el paisaje inmunitario. 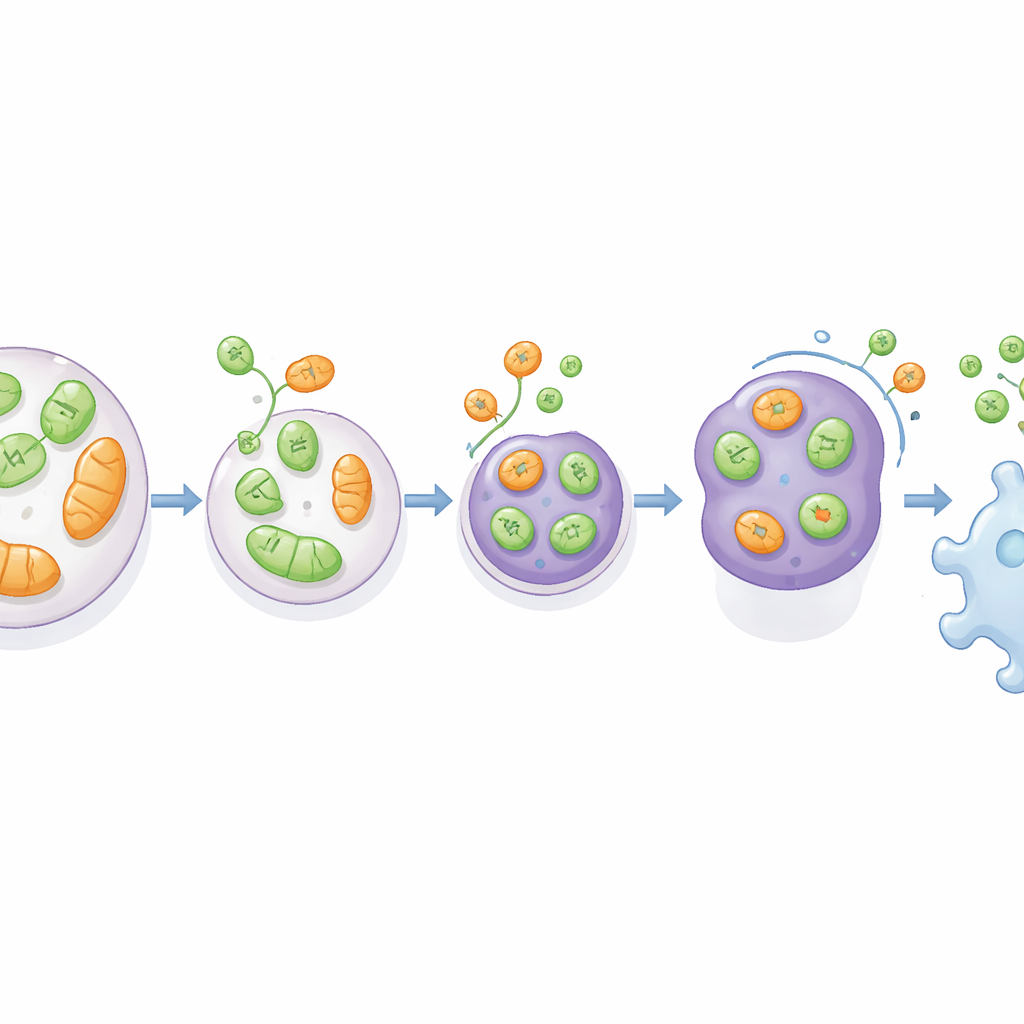
Por qué esto importa para el cáncer y la inmunidad
En términos sencillos, el estudio propone que VAMP7 ayuda a las células a empaquetar y exportar fragmentos dañados de su maquinaria interna vía endosomas tardíos, especialmente bajo estrés. En el glioblastoma, este flujo hacia el exterior de material derivado del RE y de mitocondrias parece servir como una señal de auxilio que anima a los macrófagos a entrar en el tumor y limpiar los desechos, contribuyendo a un entorno más supresor del tumor. Cuando falta VAMP7, la señal se debilita, el daño orgánular se acumula, los tumores se vuelven más necróticos y la implicación de macrófagos disminuye. Comprender y, potencialmente, modular este sistema secretor de control de calidad podría abrir formas nuevas de hacer que tumores resistentes sean más visibles y respondan mejor al sistema inmunitario.
Cita: Vats, S., Dionisio, P., Lemercier, Q. et al. VAMP7-dependent late endosomal secretion of ER and mitochondrial proteins impacts the tumor microenvironment and macrophage engagement. Nat Commun 17, 3012 (2026). https://doi.org/10.1038/s41467-026-69900-4
Palabras clave: secreción de proteínas no convencional, VAMP7, glioblastoma, microambiente tumoral, vesículas extracelulares