Clear Sky Science · es
El factor de iniciación eucariota 6 modula la plasticidad del carcinoma pulmonar de células pequeñas a través del eje de señalización integrina-FAK
Por qué importa esta investigación sobre el cáncer de pulmón
El carcinoma pulmonar de células pequeñas (CPCP) es una de las formas más letales de cáncer de pulmón. Suele responder bien a la quimioterapia inicialmente, pero casi siempre reaparece, de forma rápida y agresiva. Este estudio plantea una pregunta central: ¿qué permite a las células del CPCP “cambiar de personalidad” y volverse resistentes a los fármacos, y se puede frenar o bloquear ese cambio de forma?
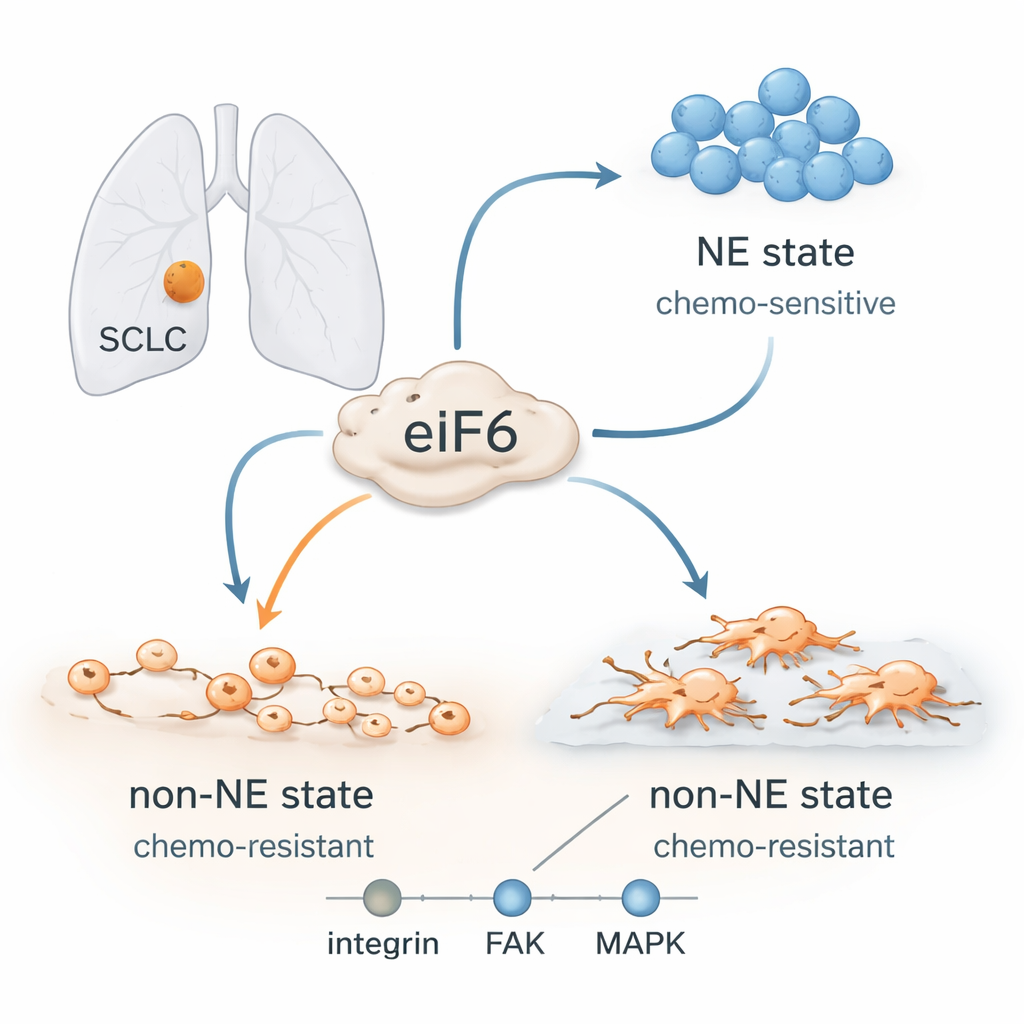
Células cancerosas que cambian de forma
Antes los médicos pensaban que el CPCP era una enfermedad uniforme, pero ahora está claro que estos tumores contienen distintos tipos celulares. Algunas células tienen una identidad “neuroendocrina” pronunciada: crecen en agregados flotantes compactos, responden bien a la quimioterapia basada en platino y suelen ser ricas en ciertas proteínas de tipo nervioso. Otras pierden esa identidad y adoptan un estado “no neuroendocrino”: se expanden, se adhieren al tejido circundante, muestran características de células más móviles e invasivas y son mucho más difíciles de eliminar con fármacos. Los tumores de los pacientes a menudo evolucionan del estado sensible al resistente durante o después del tratamiento, aunque su ADN cambie poco. Eso apunta a programas celulares flexibles más que a nuevas mutaciones como motor de la recaída.
Un factor de traducción con doble vida
Los autores se centraron en una proteína llamada eIF6, conocida sobre todo por ayudar en el ensamblaje de los ribosomas, las fábricas de proteínas de la célula. Estudiando muestras de pacientes, modelos de ratón y varias líneas celulares humanas de CPCP, encontraron que los niveles de eIF6 aumentaban de forma consistente cuando las células pasaban al estado no neuroendocrino resistente a fármacos. Sorprendentemente, este aumento coincidía con una caída general en la producción total de proteínas, lo que sugiere que eIF6 podría estar haciendo algo más que su función clásica. Análisis detallados de cómo los ARNm se asocian a los ribosomas mostraron que las partes básicas del ribosoma no cambiaban mucho. En cambio, se remodeló la forma en que se seleccionaban y procesaban los mensajes para la traducción cuando las células cambiaban de identidad.
Separarse para conectarse a señales de supervivencia
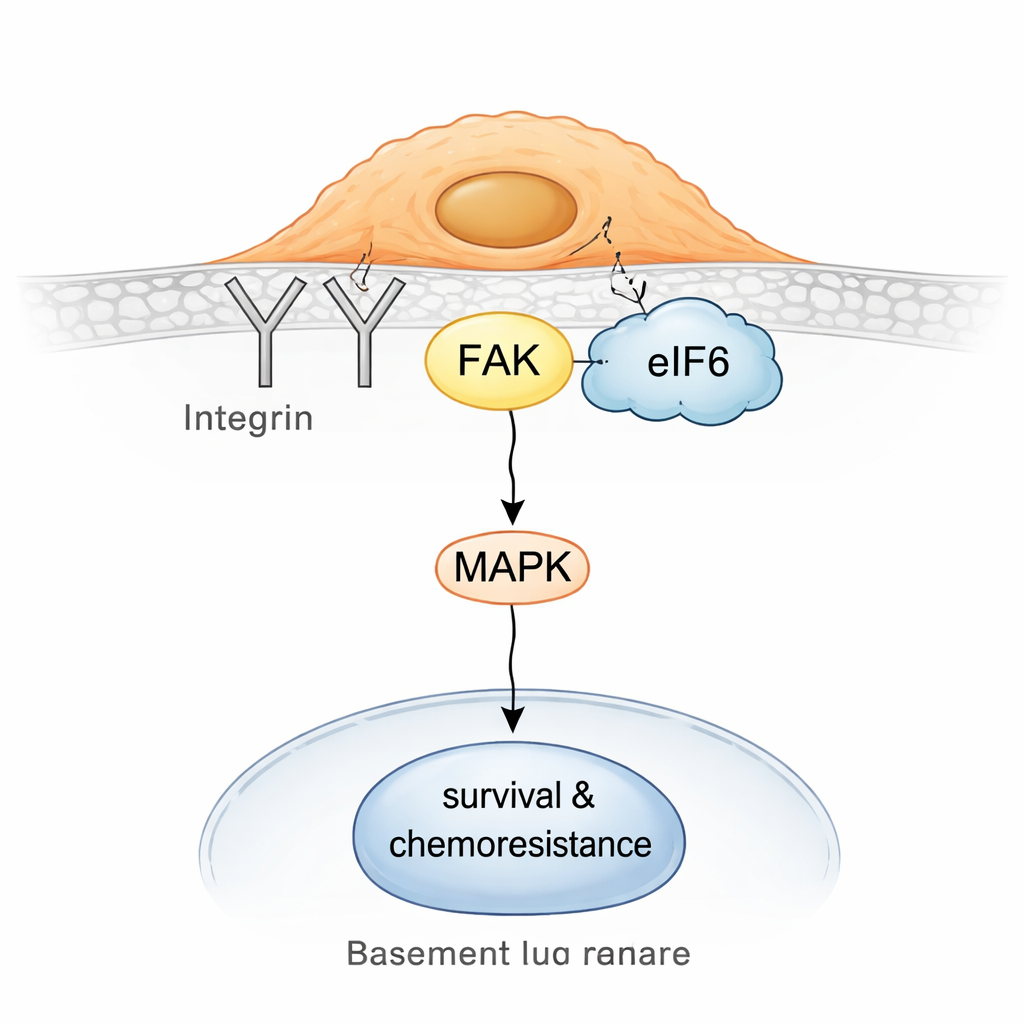
Al profundizar, el equipo descubrió que en las células resistentes eIF6 se desprende en parte de los ribosomas y se asocia con un centro de señalización en la superficie formado por integrinas y una proteína llamada quinasas de adhesión focal (FAK). Las integrinas ayudan a las células a sentir y adherirse al entorno; FAK transmite esas señales hacia el interior, a menudo activando vías que apoyan el movimiento, la supervivencia y la tolerancia a fármacos. Ensayos bioquímicos de captura y pruebas de proximidad in situ mostraron que eIF6 interactúa físicamente con la integrina CD104 y con FAK, y que estos complejos son más abundantes en células no neuroendocrinas. Este ensamblaje eIF6–integrina–FAK, a su vez, potencia la actividad en la vía de señalización MAPK, un conocido impulsor del crecimiento y la resistencia al estrés.
Volver a hacer vulnerables a los tumores resistentes
Los investigadores se preguntaron entonces si manipular eIF6 podría cambiar el comportamiento del CPCP. Cuando redujeron los niveles de eIF6 en células resistentes, los genes asociados a un programa móvil y formador de cicatriz (epitelio–mesénquima) se redujeron, mientras que los genes neuroendocrinos clásicos se restauraron parcialmente. Estos cambios no revertían por completo el estado, pero ralentizaron la transición hacia la resistencia. De forma crucial, las células con menos eIF6 se volvieron más sensibles a la quimioterapia estándar con carboplatino–etopósido en cultivo y en tumores de ratón, con menos colonias sobrevivientes y una reducción más duradera. Dado que actualmente no existen fármacos específicos contra eIF6, el equipo probó inhibidores de FAK que ya están en desarrollo clínico. Bloquear la señalización FAK volvió a sensibilizar las células resistentes a la quimioterapia y, en ratones, el tratamiento combinado produjo el control tumoral más eficaz.
Del hallazgo en el laboratorio a herramientas futuras para pacientes
Por último, los autores examinaron muestras tumorales de pacientes con CPCP en estadio limitado que habían sido operados. Usando un método de tinción sensible que ilumina las proteínas solo cuando están próximas, midieron con qué frecuencia eIF6 forma complejos con CD104 o FAK dentro de las células tumorales. Altos niveles de estos complejos—más que de eIF6 por sí solo—se asociaron con recurrencia más temprana y supervivencia más corta, lo que los señala como marcadores pronósticos prometedores. En conjunto, este trabajo revela que eIF6 puede “hacer la doble función” separándose de los ribosomas para ayudar a conectar a las células cancerosas con circuitos potentes de supervivencia. Al mapear este eje eIF6–integrina–FAK, el estudio sugiere formas de identificar a pacientes con mayor riesgo de recaída y respalda la combinación de inhibidores de FAK con quimioterapia para contrarrestar la peligrosa plasticidad del CPCP.
Cita: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Palabras clave: carcinoma pulmonar de células pequeñas, resistencia a fármacos, plasticidad celular, eIF6, señalización integrina FAK