Clear Sky Science · es
Inhibición de la traducción dependiente del contexto como modalidad terapéutica contra el cáncer
Volver las fábricas de proteínas contra el cáncer
Las células cancerosas sobreviven fabricando constantemente grandes cantidades de proteínas «conductoras» de corta vida que las mantienen creciendo y dividiéndose. Este estudio explora una nueva forma de combatir el cáncer atascando sutilmente las máquinas productoras de proteínas de la célula —los ribosomas— solo cuando intentan ensamblar secuencias proteicas concretas, en especial las presentes en oncogenes difíciles de tratar como MYC. Esa interferencia selectiva podría matar las células tumorales mientras se preserva gran parte de la producción proteica normal.
Cómo construyen las células las proteínas —y dónde pueden fallar las cosas
Cada célula depende de los ribosomas, pequeñas fábricas moleculares que leen mensajes genéticos (ARNm) y enlazan aminoácidos para formar proteínas. La mayoría de los fármacos existentes que atacan a los ribosomas, como los antibióticos o fármacos oncológicos antiguos, actúan como instrumentos contundentes: bloquean de forma amplia la síntesis proteica, lo que puede dañar células sanas y causar efectos adversos graves. Los autores razonaron que, puesto que cada cadena proteica naciente tiene su propia secuencia y carácter químico únicos, podría ser posible diseñar pequeñas moléculas que solo bloqueen el ribosoma cuando una secuencia específica esté dentro de la máquina, dejando el resto de la producción proteica celular en gran medida intacta.
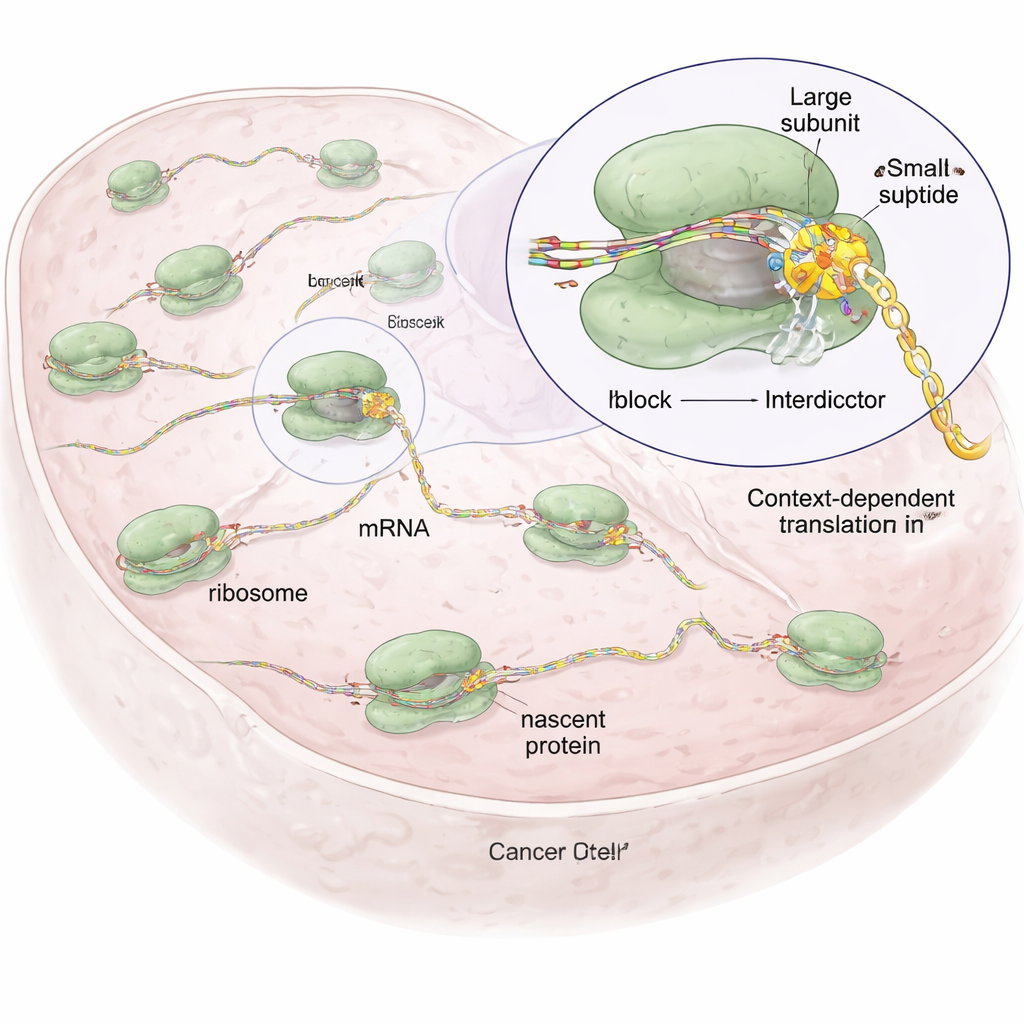
Moléculas diseñadas que detienen solo ciertas secuencias proteicas
Partiendo de un compuesto natural llamado anisomicina, que se une al corazón catalítico del ribosoma donde se forman los enlaces peptídicos, los investigadores crearon una familia de moléculas sintéticas a las que denominan «interdictores». Todas comparten un andamiaje central que las ancla dentro del ribosoma, pero difieren en grupos laterales que apuntan hacia la cadena proteica en crecimiento. Esos grupos laterales están ajustados para favorecer tipos concretos de aminoácidos; por ejemplo, un interdictor (IDB‑001) se atrae por residuos cargados negativamente, mientras que otro (IDB‑002) prefiere residuos pequeños y aceitosos (hidrofóbicos). Mediante una técnica llamada ribosome profiling, que cartografía de forma global dónde se detienen los ribosomas sobre los ARNm dentro de las células, el equipo demostró que cada compuesto provoca detenciones en motivos cortos y distintos de la cadena naciente, a menudo en el aminoácido penúltimo (−1), lo que evidencia una acción dependiente de la secuencia en lugar de un apagado indiscriminado.
Observar el encuentro entre el fármaco y el ribosoma átomo por átomo
Para ver en detalle físico cómo funciona esa selectividad, los autores congelaron ribosomas humanos en el acto de traducir secuencias peptídicas diseñadas y los visualizaron mediante microscopía electrónica criogénica a resolución casi atómica. Observaron al interdictor alojado en el sitio activo del ribosoma haciendo contactos precisos con los últimos aminoácidos de la cadena naciente. En una estructura, un grupo lateral hidrofóbico de IDB‑002 queda acunado por residuos pequeños y no voluminosos en el péptido, lo que explica por qué allí se desaconsejan cadenas laterales más grandes. En otra, la cadena lateral ácida de un residuo derivado de MYC se orienta para formar un puente salino con un grupo cargado positivamente en IDB‑001. La presencia del fármaco también desplaza bases de ARN ribosómico cercanas hacia nuevas posiciones que constriñen el sitio activo y bloquean parcialmente la entrada del siguiente ARNt, contribuyendo a congelar la elongación en esas secuencias favorecidas.
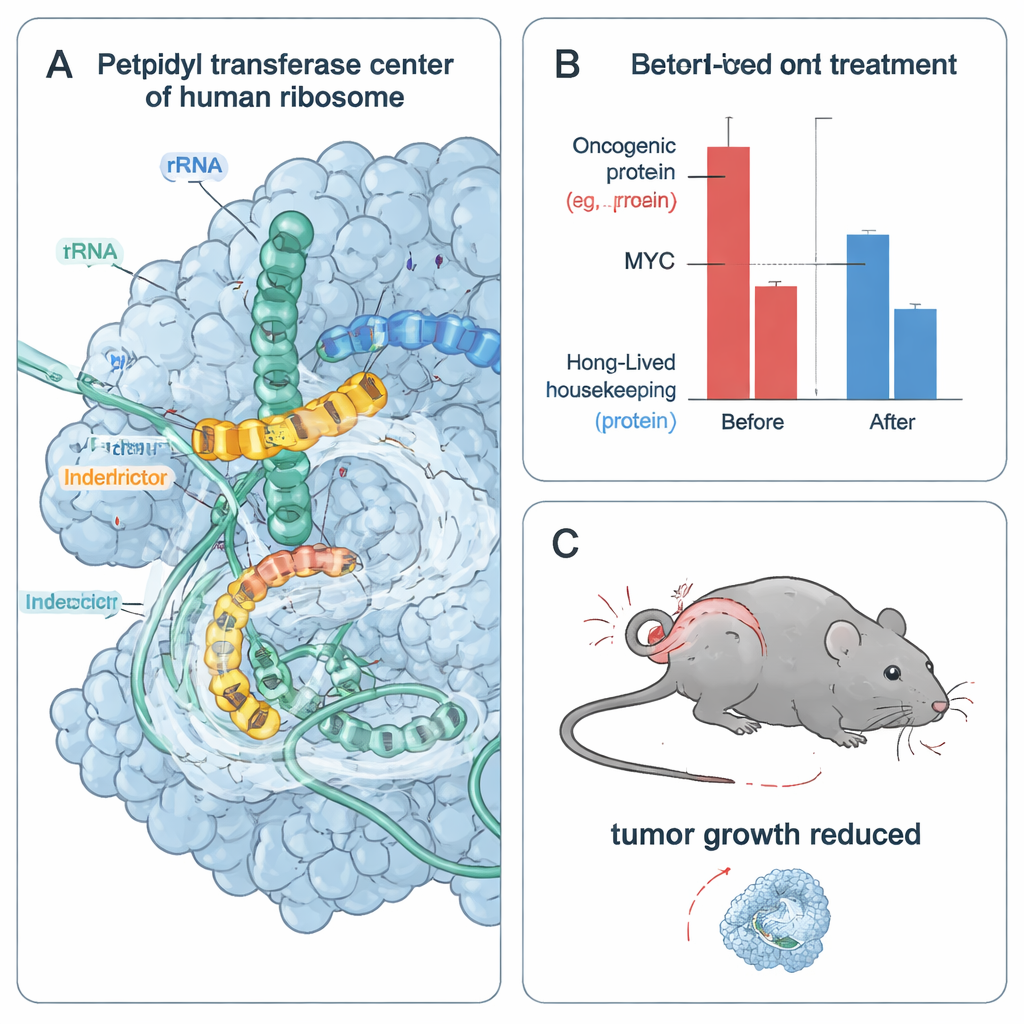
De ribosomas atascados a células tumorales estresadas y moribundas
Puesto que las células cancerosas que se dividen rápidamente dependen en gran medida de proteínas oncongénicas de vida corta como MYC y CCND1, el equipo evaluó cómo afectan los interdictores a la supervivencia celular tumoral. En varias líneas celulares cancerosas dependientes de MYC, IDB‑001 e IDB‑002 redujeron la viabilidad celular en concentraciones nanomolares a micromolares bajas. Un análogo optimizado adicional, IDB‑003, resultó aún más potente y apto para administración oral. En las células, estos compuestos agotaron con rapidez MYC y otras oncoproteínas de recambio rápido, mientras que las proteínas domésticas de vida más larga permanecieron relativamente estables en la misma ventana temporal. Los fármacos también desencadenaron respuestas de estrés celular vinculadas a ribosomas colisionados, pero bloquear esas vías de señalización de estrés no eliminó la pérdida de viabilidad, lo que sugiere que la privación directa de proteínas oncongénicas esenciales es un motor principal de la muerte de las células tumorales.
Prueba de concepto en un modelo de cáncer de mama difícil
Para probar si este enfoque funciona en animales, los autores trataron ratones con tumores humanos de cáncer de mama triple negativo mediante administración oral de IDB‑003. Durante 28 días, los tumores tratados crecieron mucho más despacio que los de los animales control, con hasta un 80 % de inhibición del crecimiento tumoral a dosis más altas y sin toxicidad grave reportada en este estudio. El análisis de la expresión génica de los tumores mostró una fuerte regulación a la baja de los programas génicos diana de MYC, coherente con una reducción de la actividad de MYC in vivo. En conjunto, estos resultados indican que bloquear selectivamente los ribosomas en secuencias proteicas específicas puede debilitar tumores que dependen de conductores oncongénicos inestables, a la vez que potencialmente evita la toxicidad general de los inhibidores clásicos de la traducción.
Por qué esto importa para futuros tratamientos contra el cáncer
Este trabajo presenta un nuevo tipo de fármaco de pequeña molécula: uno que no actúa uniéndose a una proteína terminada, sino interceptándola mientras se fabrica y solo cuando está presente una corta «etiqueta de dirección» en la secuencia. Dado que muchas proteínas promotoras de cáncer son flexibles, de vida corta o carecen de cavidades evidentes para fármacos convencionales, dirigir su síntesis directamente en el ribosoma podría abrir una vía para tratar tumores impulsados por genes actualmente «intratables» como MYC. El estudio también sugiere que, afinando la química de los interdictores, futuros medicamentos podrían diseñarse para centrarse en diferentes motivos de secuencia y dianas de enfermedad, extendiendo esta estrategia más allá de la oncología a otras condiciones en las que reducir proteínas específicas podría restaurar la salud.
Cita: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Palabras clave: terapia contra el cáncer dirigida al ribosoma, inhibición de la traducción, tumores impulsados por MYC, pequeñas moléculas dependientes del contexto, cáncer de mama triple negativo