Clear Sky Science · es
La subunidad COMPASS Bre2 regula el remodelador de cromatina Arp9 para controlar la síntesis de aflatoxina y la virulencia de Aspergillus flavus
Por qué un moho alimentario importa para tu salud
Las aflatoxinas son venenos producidos por ciertos mohos que crecen en cultivos como cacahuetes y maíz. La más peligrosa, la aflatoxina B1, es un potente carcinógeno hepático que puede contaminar alimentos y piensos. Este estudio desvela cómo el hongo común que infecta cultivos, Aspergillus flavus, activa la maquinaria que sintetiza aflatoxina y aumenta su capacidad para infectar plantas y animales, señalando vías nuevas para evitar la contaminación antes de que llegue a nuestros platos.
Un interruptor de control oculto dentro del ADN fúngico
Dentro de cada célula de A. flavus, largas hebras de ADN se enrollan alrededor de proteínas para formar cromatina, que actúa como un guardián de la actividad génica. Los autores se centran en una proteína llamada Bre2, parte de un complejo mayor COMPASS que coloca pequeñas marcas químicas en las histonas, especialmente en una posición conocida como H3K4. Estas marcas no cambian la secuencia del ADN en sí, pero influyen en si los genes se encienden o se apagan. El equipo muestra que Bre2 es crucial para añadir marcas activadoras (H3K4me2 y H3K4me3), y que eliminar el gen bre2 reduce drásticamente estas señales en regiones clave del genoma fúngico.
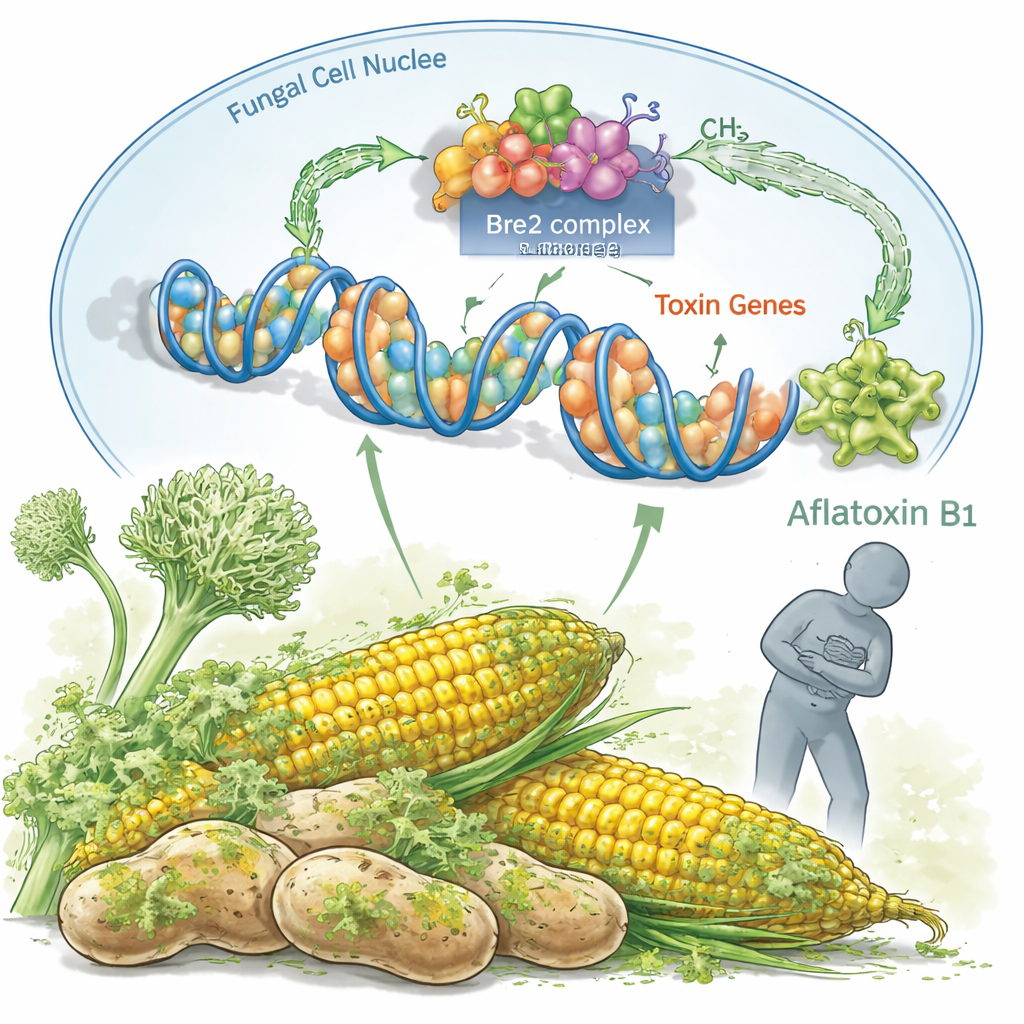
De las marcas génicas al crecimiento del moho y la producción de toxinas
Cuando Bre2 se elimina, el hongo se vuelve lento y menos capaz de reproducirse. Las colonias crecen menos de la mitad de su tamaño normal y el número de esporas, que diseminan el hongo, desciende de forma dramática. El hongo también deja de formar estructuras de reposo resistentes llamadas esclerocios, que le ayudan a sobrevivir en el suelo y en cultivos almacenados. Al mismo tiempo, la producción de aflatoxina B1 cae en picado, según pruebas químicas. El estudio vincula esta caída en la producción de toxina con una actividad más débil en el clúster de genes de aflatoxina, un grupo de unas 30 genes estrechamente coordinados. Sin Bre2, los interruptores maestros aflR y aflS y varios genes constructores de toxinas quedan reprimidos, de modo que el hongo simplemente no puede fabricar tanto veneno.
Infección más débil de cultivos e insectos
Las consecuencias de perder Bre2 se extienden del plato de laboratorio a huéspedes vivos. Cuando los investigadores infectaron granos de cacahuete y maíz con el hongo deficiente en bre2, observaron un crecimiento fúngico mucho más escaso y muchas menos esporas en la superficie del grano. Los granos también contenían mucho menos aflatoxina B1. Efectos similares aparecieron en modelos animales: larvas de insectos infectadas con el hongo mutante sobrevivieron más tiempo y portaron menos esporas y menos toxina que las expuestas a A. flavus normal. El trabajo muestra además que genes fúngicos vinculados a la degradación de las defensas del hospedador están menos activos sin Bre2, lo que sugiere que esta proteína ayuda al patógeno tanto a crecer como a evadir la inmunidad de sus hospedadores.
Una asociación con un remodelador de cromatina
Para entender cómo las marcas de histonas de Bre2 se traducen en cambios amplios en la actividad génica, los autores buscaron actores aguas abajo. Mediante mapeo a escala del genoma, encontraron que Bre2 marca fuertemente y potencia la expresión de un gen llamado arp9, que codifica un componente de un complejo remodelador de cromatina. Esta proteína Arp9 ayuda a desplazar y aflojar nucleosomas, abriendo tramos de ADN para que los genes puedan ser leídos. Cuando se elimina arp9, A. flavus presenta muchos de los defectos observados en el mutante bre2: crecimiento deficiente, bajo recuento de esporas, ausencia de esclerocios y casi nula producción de aflatoxina en medios y en granos de cultivo. Estudios proteicos detallados revelan que Arp9 actúa junto con otras subunidades del remodelador (incluyendo RSC8, Arp7 y Sth1) para remodelar la cromatina.
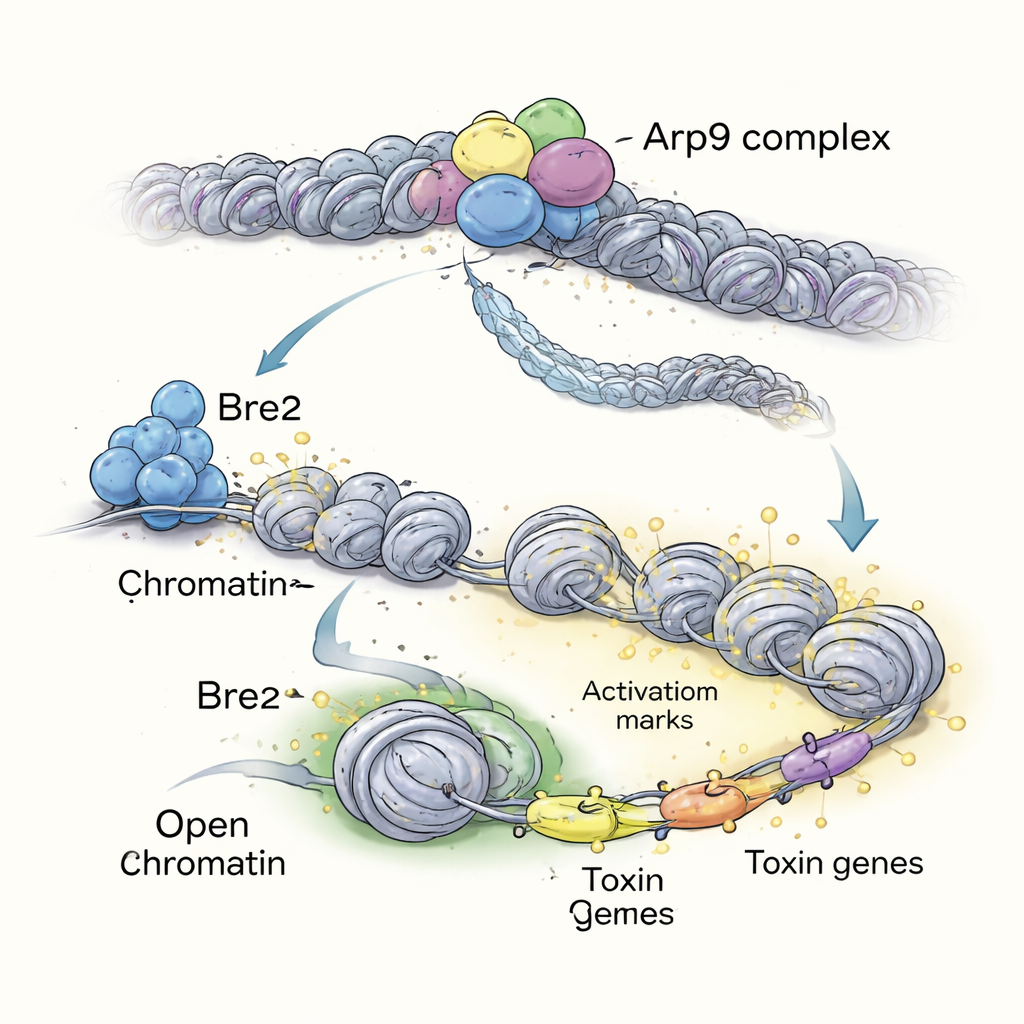
Genes aguas abajo que ajustan la virulencia y las toxinas
Al sondear la accesibilidad de distintas regiones del ADN en hongos carentes de Arp9, los investigadores identificaron más de 200 genes que dependen de este remodelador para mantenerse activos. Muchos de estos genes están involucrados en metabolismo, respuestas al estrés y producción de compuestos secundarios como toxinas. El equipo eliminó luego un conjunto de genes controlados por Arp9 uno por uno. Varios, incluido un proteínade membrana llamado SMAP y transportadores como CDR1 y UMF1, resultaron ser importantes para el crecimiento de la colonia, la formación de esporas, el desarrollo de esclerocios y la síntesis de aflatoxina B1. En algunos mutantes, la producción de toxina quedó completamente bloqueada. Esto sitúa a Bre2 en la cima de una vía “epigenética”: Bre2 marca la cromatina, activa arp9, y Arp9 a su vez abre la cromatina en muchos genes diana que afinan la virulencia fúngica y la producción de toxinas.
Qué significa esto para alimentos más seguros
En términos sencillos, el estudio traza una cadena de mando dentro de A. flavus que controla cuán agresivamente crece y cuánto aflatoxina produce. Bre2 actúa como un interruptor al decorar histonas, lo que activa a Arp9 y sus socios para abrir o cerrar tramos de ADN ligados a genes de desarrollo y de toxinas. Interrumpir este eje Bre2–Arp9, o algunos de sus blancos clave, debilita notablemente al hongo y casi detiene la producción de aflatoxinas. Estos hallazgos sugieren que tratamientos antifúngicos futuros o estrategias de protección de cultivos podrían dirigirse a componentes epigenéticos y de remodelado de la cromatina para mantener a este moho peligroso bajo control antes de que contamine los alimentos.
Cita: Zhuang, Z., Sun, M., Wu, D. et al. COMPASS subunit Bre2 regulates chromatin remodeler Arp9 to control Aspergillus flavus aflatoxin synthesis and virulence. Nat Commun 17, 1862 (2026). https://doi.org/10.1038/s41467-026-69877-0
Palabras clave: aflatoxina, Aspergillus flavus, epigenética, remodelado de cromatina, control de micotoxinas