Clear Sky Science · es
Identificación de la señalización ephrin-A1–EphA2 como posible diana para la prevención de fracturas
Por qué importa proteger los huesos frágiles
A medida que las personas envejecen, sus huesos pueden volverse delgados y quebradizos, convirtiendo percances cotidianos, como tropezar con una alfombra, en fracturas graves. Estas fracturas osteoporóticas no solo son dolorosas, sino también costosas para los sistemas de salud y pueden restar años de vida sana. Los medicamentos actuales ayudan, pero normalmente se reservan para personas con osteoporosis establecida y pueden presentar efectos adversos raros pero preocupantes. Este estudio plantea una pregunta prospectiva: ¿podemos usar la genética y las mediciones de proteínas en grandes poblaciones para descubrir formas completamente nuevas de fortalecer el hueso y prevenir fracturas antes de que ocurran?
Buscando pistas de fractura en la sangre
Los investigadores comenzaron tratando a las proteínas circulantes del cuerpo como un gran libro de pistas. Muchos fármacos ya actúan sobre proteínas en la sangre, por lo que encontrar proteínas que influyan realmente en el riesgo de fractura podría señalar directamente nuevas terapias. Usando muestras del UK Biobank, examinaron variantes genéticas que elevan o disminuyen los niveles de 1.615 proteínas sanguíneas diferentes. Luego vincularon estas “huellas proteicas” genéticas con datos de un enorme estudio genético de más de 50.000 casos de fractura de antebrazo. Un método estadístico llamado aleatorización mendeliana les permitió preguntar: cuando las personas nacen con genes que aumentan o disminuyen el nivel de una proteína, ¿cambia su riesgo de fractura durante toda la vida de forma consistente?
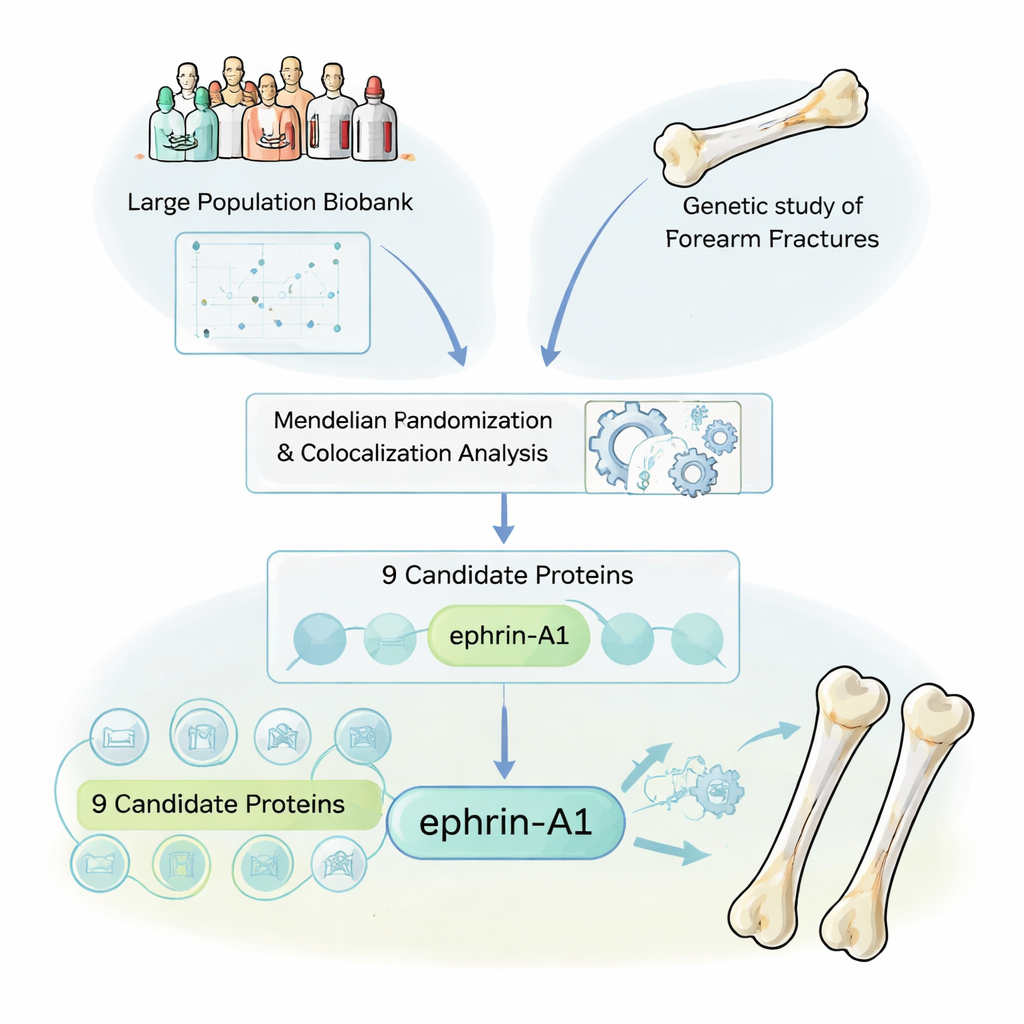
Separando señales reales del ruido genético
Dado que los genes cercanos suelen viajar juntos, el equipo utilizó una segunda capa de análisis, llamada colocación, para asegurarse de que observaban causa y efecto reales en lugar de vecinos genéticos engañosos. De las 1.615 proteínas, nueve destacaron por estar vinculadas causalmente con fracturas de antebrazo. Es importante señalar que varias de estas ya eran conocidas como actuantes en el hueso: la esclerostina y el osteoprotegerina, que son dianas de fármacos para la osteoporosis existentes, y otras proteínas estrechamente vinculadas a la densidad mineral ósea. Su redescubrimiento proporcionó un control de calidad crucial, mostrando que el método podía volver a identificar dianas farmacológicas probadas al tiempo que sacaba a la luz candidatas nuevas.
Un protector sorprendente: ephrin-A1
Entre las proteínas recientemente destacadas, una en particular atrajo la atención: ephrin‑A1. Las personas con predisposición genética a tener niveles sanguíneos más altos de ephrin‑A1 presentaban huesos más densos y menos fracturas de antebrazo. Ephrin‑A1 normalmente está unida a la superficie celular y puede desprenderse hacia el torrente sanguíneo. Se une a un receptor llamado EphA2, que el equipo halló altamente expresado en las células formadoras de hueso llamadas osteoblastos. Al examinar tejidos humanos y de ratón mediante secuenciación unicelular, imagen de ARN in situ y una avanzada técnica 3D de aclaramiento denominada “DeepBone”, observaron un patrón consistente: ephrin‑A1 se localiza en las células de revestimiento de los vasos sanguíneos dentro del hueso, mientras que EphA2 se encuentra en los osteoblastos a lo largo de la superficie ósea, a menudo separados por apenas unas pocas diámetros celulares. Esta disposición hace que la comunicación directa célula a célula entre las células vasculares y las formadoras de hueso no solo sea posible, sino también probable.
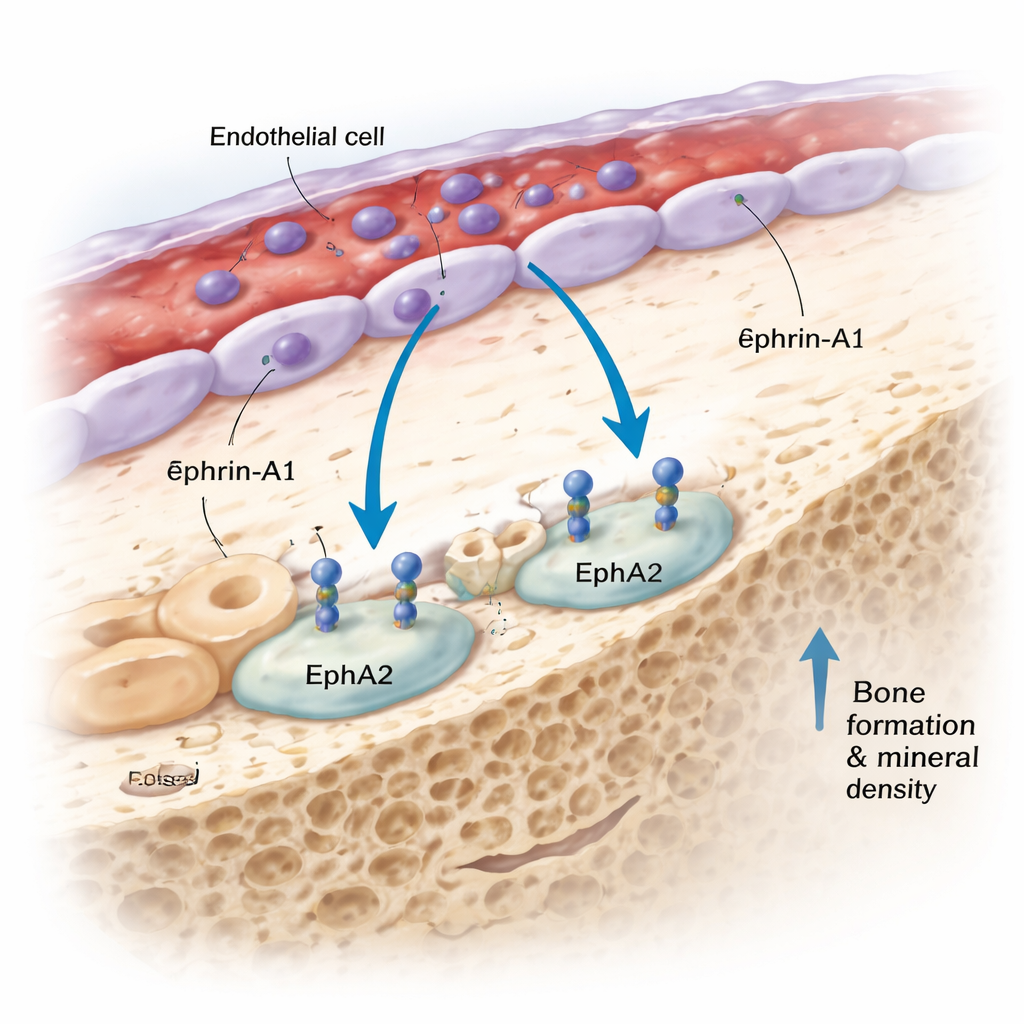
Ponerse a prueba en huesos vivos
Para averiguar si esta conversación ephrin‑A1–EphA2 realmente importa para la resistencia ósea, los investigadores recurrieron a la genética en ratones. Los ratones diseñados para carecer de ephrin‑A1 o de su receptor EphA2 presentaron una densidad mineral ósea corporal total significativamente menor que sus compañeros normales, en ambos sexos. El equipo examinó entonces cómo se comportaba este par señalizador en distintos modelos de ratón que imitan la pérdida y ganancia de hueso humana. La inflamación, el envejecimiento y la administración de dosis altas de vitamina A—cada uno conocido por debilitar el hueso—se asociaron con una reducción de la expresión de ephrin‑A1 y/o EphA2 en tejido óseo. En contraste, la carga mecánica, que imita el efecto beneficioso del ejercicio con carga de peso, aumentó la expresión de ephrin‑A1. Cabe destacar que estos cambios no reflejaron los observados con los fármacos actuales para la osteoporosis, lo que sugiere que ephrin‑A1–EphA2 podría operar por una vía distinta que podría complementar las terapias existentes.
Qué significa esto para la prevención futura de fracturas
En conjunto, el estudio demuestra que un enfoque sofisticado que combina genética y proteínas puede redescubrir dianas conocidas para fármacos óseos y descubrir otras nuevas. Señala a ephrin‑A1, que interactúa con EphA2 en los osteoblastos, como una señal clave que ayuda a mantener los huesos densos y resistentes. Para un lector no especializado, el mensaje principal es que nuestra sangre y nuestros genes contienen planos detallados de cómo se mantienen fuertes los huesos, y que ephrin‑A1 es ahora un interruptor prometedor en ese plano. Si futuros estudios logran activar este interruptor con seguridad, quizá mediante fármacos que potencien la señalización ephrin‑A1–EphA2, podría ofrecer una vía nueva y potencialmente más segura para prevenir fracturas, sobre todo en las muchas personas que actualmente quedan sin tratamiento.
Cita: Movérare-Skrtic, S., Nethander, M., Li, L. et al. Identification of ephrin-A1–EphA2 signalling as a potential target for fracture prevention. Nat Commun 17, 1988 (2026). https://doi.org/10.1038/s41467-026-69863-6
Palabras clave: osteoporosis, densidad mineral ósea, prevención de fracturas, ephrin-A1 EphA2, aleatorización mendeliana