Clear Sky Science · es
La ingeniería in situ de TRIM13 potencia la capacidad antiinflamatoria de los CAR‑M para la terapia de la fibrosis hepática
Reprogramando al equipo de limpieza del hígado
La fibrosis hepática, un proceso de cicatrización que puede derivar en cirrosis e insuficiencia hepática, afecta a millones de personas y actualmente tiene pocas opciones terapéuticas efectivas. Este estudio explora una forma de aprovechar y reprogramar a las propias células inmunitarias del hígado para que no solo eliminen las células formadoras de cicatriz, sino que también apacigüen la inflamación dañina, lo que podría ofrecer una terapia más segura y potente para la enfermedad hepática crónica.
Por qué es tan difícil frenar la cicatrización hepática
Cuando el hígado se lesiona repetidamente —por virus, alcohol o enfermedad metabólica— intenta sanar depositando tejido cicatricial. Células especializadas llamadas células estrelladas hepáticas pasan a un estado “activado” y secretan fibras resistentes, como si obreros vertieran hormigón. Con el tiempo, esta cicatrización, conocida como fibrosis, deforma el órgano y deteriora su función. Las células inmunitarias llamadas macrófagos están en el centro de este proceso. En un hígado dañado, pueden comportarse como una espada de doble filo: en un modo promueven la inflamación y activan las células estrelladas, mientras que en otro, más reparador, ayudan a descomponer la cicatriz y restaurar el equilibrio.
Convertir señales dañinas en respuestas útiles
Los investigadores se centraron en una señal de peligro clave en hígados lesionados: ADN mitocondrial que se filtra desde células dañadas. Los macrófagos detectan este ADN a través de una vía conocida como cGAS‑STING, que los empuja hacia un estado proinflamatorio y pro‑fibrogénico. Una proteína llamada TRIM13 suele ayudar a frenar a STING marcándolo para su destrucción. El equipo razonó que aumentar TRIM13 dentro de los macrófagos hepáticos podría reconducirlos hacia un modo calmante y reparador del tejido. Al mismo tiempo, querían que estas células persiguieran y eliminaran directamente a las células estrelladas formadoras de cicatriz. Para ello utilizaron el concepto del receptor de antígeno quimérico (CAR) tomado de la terapia contra el cáncer: un receptor sintético que permite a las células inmunitarias reconocer un objetivo elegido —en este caso, una proteína llamada FAP que abunda en las células estrelladas activadas.
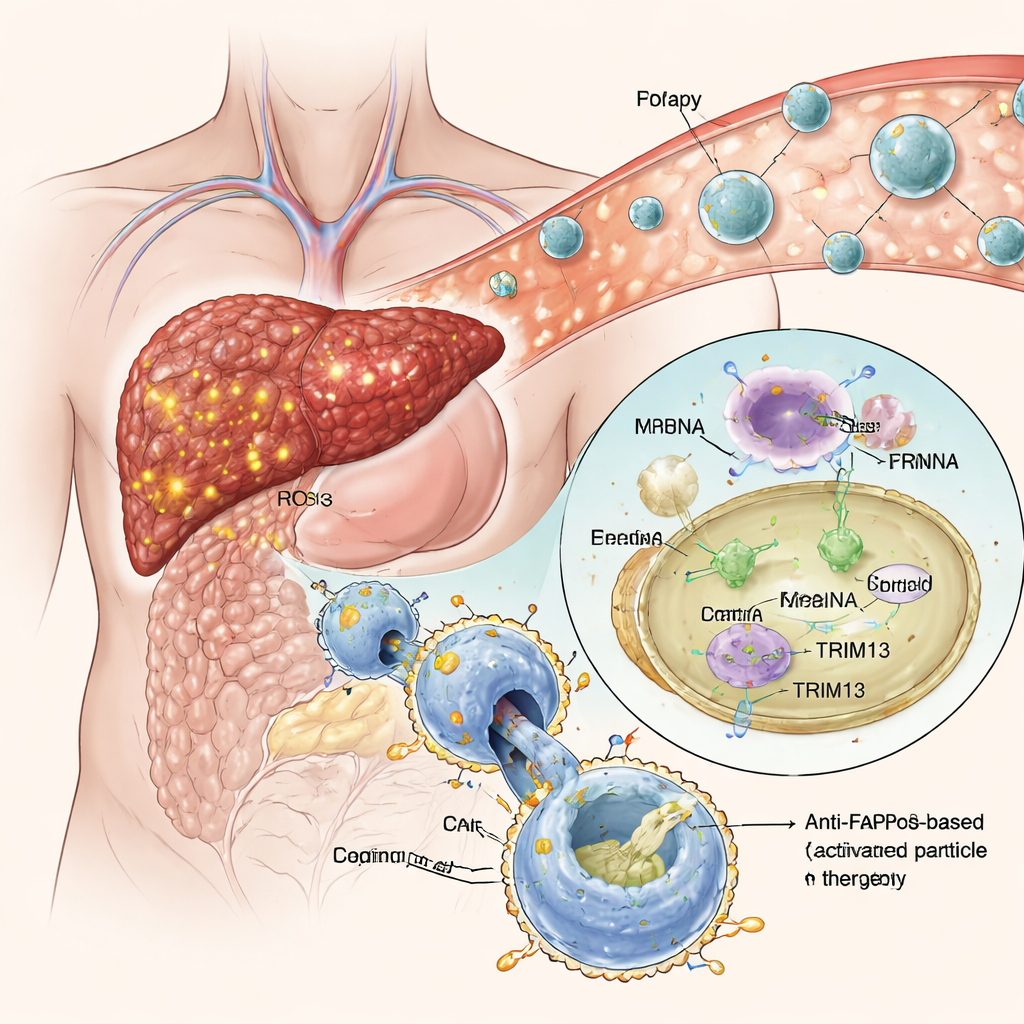
Nanopartículas inteligentes que se dirigen al tejido enfermo
En lugar de modificar macrófagos fuera del cuerpo, el equipo desarrolló nanopartículas lipídicas “activadas por efagocitosis” —pequeñas esferas grasas que transportan instrucciones genéticas como mensajeros ARN (ARNm). Estas partículas están recubiertas con una forma enmascarada de fosfatidilserina, una señal natural de “cómeme” que exhiben las células moribundas para atraer macrófagos. En el entorno altamente oxidativo del tejido hepático fibrótico, el camuflaje se elimina y la señal queda expuesta, incitando a los macrófagos cercanos a engullir las nanopartículas. Una vez dentro, el ARNm se libera y es traducido por la célula, conduciendo a la producción tanto de TRIM13 como del CAR anti‑FAP. En cultivos celulares, este enfoque impulsó con éxito a los macrófagos hacia un estado antiinflamatorio a la vez que les dio un apetito fuerte y selectivo por las células formadoras de cicatriz FAP‑positivas, sin perturbar su capacidad normal de limpiar otros desechos.
De hígados enfermos a regeneradores en ratones
El equipo probó después esta estrategia en modelos murinos de fibrosis hepática causada ya sea por un químico tóxico o por una dieta grasa deficiente en nutrientes. Las nanopartículas inyectadas sistémicamente llegaron eficientemente al hígado y, especialmente en animales fibróticos, fueron captadas principalmente por macrófagos. Allí, las células modificadas mostraron menor actividad de la vía STING y menor producción de moléculas inflamatorias, junto con una mayor eliminación de células estrelladas activadas. Los análisis tisulares revelaron descensos notables en colágeno y otros marcadores de cicatriz, una estructura de matriz extracelular más fina y normal, y pruebas sanguíneas de función hepática mejoradas. Los hígados de los ratones tratados mostraron más células proliferantes y recuperaron una arquitectura más saludable, lo que sugiere una reparación orgánica genuina y no solo un atenuamiento temporal de la inflamación.
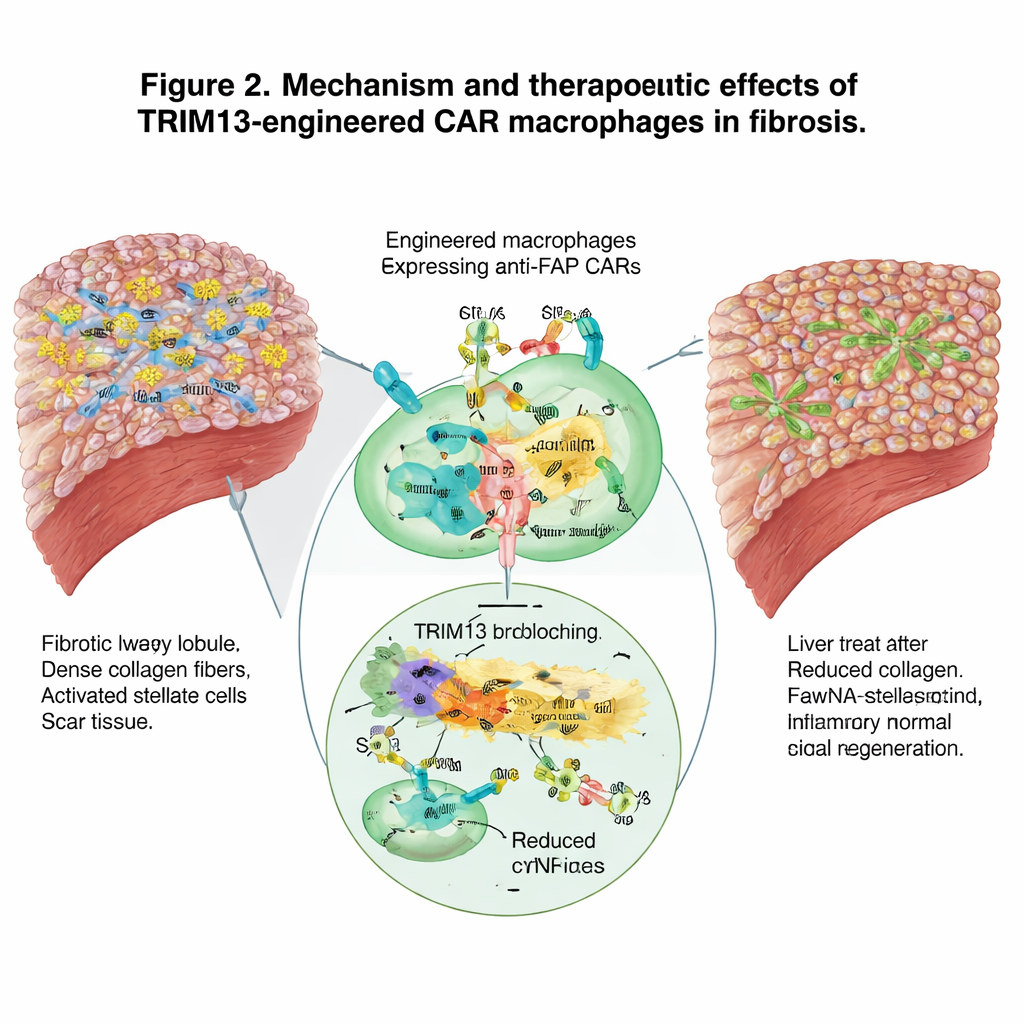
Movilizando al sistema inmunitario más amplio
Más allá de la eliminación directa de la cicatriz, los macrófagos reprogramados remodelaron el panorama inmunitario general. Pasaron de un perfil agresivo y promotor del daño a otro más resolutivo y reparador, y redujeron las señales inflamatorias en la sangre. Al mismo tiempo, al devorar las células formadoras de cicatriz, parecieron actuar como instructores para el sistema inmunitario adaptativo, atrayendo neutrófilos, células dendríticas y linfocitos T e incentivando una respuesta coordinada contra el tejido fibrótico. La secuenciación de ARN a nivel de célula única de las células inmunitarias hepáticas confirmó un desplazamiento lejos de programas génicos proinflamatorios y hacia una mayor capacidad para engullir y eliminar células y desechos dañinos.
Qué podría significar esto para los pacientes
Para un lector general, la conclusión es que este trabajo señala una forma de “reeducar” las propias células limpiadoras del hígado para que tanto desmantelen el tejido cicatricial como apagen las señales de alarma crónicas que perpetúan el daño. Al usar instrucciones de ARNm de corta duración empaquetadas en nanopartículas inteligentes, la terapia evita alterar las células de forma permanente y limita la actividad a las regiones enfermas, lo que podría reducir los efectos secundarios. Aunque se necesita mucha más investigación antes de poder probarse en humanos, esta estrategia dibuja un plan prometedor para tratar la fibrosis hepática —y potencialmente otras enfermedades fibróticas— convirtiendo al sistema inmunitario del propio cuerpo, de impulsor de la cicatrización, en un socio activo en la reparación.
Cita: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Palabras clave: fibrosis hepática, terapia con macrófagos, entrega de ARNm mediante nanopartículas, receptor de antígeno quimérico, vía TRIM13‑STING