Clear Sky Science · es
Radiomarcado de oligopeptidos mediante intercambio selectivo de isótopos de hidrógeno con deuterio y tritio en tampones acuosos
Rastreando medicamentos a nivel atómico
Los medicamentos modernos incluyen cada vez más moléculas biológicas complejas, como péptidos y pequeñas proteínas. Para entender a dónde van estos fármacos en el cuerpo y cuánto tiempo permanecen, los científicos a menudo sustituyen algunos átomos ordinarios por otros raros o radiactivos que pueden ser rastreados. Este artículo presenta una forma de “etiquetar” fármacos peptídicos con átomos trazadores directamente en soluciones acuosas, mucho más próxima a las condiciones biológicas reales que la mayoría de los métodos anteriores.
Por qué importan estos pequeños intercambios atómicos
Reemplazar el hidrógeno normal por formas más pesadas como el deuterio o el tritio convierte moléculas corrientes en potentes trazadores científicos. Estas versiones marcadas se comportan casi igual que el fármaco original, pero pueden seguirse con instrumentos sensibles que detectan masa o radiación. Para moléculas pequeñas, los químicos han desarrollado una amplia caja de herramientas para fabricar estos compuestos marcados. En cambio, los métodos para marcar biofármacos mayores y frágiles—como péptidos y proteínas—son escasos, a menudo complejos y poco adecuados para medios acuosos similares a la sangre o los fluidos celulares. Los autores se propusieron cerrar esta brecha: una forma simple y selectiva de insertar deuterio o tritio en bloques de construcción peptídicos directamente en tampones acuosos.
Una estrategia de marcado en un solo paso, en agua
El equipo se centró en un tipo de reacción llamada intercambio de isótopos de hidrógeno, en la que un átomo de hidrógeno de una molécula se sustituye por su homólogo más pesado procedente de un gas como deuterio (D2) o tritio (T2). Construyeron un catalizador in situ basado en iridio y una molécula auxiliar de fosfina especialmente seleccionada. Al mezclarse en un tampón ligeramente básico y calentarse, este sistema activa enlaces específicos carbono–hidrógeno en aminoácidos y pequeños péptidos y reemplaza esos hidrógenos por deuterio o tritio procedente del gas. De forma crucial, esto se realiza en un solo paso, en medios ricos en agua y con cantidades muy bajas de metal—condiciones más favorables para péptidos delicados y para flujos de trabajo prácticos en laboratorio. 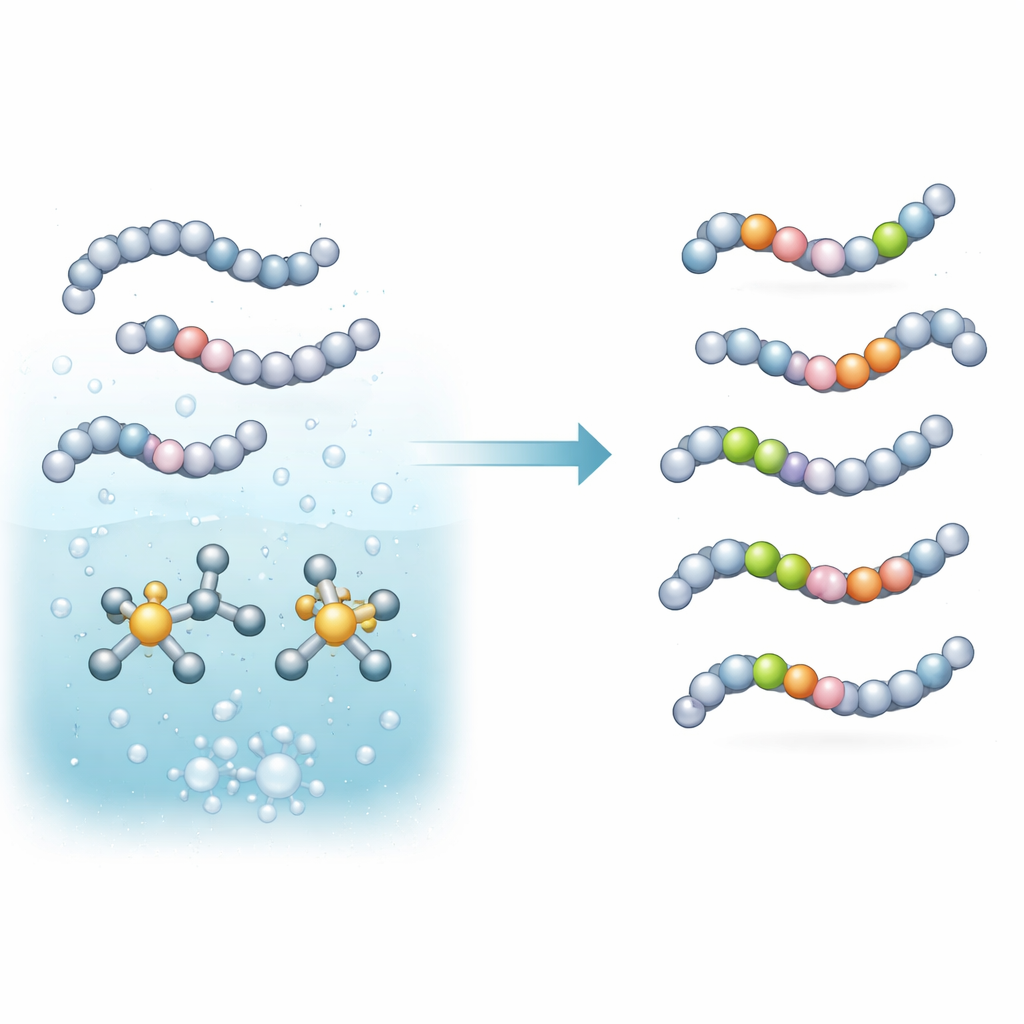
Elegir exactamente los sitios adecuados en los péptidos
No todos los átomos de hidrógeno en un péptido son igualmente útiles como etiquetas. Algunos se pierden fácilmente durante el metabolismo, lo que eliminaría la etiqueta radiactiva. Los autores exploraron cuidadosamente dónde prefiere actuar su catalizador. Descubrieron que aminoácidos no protegidos como la lisina y la arginina son particularmente adecuados. En la lisina, el método etiqueta selectivamente un carbono en la cadena lateral (la denominada posición gamma), un sitio considerado “no activado” y más propenso a permanecer estable en el organismo. La arginina muestra un comportamiento similar en posiciones cercanas de su cadena lateral. Al probar una serie de moléculas relacionadas, incluidas cadenas cortas con dos grupos amino, el equipo halló que tener dos sitios de nitrógeno posicionados de forma adecuada ayuda al catalizador metálico a sujetar la molécula y alcanzar el enlace carbono–hidrógeno objetivo.
Mirando bajo el capó del catalizador
Para entender por qué surge esta selectividad, los investigadores combinaron experimentos con detalladas simulaciones por ordenador usando teoría del funcional de la densidad. Estos cálculos describen el paisaje energético mientras el complejo de iridio se forma a partir de un precursor dimerizado, se une al agua, luego al aminoácido y, finalmente, inserta en un enlace carbono–hidrógeno específico. Los modelos muestran que romper el dímero original de iridio es energéticamente factible en agua para un tipo de precursor pero no para otro estrechamente relacionado, explicando por qué solo ciertos complejos iniciales son eficaces. También revelan que el propio sustrato ayuda a estabilizar el centro metálico activo y evitar que se aglomere en partículas inactivas. La vía más favorable implica que el aminoácido se una a través de dos átomos de nitrógeno, formando una sujeción tipo “pinza” que posiciona un único enlace carbono–hidrógeno para el intercambio con deuterio o tritio.
De bloques de construcción simples a fármacos peptídicos reales
Con el mecanismo comprendido, el equipo extendió el método desde aminoácidos individuales hasta péptidos cortos de hasta siete residuos y luego a secuencias terapéuticas más complejas de hasta 13 aminoácidos. En todos los casos, el marcado se produjo en las cadenas laterales de lisina o arginina en el extremo del péptido, y los péptidos permanecieron en gran medida intactos bajo las condiciones de reacción. Para el tritio, optimizaron la reacción a bajas presiones de gas para lograr de forma segura altas actividades específicas, lo que significa que una gran fracción de las moléculas porta al menos un átomo de tritio. Estos péptidos marcados con tritio se produjeron en un solo paso y están listos para usarse como trazadores en estudios in vitro y, potencialmente, in vivo. 
Qué implica esto para los medicamentos del futuro
Este trabajo demuestra que es posible unir selectivamente deuterio o tritio a fármacos peptídicos realistas en un paso simple y acuoso, dirigéndose a posiciones metabólicamente robustas en aminoácidos clave. Para desarrolladores de fármacos, eso significa un acceso más sencillo a versiones trazadoras marcadas con precisión de terapias peptídicas, vitales para medir absorción, distribución y metabolismo. Más allá de la producción de trazadores, las ideas mecanísticas sobre cómo el catalizador de iridio interactúa con los aminoácidos pueden inspirar nuevas formas de afinar dónde y cómo se modifican moléculas biológicas complejas, abriendo puertas a un control químico más preciso sobre futuros medicamentos biológicos.
Cita: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
Palabras clave: péptidos radiomarcados, intercambio de isótopos de hidrógeno, marcado con deuterio y tritio, terapéuticos peptídicos, catálisis con iridio