Clear Sky Science · es
ERCC6L2 garantiza la fidelidad de la reparación de rupturas de doble cadena del ADN con extremos escalonados
Por qué este descubrimiento importa para nuestro ADN
Cada célula de su cuerpo sufre constantemente daños en su ADN, especialmente el tipo más peligroso: rupturas que cortan ambas hebras de la doble hélice. Estas rupturas pueden provocar cáncer, trastornos hereditarios o fallos en la edición médica del genoma si no se reparan correctamente. Este estudio revela una proteína “guardiana” hasta ahora poco valorada, ERCC6L2, que protege de forma específica a un tipo complejo de ruptura frente a la conversión en grandes huecos y cromosomas desordenados. Entender a esta guardiana ayuda a explicar una rara enfermedad de la médula ósea humana y alerta sobre cómo ciertas herramientas de edición genética podrían tener efectos adversos en pacientes vulnerables.
Diferentes tipos de rupturas del ADN, distintos riesgos
No todas las rupturas del ADN son iguales. Algunos cortes son limpios, con ambas hebras rotas en el mismo punto, como cortar una cuerda de un tajo. Otros son escalonados, dejando extremos salientes cortos que no encajan perfectamente. Los editores genómicos modernos como Cas9 suelen crear cortes limpios y romos, mientras que herramientas como Cas12a, TALENs y algunos sistemas de nickasa emparejada generan rupturas escalonadas con extremos salientes. Los investigadores compararon de manera sistemática cómo las células humanas gestionan estos dos tipos de ruptura mediante la inhibición de miles de genes y luego preguntaron cuáles eran especialmente importantes para reparar cada tipo de corte.
Un guardián oculto para las rupturas escalonadas
De estas pantallas a escala genómica, ERCC6L2 surgió como un protector crucial para las rupturas escalonadas pero en gran medida prescindible para las romas. Las células que carecían de ERCC6L2 podían todavía reparar cortes romos de Cas9 con solo pequeñas inserciones o deleciones, las huellas típicas de la reparación rutinaria del ADN. En marcado contraste, cuando las rupturas escalonadas eran inducidas por Cas12a, TALENs o Cas9 de doble nickasa, las células deficientes en ERCC6L2 generaron muchas más deleciones grandes que alcanzaban miles de bases y redistribuciones cromosómicas ampliamente espaciadas llamadas translocaciones. Estos efectos se observaron no solo en líneas celulares manipuladas, sino también en células de médula ósea de pacientes portadores de mutaciones hereditarias en ERCC6L2, lo que subraya la relevancia clínica del hallazgo. 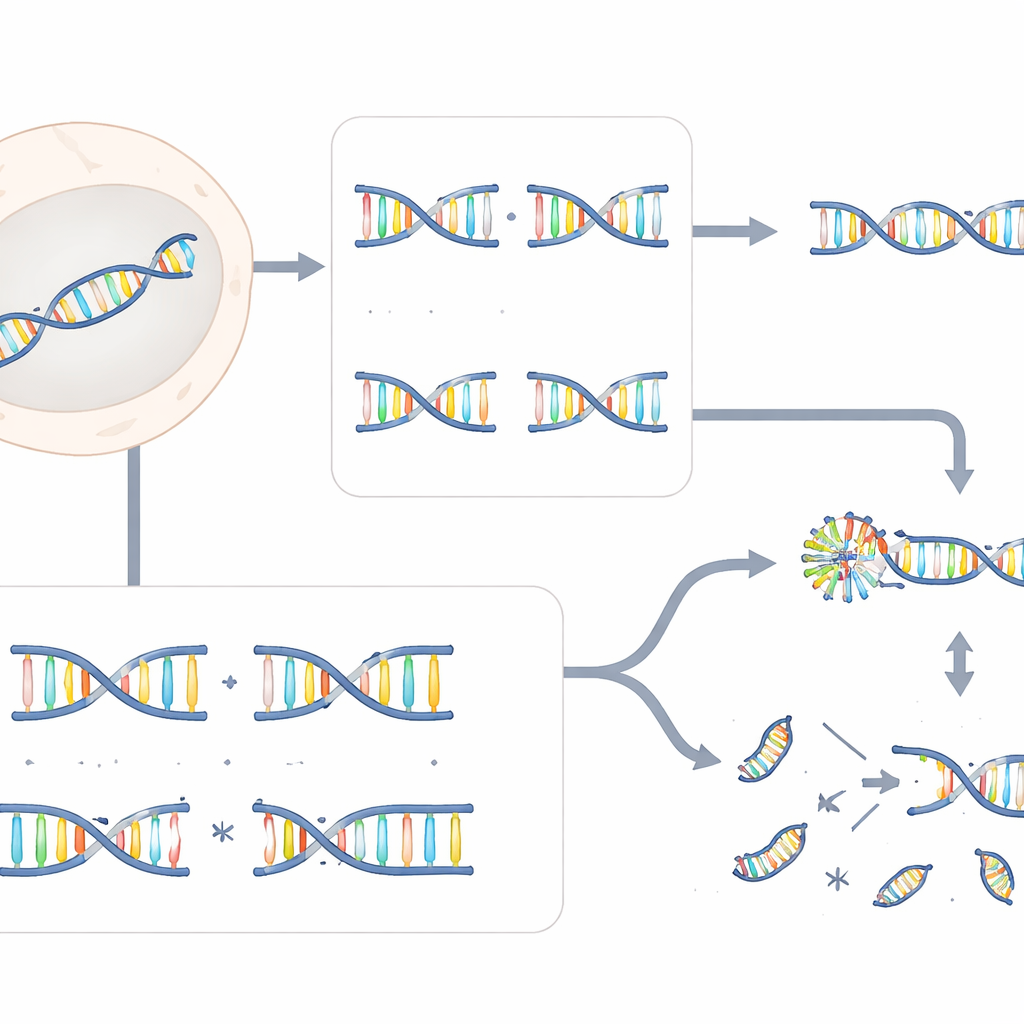
Cuando se acumulan muchos cortes, las células empiezan a fallar
El peligro de perder ERCC6L2 se volvió aún más evidente cuando el equipo indujo múltiples rupturas escalonadas en el genoma al mismo tiempo. En estos experimentos, las células sin ERCC6L2 tuvieron dificultades para sobrevivir y con frecuencia formaron micronúcleos—pequeños cuerpos con ADN desplazado que indican que los cromosomas se han fragmentado o segregado incorrectamente. La misma vulnerabilidad apareció cuando los investigadores recurrieron a una fuente natural de rupturas escalonadas: la enzima TOP2, que corta temporalmente el ADN para aliviar el torsión durante la actividad celular normal. Un fármaco quimioterápico, etopósido, atrapa a TOP2 en su estado roto, convirtiendo esas incisiones temporales en rupturas escalonadas duraderas. Las células sin ERCC6L2 fueron dramáticamente más sensibles al etopósido y mostraron una erosión excesiva de los extremos del ADN, reflejando lo observado con las rupturas inducidas por Cas12a.
Cómo ERCC6L2 controla la maquinaria de reparación
Para entender cómo funciona ERCC6L2 a nivel molecular, el equipo reconstituyó el proceso en un tubo de ensayo con proteínas purificadas y ADN. Hallaron que ERCC6L2 se une a muchas formas de ADN pero tiene un talento especial: puede “despegar” o desenrollar activamente los extremos salientes cortos en las rupturas escalonadas, y esto requiere su actividad motora consumidora de energía. En las células, ERCC6L2 contrarresta otra máquina de reparación, el complejo MRN, que normalmente recorta los extremos del ADN para generar tramos de cadena sencilla. Esta resecación es útil en algunas vías de reparación pero se vuelve peligrosa cuando se exagera, provocando deleciones extensas y rotura de cromosomas. En células deficientes en ERCC6L2, la resecación impulsada por MRN se descontrola en las rupturas escalonadas. Bloquear MRN o su regulador ATM revirtió la masticación excesiva del ADN y redujo la frecuencia de las deleciones grandes, demostrando que ERCC6L2 normalmente mantiene esta vía bajo control.
Qué significa esto para los pacientes y la edición del genoma
Poniendo juntas estas piezas, los autores proponen que ERCC6L2 actúa como un guardián especialista para las rupturas escalonadas del ADN. Al deshacer los salientes y promover una unión rápida y limpia, evita la pérdida prolongada de tramos de ADN y la unión indebida entre cromosomas distantes. En personas nacidas con mutaciones en ERCC6L2, las fuentes cotidianas de rupturas escalonadas—particularmente las creadas por TOP2—probablemente se acumulan sin reparar o se reparan mal, conduciendo a fallo de médula ósea, leucemia y posiblemente a ciertos problemas neurológicos. Para la terapia génica, el trabajo envía un mensaje claro: las herramientas de edición del genoma que crean deliberadamente cortes con salientes, como Cas12a, TALENs o algunos diseños de nickasa, podrían ser especialmente riesgosas en estos pacientes. Elegir estrategias de edición que eviten las rupturas escalonadas puede ser esencial para asegurar que arreglar un gen no desestabilice accidentalmente el resto del genoma. 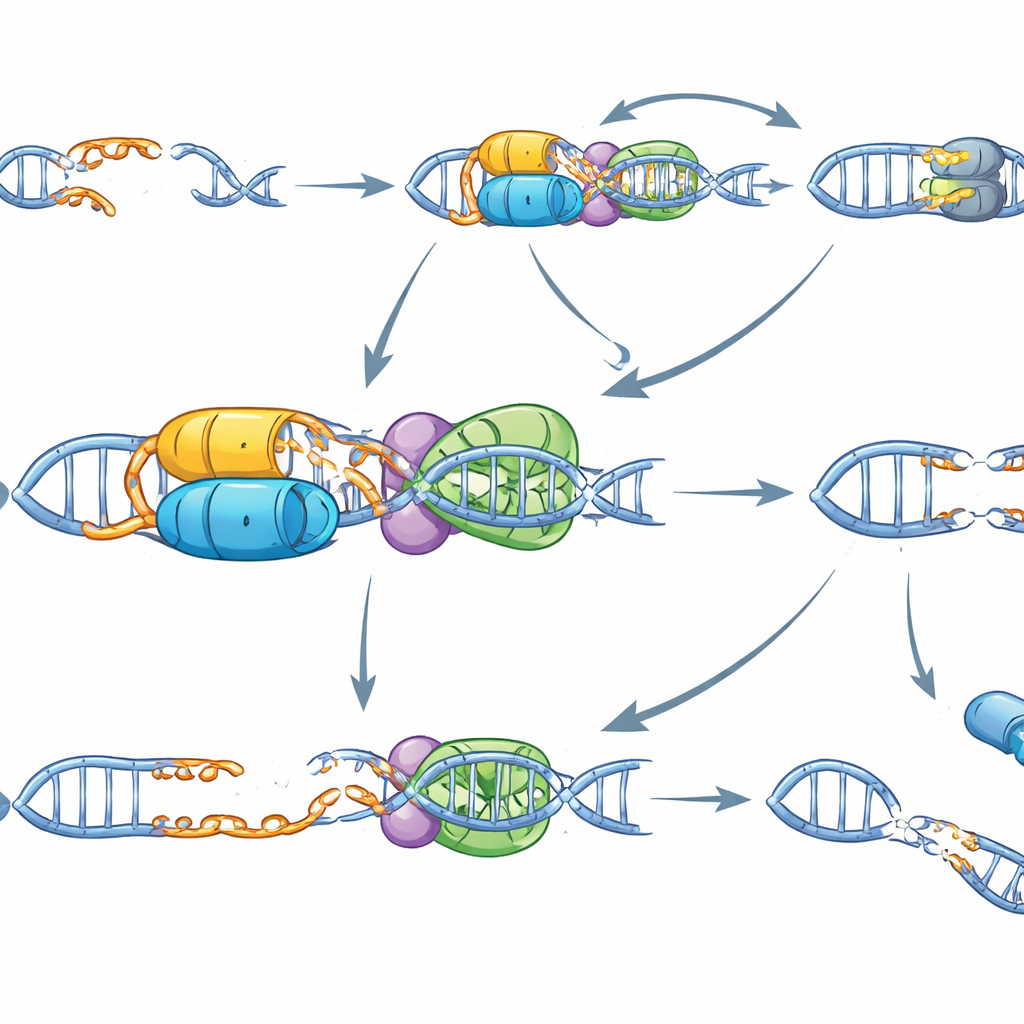
Cita: Aird, E.J., Serrano-Benitez, A., Siegner, S.M. et al. ERCC6L2 ensures repair fidelity for staggered-end DNA double-strand breaks. Nat Commun 17, 2743 (2026). https://doi.org/10.1038/s41467-026-69843-w
Palabras clave: Reparación del ADN, edición del genoma, rupturas de doble cadena, ERCC6L2, inestabilidad cromosómica