Clear Sky Science · es
Maximizar la utilización de energía y la eficiencia de lixiviación de litio mediante una doble oxidación electroquímica secuencial y un remojo-relajación
Por qué las baterías de coche viejas siguen importando
Las baterías de iones de litio alimentan nuestros teléfonos, portátiles y, cada vez más, nuestros coches. Pero a medida que millones de paquetes de vehículos eléctricos llegan al final de su vida útil, generan un nuevo tipo de residuo —y una nueva oportunidad. El litio y otros metales encerrados en baterías gastadas son valiosos pero costosos en energía de recuperar. Este estudio explora una manera más inteligente de extraer litio usando electricidad de forma más eficiente, reduciendo costes e impacto ambiental mientras se satisface el creciente apetito mundial por materiales para baterías.
Convertir baterías de desecho en un recurso
Hoy, la mayor parte del reciclaje industrial de baterías de iones de litio depende de químicos agresivos o hornos de alta temperatura. Estos métodos pueden recuperar metales, pero a menudo desperdician energía y dificultan la separación limpia del litio respecto al níquel, cobalto y manganeso en las llamadas baterías NCM. Los investigadores se centraron en una vía más nueva y limpia: usar una corriente eléctrica en agua salina para extraer litio del material de cátodo usado. Plantearon una pregunta simple pero crucial: ¿podemos reorganizar cuándo y cómo usamos la electricidad para que casi cada vatio ayude a quitar litio en lugar de perderse en reacciones secundarias?
Un baile en dos pasos: potencia y luego calma
El equipo diseñó un proceso en dos etapas que combina un “empuje” activo con un “remojo” tranquilo. En la primera etapa, llamada doble oxidación electroquímica, se aplica un voltaje constante a través de una celda que contiene un cátodo NCM gastado y una solución de cloruro de sodio. La corriente extrae iones litio del sólido hacia el líquido mientras también crea especies oxidantes potentes en la solución. Los científicos observaron que la mayor parte del trabajo útil ocurre en la primera hora: el litio abandona la estructura cristalina rápidamente al principio, pero más tarde gran parte de la energía se desperdicia en reacciones secundarias como la formación de burbujeo de oxígeno.
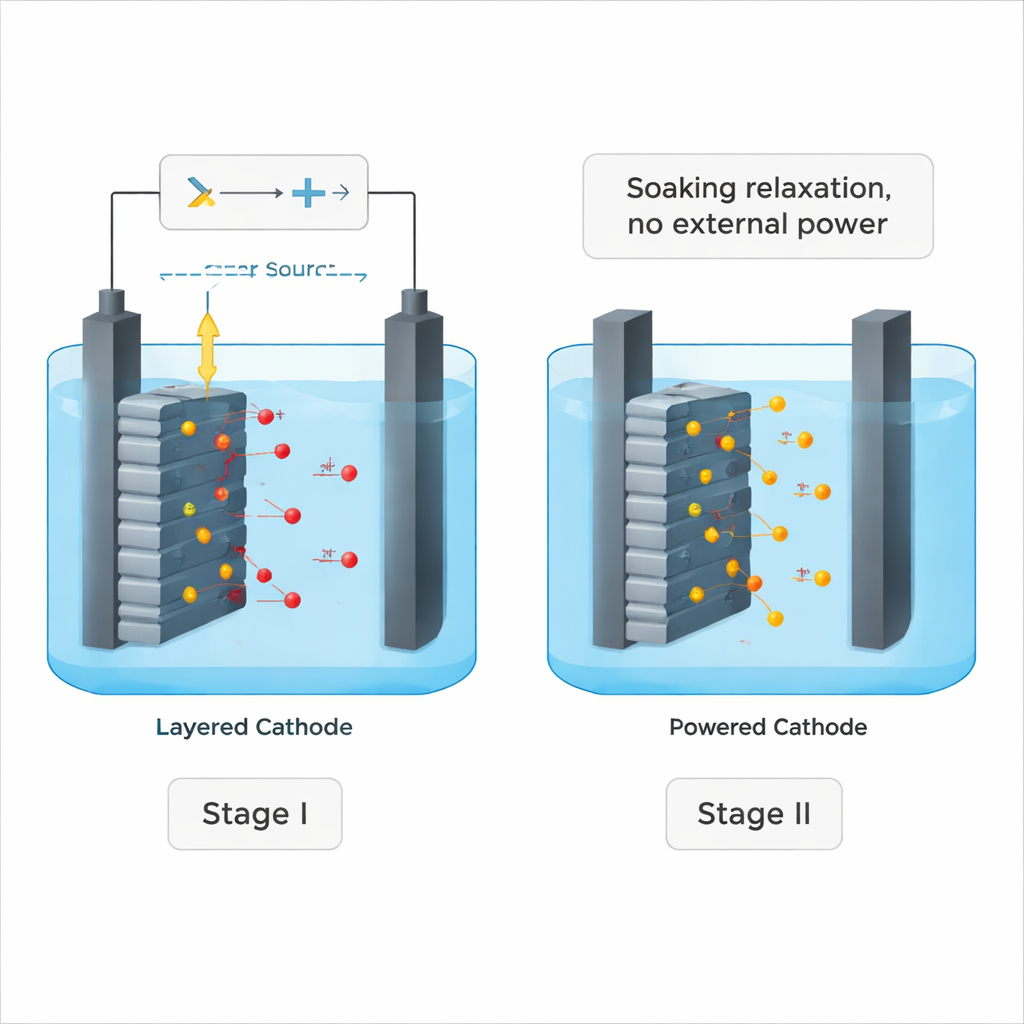
Dejar que la química termine el trabajo
En lugar de mantener la corriente durante más tiempo, los investigadores simplemente la apagaron y dejaron el electrodo en remojo en la solución salina ahora oxidante. Sorprendentemente, el litio continuó lixiviándose hasta que casi todo fue eliminado —alcanzando alrededor del 99 % de recuperación para material NCM fresco y aproximadamente el 98 % para cátodos realmente gastados. Medidas detalladas mostraron que los átomos de oxígeno dentro del cristal, temporalmente llevados a un estado más reactivo durante la etapa con corriente, se convirtieron en el impulsor oculto de esta segunda etapa tranquila. Estas especies de oxígeno “activadas” promovieron un intercambio lento: los iones de litio se difundieron hacia el líquido mientras iones de sodio (o potasio) de la solución se colaban en los huecos vacantes, todo sin aporte eléctrico adicional.
Cómo se reordena la estructura cristalina
Con microscopios electrónicos, difracción de rayos X y espectroscopía, el equipo observó cómo las partículas del cátodo se agrietaban, se adelgazaban y cambiaban su apilamiento interno a medida que el litio abandonaba la estructura. El material transitó por varias disposiciones en capas conocidas al pasar de rico en litio a pobre en litio, terminando en una forma rica en sodio que mantenía la estructura pero ya no contenía mucho litio. A lo largo de este proceso, los átomos de níquel y cobalto cambiaron sus estados de carga para mantener el equilibrio eléctrico global del material, mientras que el manganeso permaneció mayormente sin cambios, ayudando a estabilizar la red. Los investigadores también demostraron que los iones potasio, que desprenden más fácilmente sus moléculas de agua que el sodio, podían acelerar aún más el paso de intercambio iónico.
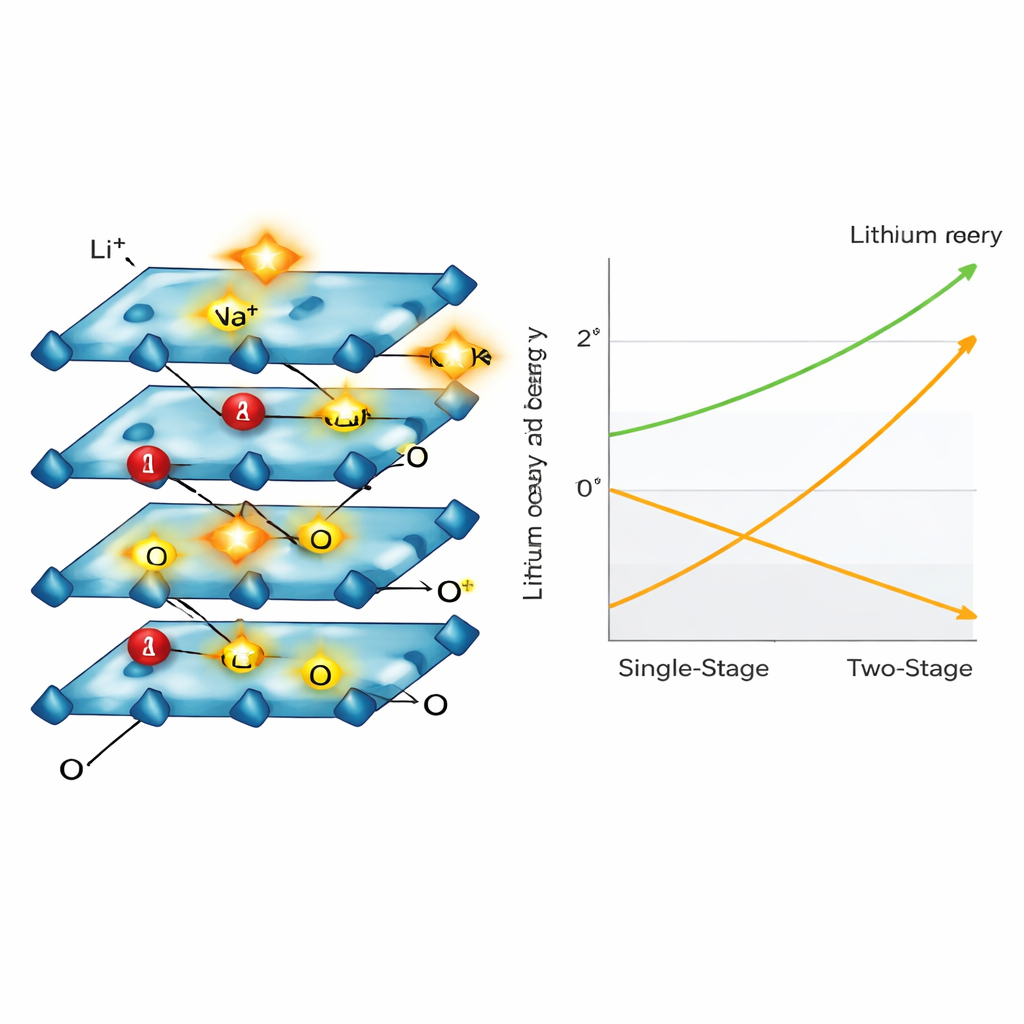
Del banco de laboratorio al suelo industrial
Para probar si esta idea podía funcionar fuera del laboratorio, el equipo construyó un sistema piloto capaz de tratar medio kilogramo de residuo de batería real por lote. Usando su método de dos etapas, recuperaron más del 98 % del litio como carbonato de litio de alta pureza, apto para fabricar nuevas baterías. De forma crucial, porque la corriente se corta una vez que la “química inteligente” se pone en marcha, el proceso consumió aproximadamente la mitad de la energía eléctrica que un método electroquímico estándar de una sola etapa, ahorrando más de una quinta parte del beneficio operativo total por tonelada de material de cátodo reciclado.
Qué significa esto para las baterías del futuro
En términos sencillos, el estudio muestra que no siempre es necesario seguir inyectando electricidad para recuperar materiales valiosos de baterías viejas. Un pulso de energía bien programado puede preparar el material y la solución para que el resto del trabajo ocurra por sí mismo, impulsado por fuerzas químicas internas. Si se adopta a escala, este enfoque en dos etapas podría hacer que el reciclaje de litio de baterías NCM gastadas sea más barato, más limpio y más atractivo para la industria, ayudando a cerrar el ciclo de vida de las baterías y aliviando la presión sobre la minería de litio nueva.
Cita: Zhong, W., Gu, X., Feng, X. et al. Maximizing energy utilization and lithium leaching efficiency via sequential electrochemical dual-oxidation and soaking-relaxation. Nat Commun 17, 2050 (2026). https://doi.org/10.1038/s41467-026-69834-x
Palabras clave: reciclaje de litio, residuos de baterías, lixiviación eficiente energéticamente, cátodos NCM, recuperación electroquímica