Clear Sky Science · es
Supervivencia de las cianobacterias y mitigación de los efectos tóxicos del Fe(II) en un océano arcaico rico en sílice
Mares antiguos y el aire que respiramos
Miles de millones de años antes de que existieran animales o plantas, diminutos microbios fotosintéticos llamados cianobacterias comenzaron a liberar oxígeno en los océanos de la Tierra. Sin embargo, pasaron cientos de millones de años antes de que el oxígeno se acumulase en la atmósfera. Este estudio plantea por qué se produjo ese retraso tan prolongado y si la química de los mares primitivos —ricos en hierro disuelto y sílice— ayudó o dificultó a esos microbios que, al final, hicieron habitable nuestro planeta.

Océanos ricos en hierro y un efecto secundario tóxico
Los océanos primitivos contenían grandes cantidades de hierro disuelto, especialmente en las regiones costeras donde aguas profundas afloraban hacia la superficie. Cuando ese hierro se encontró con el oxígeno liberado por las cianobacterias, se oxidó, formando minerales de hierro que más tarde dieron lugar a las formaciones de hierro bandeadas —rocas rayadas que son algunos de nuestros archivos geológicos más antiguos. Pero las mismas reacciones también pueden generar “especies reactivas de oxígeno”, formas altamente agresivas de oxígeno que pueden dañar el ADN, las proteínas y las membranas celulares. Trabajos previos sugirieron que esta reacción química impulsada por el hierro podría haber envenenado a las cianobacterias, frenando su expansión y retrasando el aumento de oxígeno en la atmósfera.
La sílice como guardián inesperado
Los autores se centraron en otro ingrediente abundante del agua de mar primitiva: la sílice disuelta, el mismo material básico que se encuentra en el vidrio. La evidencia geológica sugiere que los océanos antiguos contenían concentraciones de sílice muy superiores a las actuales. En experimentos de laboratorio, hicieron crecer una cianobacteria marina (Synechococcus sp. PCC 7002) bajo condiciones controladas con distintas cantidades de hierro y sílice disueltos. Registraron la velocidad de crecimiento celular, la cantidad de oxígeno producida, la rapidez de oxidación del hierro y la cantidad de oxígeno reactivo formado. A bajos niveles de hierro, las células prosperaron independientemente de la sílice. Pero cuando el hierro fue muy alto —similar a las condiciones esperadas en algunas aguas costeras del Arcaico—, las culturas sin sílice añadida flaquearon, mientras que las que contenían alta sílice permanecieron activas, produjeron más oxígeno y alcanzaron mayor número de células.
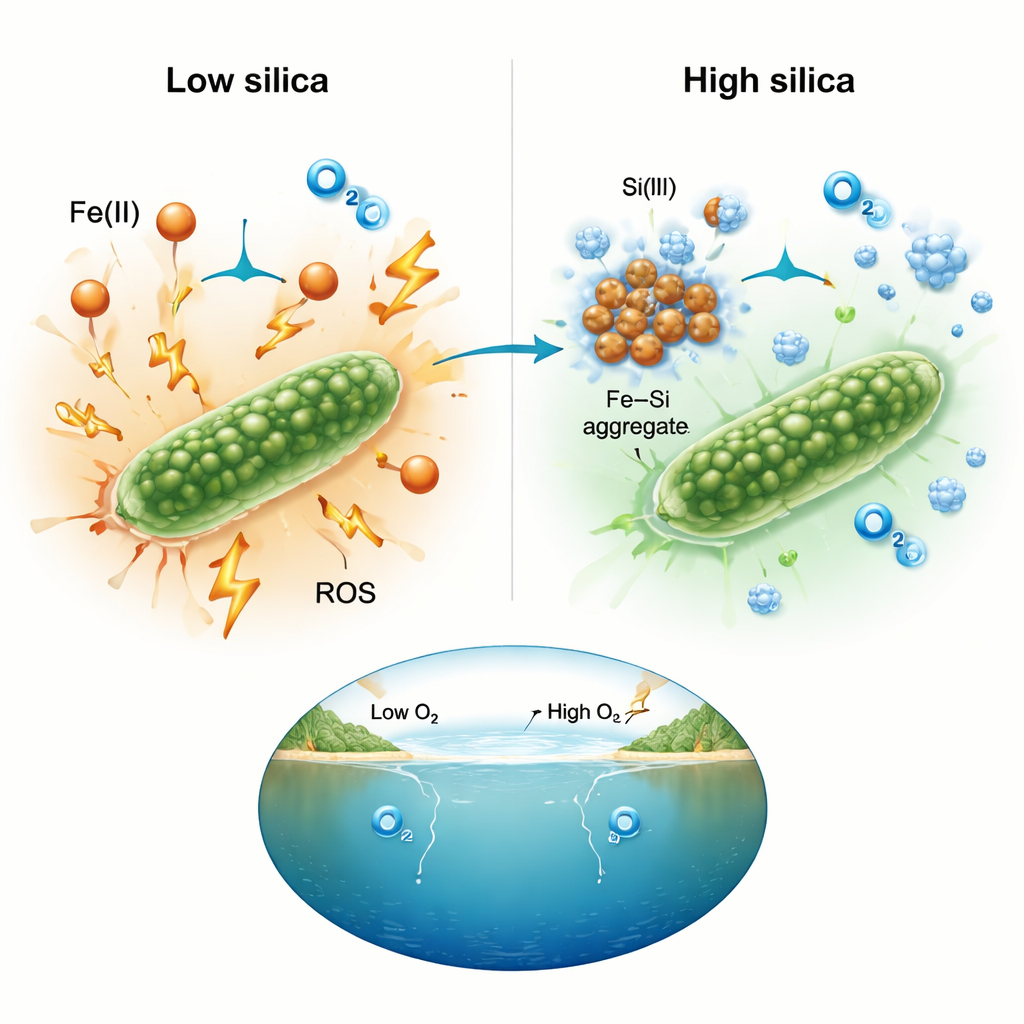
Trabajo químico conjunto que doma reacciones dañinas
Para entender por qué la sílice marcó la diferencia, el equipo midió las especies reactivas de oxígeno directamente usando tintes fluorescentes. A niveles elevados de hierro, las culturas sin sílice mostraron señales intensas de oxígeno reactivo, coherentes con una química estresante alrededor de las células. En los montajes ricos en sílice, esas señales se mantuvieron próximas al nivel de fondo incluso cuando las concentraciones de hierro eran extremas. Los investigadores interpretan esto como la unión de la sílice al hierro disuelto y la formación de agregados hierro–sílice. Una vez atrapado en esos racimos, el hierro queda menos disponible para alimentar las reacciones en cadena que generan oxidantes dañinos. El efecto neto es suavizar el entorno químico para que las cianobacterias puedan seguir fotosintetizando en lugar de quedar paralizadas por el estrés oxidativo.
Ritmos día–noche e impactos a escala oceánica
Los experimentos también se llevaron a cabo bajo ciclos de luz día–noche realistas en lugar de una iluminación constante. Bajo estas condiciones alternantes, las cianobacterias oxidaron el hierro más rápido y toleraron mejor las aguas con alto contenido de hierro, lo que sugiere que los periodos nocturnos de “reposo” reducen el estrés a largo plazo. Usando las tasas de producción de oxígeno medidas en el laboratorio, los autores construyeron un modelo numérico simple de una columna de agua del océano primitivo. Para abundancias plausibles de cianobacterias y tasas realistas de afloramiento de aguas profundas, hallaron que las aguas superficiales podían volverse ricas en oxígeno mientras las capas más profundas permanecían cargadas de hierro. En muchos escenarios, las concentraciones de oxígeno en la zona iluminada alcanzaron o superaron los niveles de saturación del agua de mar modernos, lo que implica que «oasis» locales de oxígeno sobre profundidades ricas en hierro podrían haber sido comunes.
Replantear por qué el oxígeno tardó tanto
Tomados en conjunto, los resultados sostienen que las especies reactivas de oxígeno formadas a partir del hierro y el oxígeno probablemente no fueron un obstáculo insalvable para las cianobacterias tempranas, siempre que la sílice fuera abundante y prevalecieran los ciclos naturales día–noche. En lugar de estar crónicamente envenenados, estos microbios probablemente encontraron muchos entornos costeros donde la sílice amortiguó los efectos nocivos del hierro, permitiéndoles crecer, oxidar enormes cantidades de hierro y liberar oxígeno excedente a la atmósfera. El misterio persistente de por qué la atmósfera terrestre se oxigenó tan tarde debe buscarse, por tanto, más en factores de gran escala —como la rapidez con la que el oxígeno fue consumido por gases volcánicos y rocas— que en la química local alrededor de células microbianas individuales.
Cita: Dreher, C.L., Cirpka, O.A., Schad, M. et al. Survival of cyanobacteria and mitigation of Fe(II) toxicity effects in a silica-rich Archean ocean. Nat Commun 17, 1987 (2026). https://doi.org/10.1038/s41467-026-69826-x
Palabras clave: oxígeno en la Tierra primitiva, cianobacterias, formaciones de hierro bandeadas, especies reactivas de oxígeno, océanos ricos en sílice