Clear Sky Science · es
Aprovechar un biorreactor intestinal en ratones libres de gérmenes para la evolución dirigida de probióticos contra la enfermedad hepática grasa no alcohólica
Por qué esta historia intestinal importa para tu hígado
La enfermedad hepática grasa no alcohólica (EHGNA) ya afecta a cientos de millones de personas y está estrechamente ligada a la dieta y a la salud intestinal. Este estudio explora una idea inusual: usar el propio intestino como una especie de fábrica viva para “entrenar” bacterias beneficiosas y convertirlas en mejores fármacos. Al dejar que probióticos evolucionaran dentro de ratones libres de gérmenes sometidos a una dieta alta en grasas, los investigadores moldearon una cepa bacteriana que gestiona con mayor eficacia los ácidos biliares —moléculas con efecto detergente que conectan lo que comemos con cómo el hígado almacena grasa. El trabajo sugiere una nueva vía para diseñar probióticos de próxima generación que estén naturalmente ajustados a nuestro cuerpo en lugar de solo modificados en tubos de ensayo.
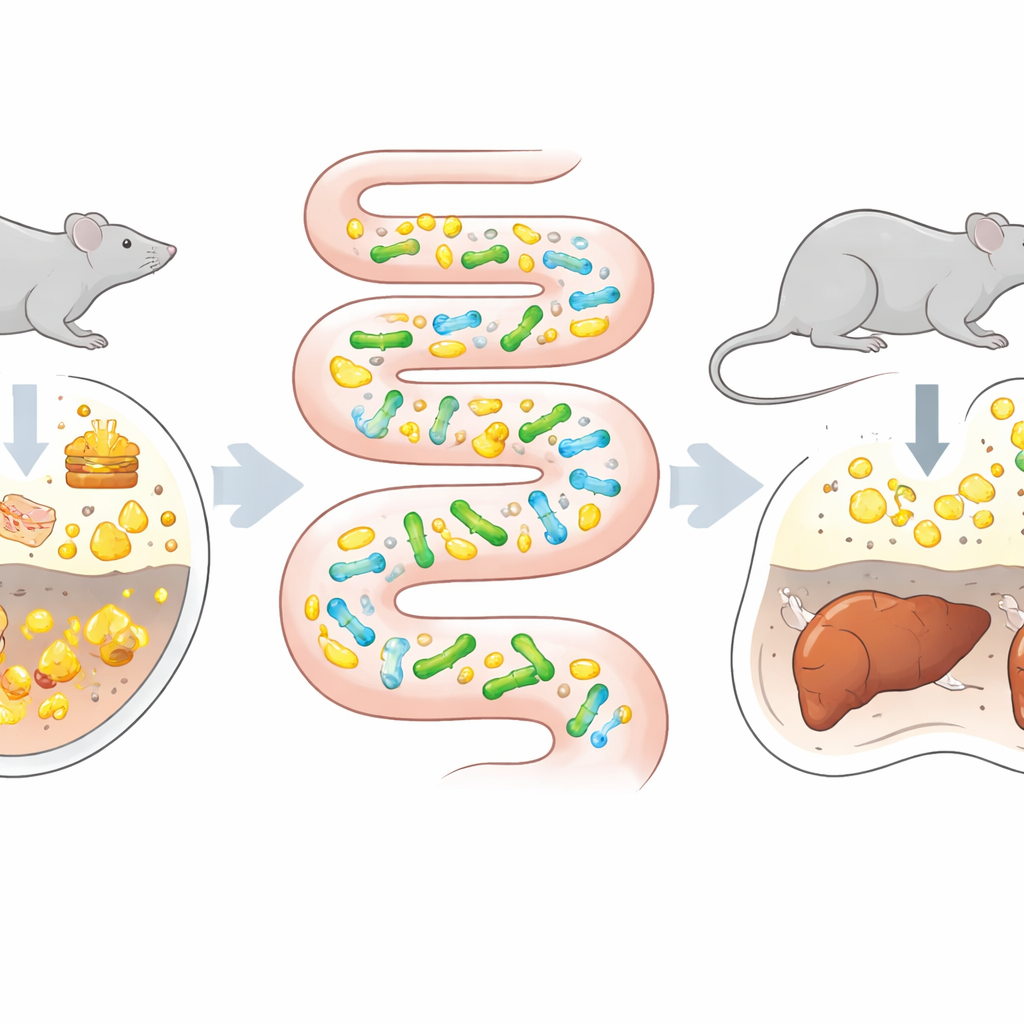
Convertir el intestino en una cámara de evolución
La evolución dirigida tradicional —mutar microbios y seleccionar a los mejores— suele realizarse en matraces de laboratorio. Eso funciona bien para enzimas o microbios industriales, pero a menudo fracasa para probióticos, que deben navegar la compleja química, las señales inmunitarias y las fuerzas físicas del intestino. Los autores se preguntaron: ¿y si el propio intestino, con todas sus presiones naturales, se usara como ambiente selectivo? Eligieron una especie probiótica, Bifidobacterium animalis subsp. lactis, que ya tiene cierta capacidad para descomponer ácidos biliares. Ratones libres de gérmenes, que no portan otros microbios, fueron colonizados con esta cepa y luego alimentados con una dieta escalonada cada vez más alta en grasas y colesterol, conocida por aumentar los niveles de ácidos biliares en el intestino. En paralelo, la misma cepa fue forzada a adaptarse en medio de laboratorio estándar que contenía ácidos biliares, lo que permitió una comparación directa de evolución in vitro frente a in vivo.
Un probiótico entrenado en el intestino supera a su primo entrenado en el laboratorio
Tras pases repetidos en matraces, las bacterias evolucionadas en el laboratorio no mostraron una mejora significativa en la actividad de procesamiento de ácidos biliares. En marcado contraste, los aislados tomados de los intestinos de los ratones alimentados con dieta alta en grasas mostraron una amplia variación en el rendimiento; aproximadamente una cuarta parte tenía una capacidad claramente mayor para romper ácidos biliares. La variante destacada, llamada W5S9, metabolizó ácidos biliares un 77 % mejor que la cepa parental. Esta diversidad, y la presencia tanto de ganadores como de perdedores, subrayó cómo el entorno intestinal del huésped aplica presiones ricas y multifacéticas que los medios simples de laboratorio no pueden imitar. También confirmó que el intestino puede actuar como un poderoso “biorreactor”, generando y probando continuamente variantes genéticas en condiciones que se parecen mucho a la vida real.
Acercándose a las mutaciones que importan
Para entender qué cambió en W5S9, el equipo secuenció su genoma y midió qué genes estaban más o menos activos en comparación con la cepa original. Entre cientos de pequeñas diferencias en el ADN, dos destacaron. Una se ubicaba justo corriente arriba de un gen llamado cbh, que produce una enzima que corta sales biliares; este cambio actuó como un interruptor más fuerte, aumentando la producción de la enzima bajo estrés por bilis. La segunda mutación alteró la estructura y la actividad de una proteína transportadora (MDR) que expulsa al exterior los ácidos biliares procesados. Pruebas de laboratorio mostraron que estos ajustes hicieron que el probiótico fuera mejor tanto en cortar ácidos biliares conjugados como en exportar los productos resultantes, mejorando su supervivencia en condiciones adversas ricas en bilis. En otras palabras, la evolución dentro del intestino afinó tanto las “tijeras” como la “puerta de salida” de la vía de los ácidos biliares.
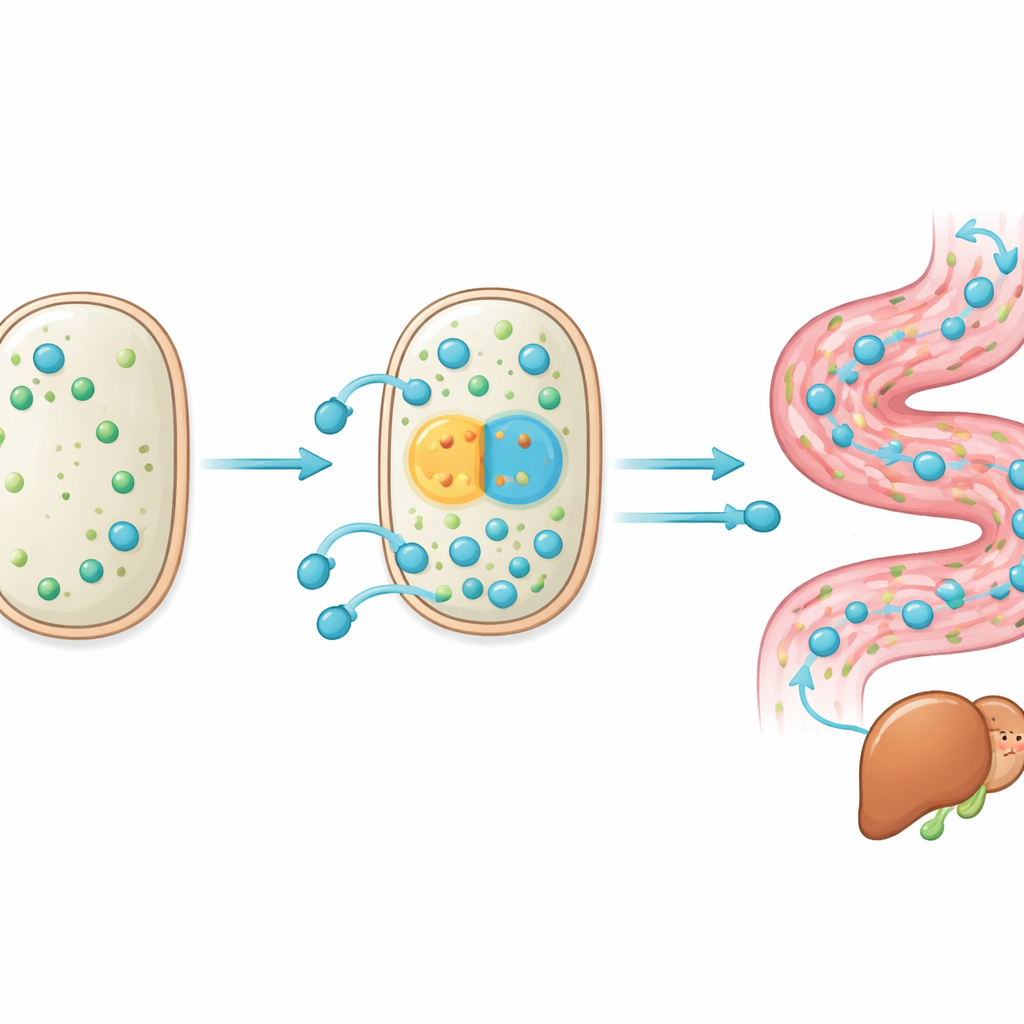
Protegiendo hígados grasos en un organismo estresado por la dieta
La prueba crucial fue si esta cepa entrenada en el intestino podía realmente proteger a un animal del daño hepático. Los investigadores usaron un modelo murino de EHGNA, en el que una dieta alta en grasas a largo plazo provoca aumento de peso, acumulación de grasa en el hígado e inflamación. Los ratones se dividieron en cuatro grupos: dieta normal, dieta alta en grasas sola, dieta alta en grasas más el probiótico original, y dieta alta en grasas más la cepa adaptada W5S9. Ambos grupos con probióticos mostraron mejoras respecto al grupo de dieta alta en grasas, pero W5S9 fue consistentemente mejor. Estos ratones ganaron menos peso, tuvieron perfiles de colesterol más saludables, mostraron marcadores más bajos de lesión e inflamación hepática y presentaron visiblemente menos gotas de grasa en el tejido hepático. Un análisis químico detallado de las heces reveló que W5S9 redujo con mayor fuerza los ácidos biliares asociados a la enfermedad y empujó el conjunto de ácidos biliares hacia un equilibrio más saludable, sin remodelar de forma dramática la comunidad intestinal global.
Qué significa esto para futuros medicamentos probióticos
Para los no especialistas, el mensaje clave es que los investigadores no limitaron a encontrar un probiótico “bueno”: usaron el propio cuerpo para esculpir uno mejor. Al permitir que la selección natural operara dentro de ratones libres de gérmenes bajo un ambiente cuidadosamente diseñado de alta grasa y alta bilis, produjeron una cepa que maneja con mayor eficiencia los ácidos biliares y, como resultado, protege mejor al hígado del daño inducido por la dieta. Dado que no se añadió ADN foráneo, estos microbios evolucionados permanecen no transgénicos, lo que puede facilitar la aceptación regulatoria y pública. La implicación más amplia es que estrategias similares de evolución guiada por el huésped podrían adaptarse a otras condiciones, desde la enfermedad inflamatoria intestinal hasta trastornos metabólicos e incluso neurológicos, abriendo la puerta a terapias microbianas vivas personalizadas y funcionalmente afinadas.
Cita: Han, Z., Sun, Z., Liu, X. et al. Harnessing a germ‑free mouse gut bioreactor for directed evolution of probiotics to combat non-alcoholic fatty liver disease. Nat Commun 17, 3133 (2026). https://doi.org/10.1038/s41467-026-69823-0
Palabras clave: probióticos, microbioma intestinal, ácidos biliares, enfermedad hepática grasa, evolución dirigida