Clear Sky Science · es
La colecistoquinina derivada de las células beta impulsa el desarrollo de adenocarcinoma pancreático asociado a la obesidad
Cuando el exceso de peso habla con el páncreas
Se sabe que la obesidad aumenta el riesgo de cáncer de páncreas, uno de los más letales, pero la “conversación” biológica que vincula la grasa corporal adicional con los tumores ha sido confusa. Este estudio descubre un mensajero inesperado: una hormona digestiva llamada colecistoquinina, o CCK, que se produce dentro de las células productoras de insulina del páncreas. Al rastrear cómo cambian estas células bajo estrés metabólico, los autores muestran cómo una hormona que de por sí ayuda al organismo puede, en su lugar, alimentar el cáncer, y sugieren nuevas formas de interceptar la enfermedad antes de que se establezca.
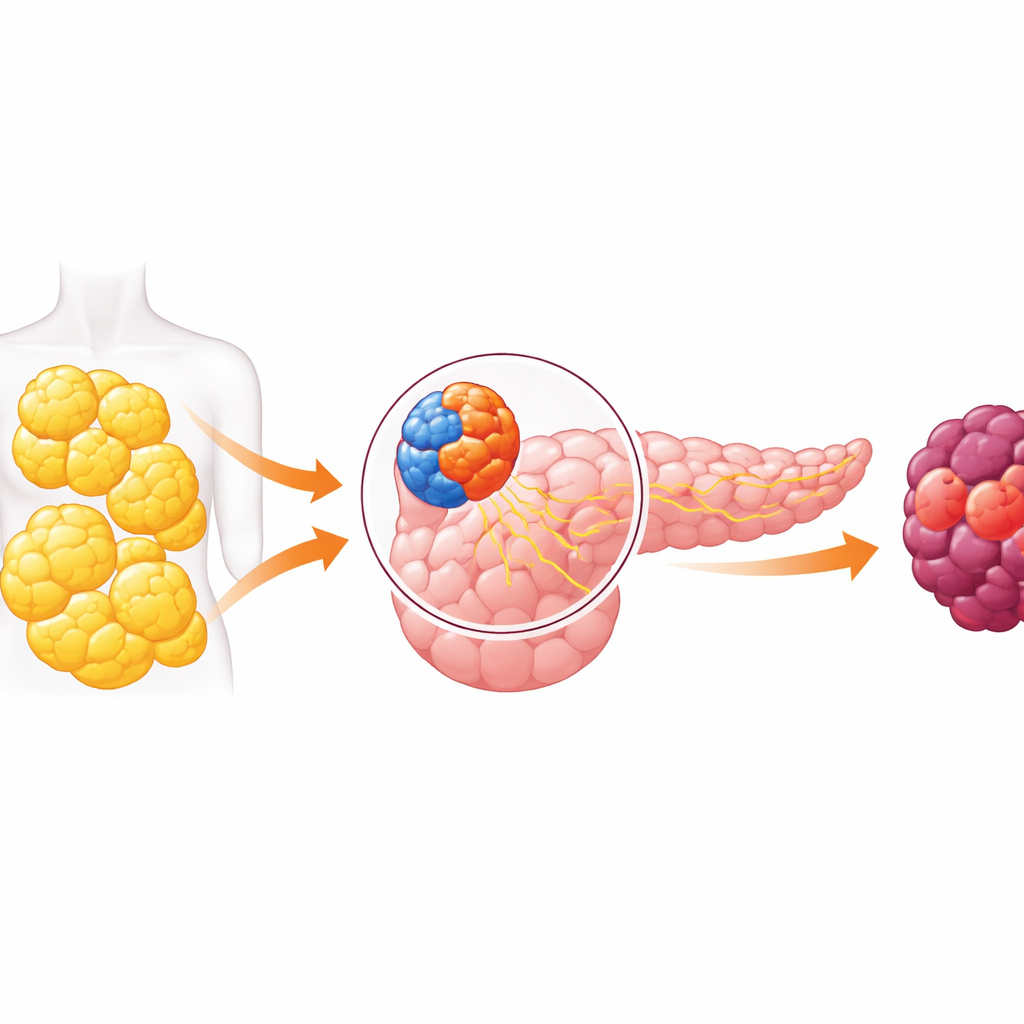
Un órgano con dos caras y un diálogo peligroso
El páncreas tiene dos funciones principales. Una parte, la endocrina, contiene pequeñas islas de células que liberan hormonas como la insulina para controlar el azúcar en sangre. La otra, la exocrina, produce jugos digestivos e incluye las células que con más frecuencia dan origen al cáncer pancreático. Durante años, los investigadores supusieron que estos compartimentos operaban en gran medida de forma aislada. Trabajos recientes han derribado esa idea, mostrando que señales de las células productoras de hormonas pueden influir en las células digestivas cercanas. Este artículo profundiza en ese diálogo y encuentra que, en la obesidad, puede empujar al lado exocrino del páncreas hacia el cáncer.
El estrés en las células hormonales enciende una nueva señal
En la obesidad, las células beta productoras de insulina están bajo presión constante para satisfacer la demanda creciente de insulina del organismo. Utilizando secuenciación de ARN a nivel de célula única y herramientas computacionales avanzadas, los investigadores siguieron a células beta individuales mientras los ratones pasaban de delgados a con sobrepeso y a obesos severos. Hallaron que un subconjunto de células beta inmaduras se expandió y gradualmente perdió su identidad especializada de insulina. A medida que estas células se estresaban, aumentaron los marcadores de tensión en el plegamiento de proteínas y de daño celular, mientras que la producción de insulina disminuía. Al mismo tiempo, estas células comenzaron a producir niveles altos de CCK, una hormona habitualmente asociada al intestino que puede estimular a las células digestivas a crecer y cambiar.
De hormona útil a combustible para el cáncer
Para comprobar si esta CCK recién producida era simplemente un subproducto del estrés o un impulsor activo de la enfermedad, el equipo diseñó ratones cuyas células beta producían CCK extra, incluso sin obesidad. Estos animales desarrollaron lesiones precancerosas pancreáticas y tumores invasivos en grado similar al de ratones obesos, a pesar de tener peso y glucemia normales. En contraste, cuando se eliminó la CCK específicamente del páncreas de ratones obesos, la carga tumoral cayó drásticamente, aunque los animales seguían siendo corpulentos y presentaban niveles altos de insulina. En múltiples modelos de ratón, los niveles de CCK en el páncreas se correlacionaron estrechamente con la cantidad de tumor, mientras que los niveles de insulina tendían a moverse en la dirección opuesta. Esto apuntó a la CCK—no a la insulina—como la hormona dominante que vincula la obesidad con el cáncer de páncreas en estos sistemas.
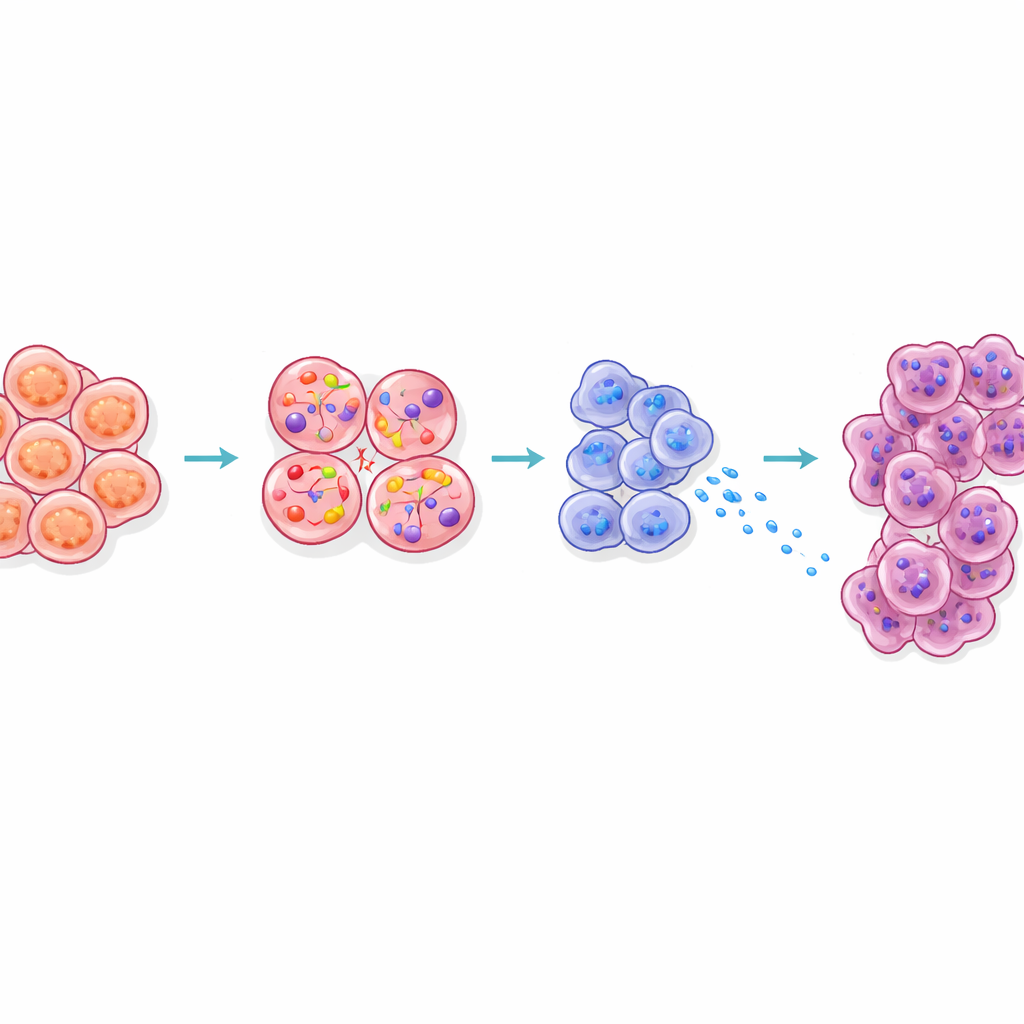
Cómo la señal alcanza y prepara a las células vecinas
El estudio también examinó cómo la CCK procedente de las células beta remodela el tejido circundante. Las células acinares, que normalmente secretan enzimas digestivas, están justo junto a los islotes en el páncreas. En ratones obesos, las células acinares cercanas a los islotes mostraron una firma de estrés, produjeron más enzimas digestivas y proteínas llamadas Reg, y cambiaron a estados conocidos por ser más fácilmente transformables en cáncer. Bloquear la señalización de CCK en ratones obesos redujo estas señales Reg. La imagen tridimensional además reveló que las lesiones precancerosas tempranas tendían a aparecer inusualmente cerca de los islotes en animales obesos. En conjunto, estos resultados sugieren que la difusión de CCK desde células beta estresadas crea una “zona caliente” alrededor de los islotes donde las células digestivas están preparadas para volverse tumorales.
Patrones compartidos con la diabetes humana y un interruptor clave
Al comparar los datos de ratón con tejido pancreático humano de personas con y sin diabetes tipo 2, los autores encontraron paralelismos notables: las células beta de donantes diabéticos se correspondían con los mismos estados estresados y menos maduros observados en ratones obesos. Luego utilizaron un análisis regulatorio para preguntar qué activa la CCK en las células beta e identificaron una vía sensible al estrés centrada en la proteína cJun. Cuando bloquearon la vía JNK–cJun aguas arriba en ratones obesos o en células tipo beta en cultivo, los niveles de CCK disminuyeron, y se observó a cJun uniéndose cerca de una región reguladora del gen CCK. Esto sugiere que el estrés crónico activa JNK–cJun, que a su vez transforma a las células beta en un modo productor de CCK.
Qué significa esto para las personas en riesgo
Para un lector no especializado, el mensaje central es que, bajo la carga de la obesidad y la diabetes, las células productoras de insulina en el páncreas no solo fallan: se adaptan de una manera que inadvertidamente fomenta que las células vecinas formen cáncer. Lo hacen activando la CCK, una hormona que actúa como señal de crecimiento y estrés para las células digestivas próximas, contribuyendo a crear un terreno fértil para los tumores. Dado que la CCK pancreática no es esencial para mantener el control de la glucosa, dirigir esta fuente hormonal específica o su interruptor activado por el estrés podría, en principio, reducir el riesgo de cáncer de páncreas en personas con obesidad o diabetes tipo 2 sin perjudicar el equilibrio hormonal general. El trabajo replantea el cáncer pancreático como una enfermedad de comunicación desorientada entre las dos caras del órgano y destaca nuevas vías para la prevención temprana.
Cita: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Palabras clave: cáncer de páncreas, obesidad, células beta, colecistoquinina, diabetes tipo 2