Clear Sky Science · es
La formación del dominio PIN compuesto SMG5-SMG6 es esencial para la NMD
Cómo se protegen las células de mensajes defectuosos
Nuestras células leen constantemente los mensajes genéticos (ARNm) para fabricar proteínas. Pero esos mensajes a veces contienen señales de parada temprana que producirían proteínas truncadas y potencialmente dañinas. El proceso que destruye tales mensajes defectuosos se llama degradación de ARNm mediada por codón de parada prematuro (NMD). Este artículo revela cómo dos proteínas clave, SMG5 y SMG6, cooperan físicamente para cortar mensajes defectuosos, explicando un misterio de larga data sobre cómo funciona el control de calidad celular.
Encontrando la asociación oculta
Durante años, los científicos supieron que SMG6 puede cortar ARN de forma directa, mientras que se pensaba que SMG5 estaba «inactivo catalíticamente» y actuaba principalmente como ayudante o andamiaje. Sin embargo, los experimentos en células mostraban algo desconcertante: SMG6 no podía funcionar correctamente sin SMG5, y la NMD colapsaba si faltaba cualquiera de los dos. Los autores utilizaron predicción estructural de última generación (AlphaFold), ensayos bioquímicos con proteínas purificadas y pruebas genéticas en líneas celulares humanas para resolver esta contradicción. Sus modelos predijeron que las regiones terminales de SMG5 y SMG6, llamadas dominios PIN, se acoplan entre sí para formar una estructura conjunta. A esta unidad compuesta —denominada «cPIN»— se propuso que fuera la verdadera máquina de corte en la NMD. 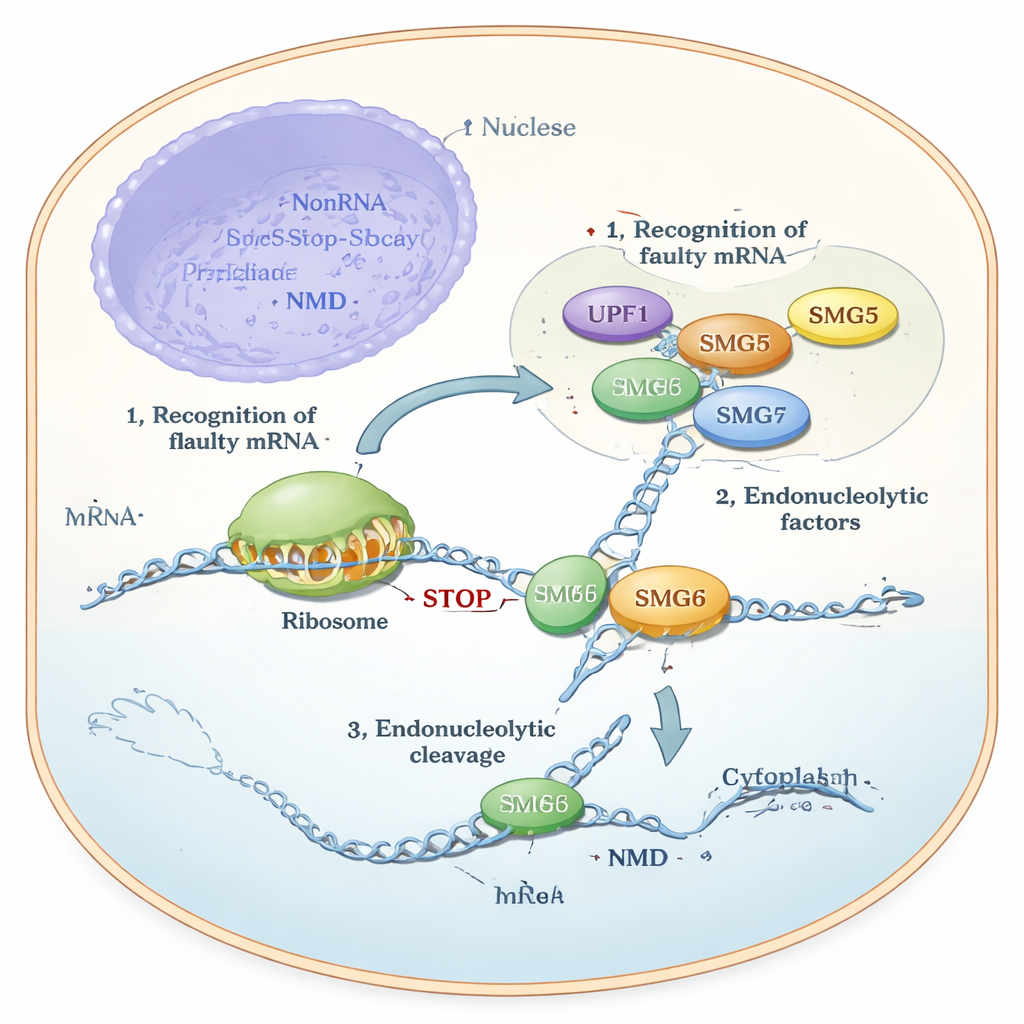
Reconstruyendo las tijeras moleculares en un tubo de ensayo
Para poner a prueba la predicción, el equipo produjo fragmentos humanos de SMG5 y SMG6 en bacterias y los purificó. Por separado, SMG6 mostró solo una capacidad débil para cortar un sustrato de ARN diseñado, y SMG5 por sí solo mostró virtualmente ninguna actividad. Pero cuando se mezclaron los dos fragmentos, la actividad de corte aumentó notablemente, incluso en condiciones en las que era poco probable la intervención de enzimas contaminantes. El mismo efecto apareció tanto en moléculas de prueba basadas en ARN lineal como circular, lo que indica que el incremento de la actividad procedía realmente del par SMG5–SMG6. La reacción cruzada química y la espectrometría de masas mostraron además que las dos proteínas se ponen en contacto estrecho, apoyando la idea de una asociación directa, aunque transitoria.
Completando el filo de corte
Los modelos estructurales sugirieron exactamente cómo SMG5 potencia a SMG6. SMG6 aporta cuatro aminoácidos ácidos que sostienen iones metálicos en el corazón del sitio catalítico, como es típico en esta familia de enzimas. Sorprendentemente, los modelos situaron un residuo ácido adicional procedente de SMG5 justo al lado de ellos, ampliando efectivamente la cavidad catalítica. Otros residuos con carga positiva de SMG5 se predijo que agarran la columna vertebral del ARN y ayudan a posicionarla para la escisión. Cuando los investigadores mutaron estos residuos críticos de SMG5 o SMG6, el complejo compuesto perdió gran parte de su capacidad de corte in vitro. Las mismas mutaciones tampoco lograron rescatar la NMD en células humanas diseñadas donde se había agotado la proteína normal, vinculando estrechamente el modelo estructural con la función celular real. 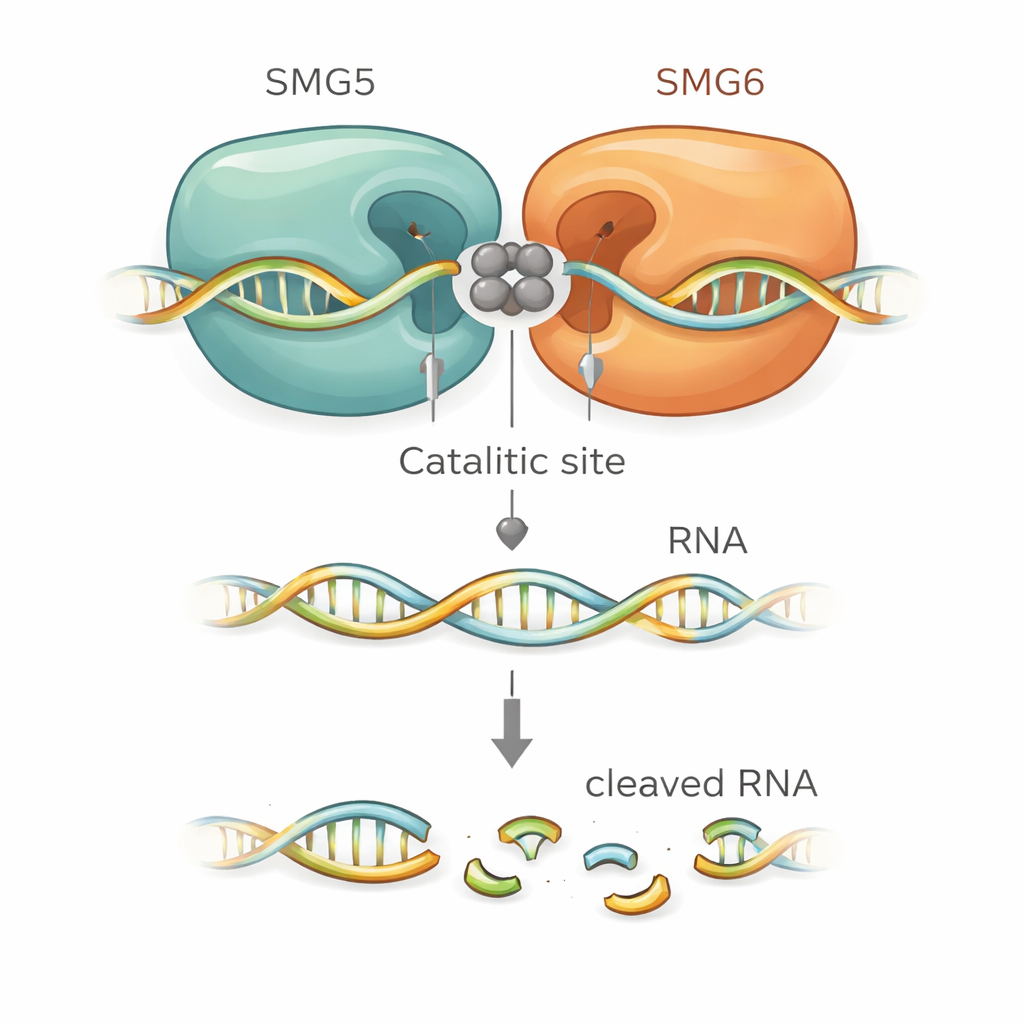
Demostrando que ambos socios son esenciales en las células
Debido a que la eliminación completa de SMG5 o SMG6 mata a las células, el equipo usó un sistema de «degrón» que les permite marcar cada proteína para que pueda ser destruida rápidamente con una pequeña molécula. Al combinar esta degradación rápida con interferencia de ARN lograron la eliminación casi total de SMG5, SMG6 o de un regulador central llamado UPF1. La secuenciación de ARN a escala del genoma reveló entonces lo que sucede con la NMD cuando se pierde cada factor. El agotamiento de SMG5 o UPF1 produjo cambios casi idénticos en los ARNs celulares, con transcripciones defectuosas y sensibles a NMD acumulándose fuertemente. La eliminación de SMG6 dio un efecto muy similar, aunque algo más leve. Estos datos muestran que SMG5 y SMG6 no son ramas paralelas opcionales de la vía; más bien, actúan junto con UPF1 como componentes centrales de una única vía principal de degradación.
Por qué esto importa para la salud celular
En términos sencillos, el estudio muestra que SMG5 y SMG6 encajan para formar un único y potente par molecular de tijeras que corta mensajes genéticos defectuosos. SMG6 aporta la mayor parte de la hoja, pero SMG5 suministra un borde faltante y ayuda a sujetar el ARN en su sitio, convirtiendo un cortador débil en uno eficiente. Este «cPIN» compuesto explica por qué las células requieren absolutamente ambas proteínas para mantener sus mensajes de ARN limpios. Al clarificar cómo se activa el paso clave de corte de la NMD solo cuando se reconocen mensajes defectuosos, el trabajo ofrece una imagen más nítida de cómo las células previenen la acumulación de proteínas truncadas y tóxicas y regulan con precisión la expresión génica.
Cita: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Palabras clave: degradación de ARNm mediada por codón de parada prematuro, control de calidad del ARN, SMG5 SMG6, vigilancia del ARNm, regulación de la expresión génica