Clear Sky Science · es
Interacciones metal-soporte moduladas para la electroreducción eficiente de nitratos a potenciales positivos
Convertir agua contaminada en un recurso útil
La contaminación por nitratos en ríos, lagos y aguas residuales industriales es una preocupación creciente para los ecosistemas y la salud humana, pero también representa un recurso desaprovechado. El mismo nitrógeno que daña las vías fluviales puede transformarse de nuevo en amonio, piedra angular de fertilizantes, combustibles y productos químicos. Este estudio explora una nueva forma de limpiar aguas contaminadas con nitratos mientras se recupera amonio usando electricidad de manera más eficiente que antes, apuntando hacia una agricultura más limpia, tratamientos de residuos más inteligentes y nuevas formas de almacenamiento energético.
Por qué el exceso de nitrógeno es un problema
La agricultura moderna y la industria dependen en gran medida del amonio, producido principalmente por el energético proceso de Haber–Bosch. Durante su uso y eliminación, gran parte de este amonio acaba como nitrato en las aguas residuales, alterando el ciclo natural del nitrógeno y contribuyendo a problemas ambientales como floraciones algales y contaminación del agua potable. Los métodos actuales para eliminar nitratos pueden ser costosos y a menudo simplemente ocultan o diluyen el problema. La conversión eléctrica de nitrato de vuelta a amonio ofrece una vía para limpiar el agua mientras se recicla el nitrógeno, pero la mayoría de los sistemas actuales exigen un gran aporte energético porque deben funcionar a voltajes fuertemente negativos.
Diseñar una superficie catalítica más inteligente
Para abordar este reto, los investigadores diseñaron un nuevo catalizador formado por diminutos agregados de rutenio anclados sobre láminas delgadas de hidróxido de cobalto. Utilizaron un método simple de “autocorrosión”: una espuma metálica se disuelve lentamente en presencia de una sal de rutenio y oxígeno, formando una capa fresca de hidróxido mientras los agregados de rutenio se depositan directamente sobre ella. Este proceso puede aplicarse a distintos metales, pero el equipo se centró en soportes de cobalto, níquel y hierro para ver cómo cada uno afecta al rendimiento. Microscopía y espectroscopía confirmaron que los agregados de rutenio son ultrafinos y están repartidos de manera uniforme sobre las láminas de hidróxido, y que se producen transferencias electrónicas entre el metal y su soporte, afinando sutilmente cómo la superficie interactúa con el nitrato y el agua.

Equilibrar agarre y flujo para una mejor conversión
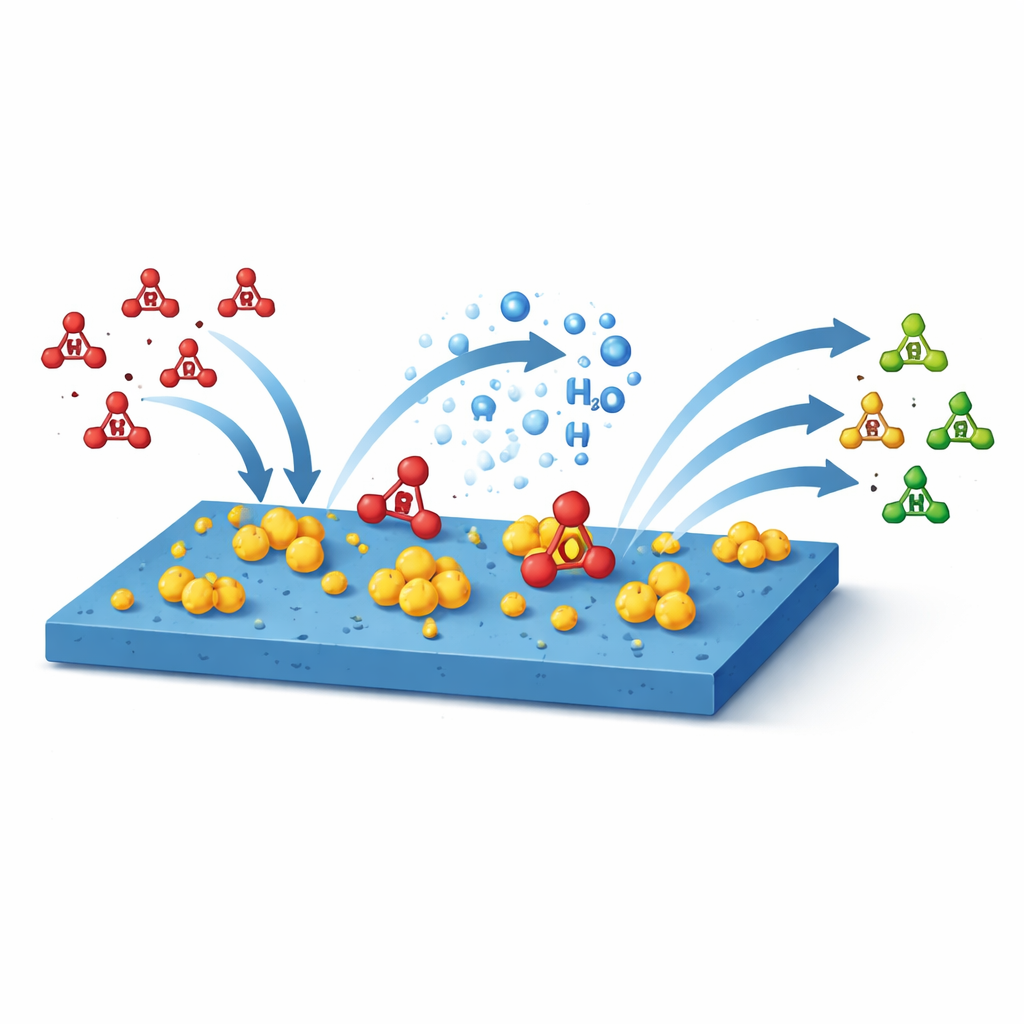
Para que la reacción sea eficiente deben ocurrir dos cosas en armonía: el nitrato debe adherirse a la superficie del catalizador con la suficiente firmeza para reaccionar, y el agua en la interfaz debe escindirse para aportar átomos de hidrógeno “activos” que transformen gradualmente el nitrato en amonio. Si el nitrato se une demasiado, la superficie se atasca; si lo hace débilmente, se pierde sin reaccionar. Del mismo modo, una escisión lenta del agua priva a la reacción de hidrógeno. Las pruebas mostraron que el catalizador a base de cobalto alcanza este punto óptimo. En comparación con las versiones sobre níquel y hierro, inicia la reacción más cerca del voltaje ideal, alcanza casi un 100% de selectividad hacia el amonio y logra una eficiencia energética de aproximadamente el 50% a un voltaje de operación positivo—una demanda energética inusualmente baja para esta química. Además mantiene alta actividad durante más de 1.200 horas a niveles de corriente relevantes para la industria, mientras reduce los nitratos en aguas residuales simuladas por debajo de los límites de agua potable.
Escudriñando los pasos ocultos
Para entender por qué el cobalto funciona mejor, el equipo monitorizó la reacción en tiempo real usando sondas ópticas y electroquímicas, y respaldó las observaciones con modelado por ordenador. Encontraron que el soporte de hidróxido de cobalto reconfigura la capa delgada de agua en la superficie, debilitando su red de puentes de hidrógeno de modo que las moléculas de agua se escinden más fácilmente en fragmentos reactivos. Al mismo tiempo, la interacción electrónica entre el hidróxido de cobalto y el rutenio ajusta la fuerza con que se unen el nitrato y sus intermedios. Los cálculos muestran que en esta superficie, el paso más difícil—convertir un fragmento parecido a nitrosilo en una especie más rica en hidrógeno—requiere mucho menos energía que en las versiones soportadas sobre níquel o hierro. En efecto, el soporte de cobalto ofrece el equilibrio justo: el nitrato se retiene con firmeza pero sin quedar atrapado, y el agua aporta hidrógeno con rapidez, permitiendo que la secuencia de pasos desde el nitrato al amonio avance sin tropiezos.
Del tratamiento de residuos al almacenamiento de energía y el reciclado de plásticos
Partiendo del catalizador eficiente, los autores montaron una batería recargable que empareja zinc metálico con la reducción de nitrato en el cátodo de cobalto–rutenio. Durante la descarga, el nitrato se convierte en amonio mientras el zinc se oxida, suministrando energía eléctrica. Durante la carga, sustituyen la habitual reacción formadora de oxígeno por la oxidación más suave del etilenglicol, un bloque de construcción que puede recuperarse de plásticos residuales. Este giro reduce la energía necesaria para recargar la batería y mejora las moléculas derivadas del plástico hacia productos de mayor valor, mientras que el amonio producido puede convertirse en sales de amonio. El dispositivo híbrido funciona de manera estable durante muchos ciclos, ilustrando cómo el control de la contaminación, la recuperación de recursos y el almacenamiento de energía pueden integrarse en un solo sistema.
Una nueva palanca para una química más limpia
En términos accesibles, este trabajo muestra que afinar la interacción entre un catalizador metálico y su material de soporte puede mejorar drásticamente la eficiencia de convertir nitrato nocivo en agua en amonio útil. Al elegir un soporte que ni retenga el nitrato con demasiada fuerza ni lo deje escapar, y que además facilite la ruptura del agua para alimentar la reacción, los investigadores alcanzan alta eficiencia a voltajes más suaves y mantienen el rendimiento durante largos periodos. El mismo principio de diseño—ajustar cuidadosamente las interacciones metal-soporte—podría guiar el desarrollo de futuros catalizadores para muchos otros procesos químicos sostenibles.
Cita: Tang, Y., Wan, Y., Yan, W. et al. Modulated metal-support interactions for efficient nitrate electroreduction at positive potentials. Nat Commun 17, 3006 (2026). https://doi.org/10.1038/s41467-026-69802-5
Palabras clave: contaminación por nitratos, producción de amonio, electrocatalisis, tratamiento de aguas residuales, almacenamiento de energía