Clear Sky Science · es
Análogos no hidrolizables de acetillisina para estudiar la acetilación de proteínas in vitro y en células
Por qué importan las pequeñas etiquetas químicas en las proteínas
Dentro de cada célula, las proteínas se modifican continuamente con pequeñas etiquetas químicas que actúan como interruptores de encendido/apagado o como reguladores de intensidad de su actividad. Una de las más importantes se llama acetilación, que puede alterar el comportamiento de una proteína sin cambiar su código genético subyacente. Entender exactamente qué hace la acetilación en un sitio concreto de una proteína determinada ha resultado sorprendentemente difícil, porque las células pueden eliminar estas etiquetas con la misma rapidez con que las añaden. Este estudio presenta un ingenioso “sustituto” químico de la acetilación que no puede ser eliminado, dando a los científicos una forma de congelar esos interruptores y observar lo que ocurre.
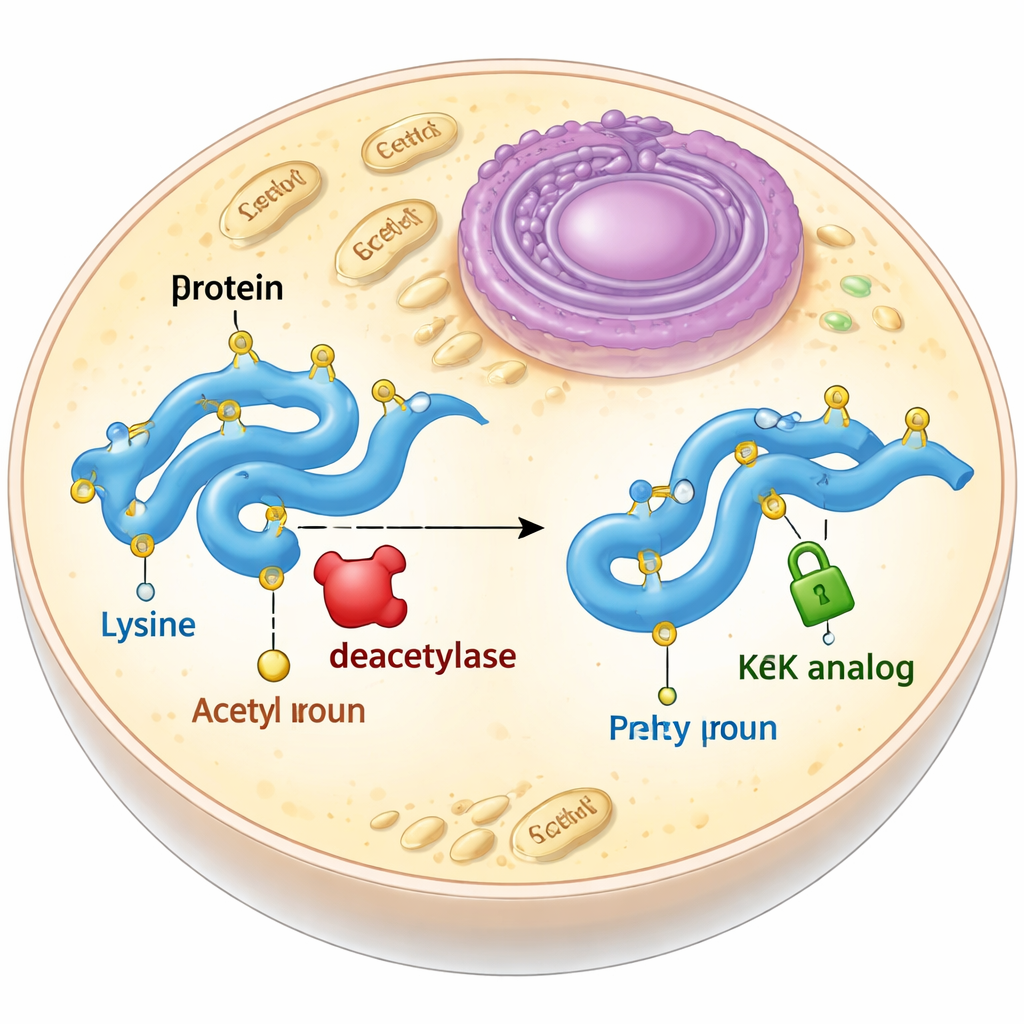
Un sustituto estable para una etiqueta efímera
La acetilación suele producirse sobre un bloque constituyente de las proteínas llamado lisina. Cuando una lisina se acetila, pierde su carga positiva y su cadena lateral se alarga un poco. Los biólogos suelen intentar imitar esto mutando la lisina por otro aminoácido, la glutamina, que es neutra pero más corta, o incorporando acetillisina real mediante expansión del código genético. Ambos enfoques tienen inconvenientes: la glutamina no reproduce completamente los cambios de forma causados por la acetilación, y la acetillisina real es rápidamente eliminada por enzimas llamadas desacetilasas dentro de las células. Los autores se propusieron diseñar y probar análogos de acetillisina que mantuvieran el tamaño y la forma adecuados pero no pudieran ser eliminados.
Probando nuevos imitadores químicos en una proteína modelo
El equipo se centró primero en la ubiquitina, una proteína pequeña y bien estudiada que a su vez recibe muchas etiquetas diferentes. Mediante ingeniería genética avanzada colocaron variantes de lisina en una posición de la ubiquitina: acetillisina natural, dos análogos no removibles llamados TFAcK y cetolisina (KeK), y sustitutos habituales como glutamina, alanina y arginina. A continuación examinaron cómo afectaban estos cambios a la forma y función de la ubiquitina. Mediciones de RMN de alta resolución mostraron que la acetillisina, TFAcK y KeK producían cambios estructurales casi idénticos, especialmente alrededor de una hélice central, mientras que la glutamina y otras mutaciones simples no lo hacían. Pruebas funcionales con una enzima llamada HDM2 revelaron que la ubiquitina que portaba acetillisina, TFAcK o KeK se comportaba de forma similar entre sí y distinta respecto a la versión con glutamina, subrayando que la longitud y el volumen de la cadena lateral —no solo su carga— son cruciales.
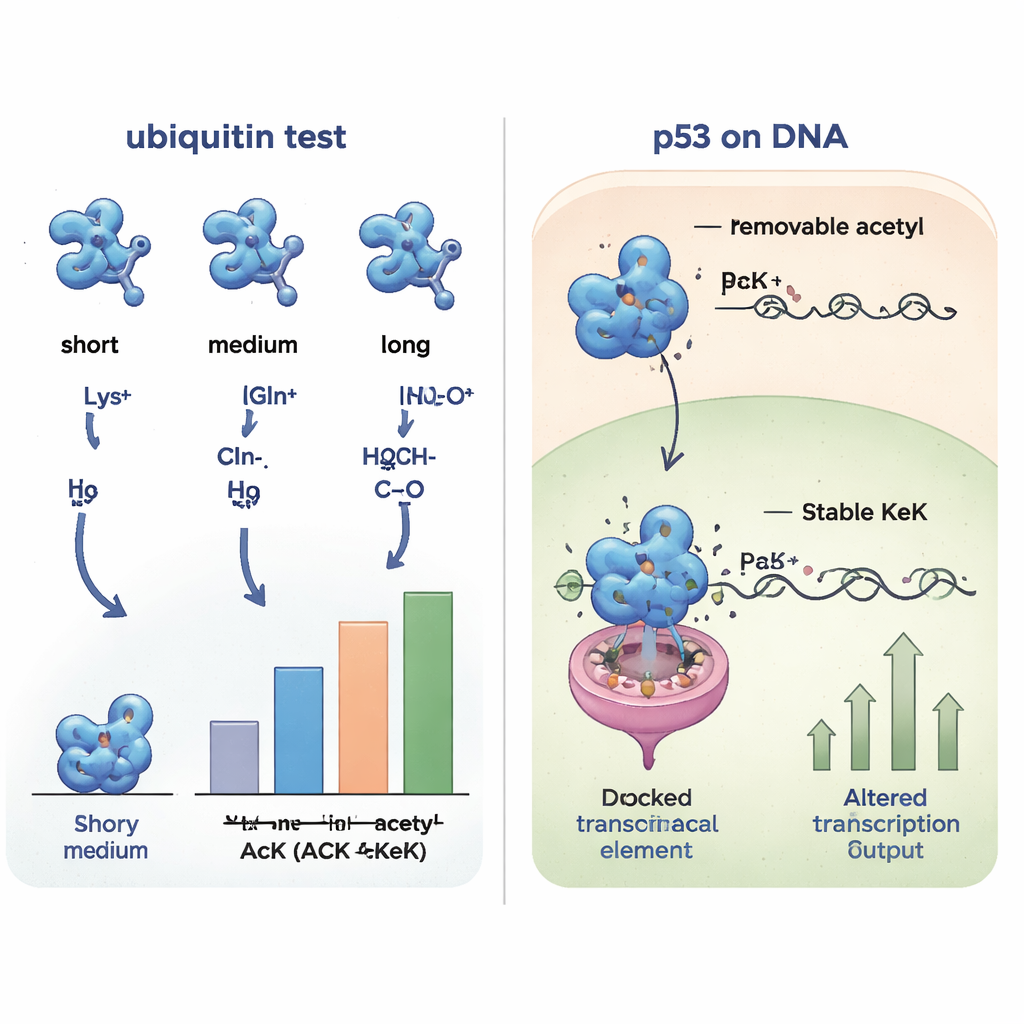
Rastreando asociaciones proteicas en toda la célula
Dado que pequeños cambios estructurales pueden alterar con qué socios interactúa una proteína, los investigadores compararon a continuación cómo las distintas versiones de ubiquitina se unían a otras proteínas procedentes de extractos de células humanas. Tras pescar los interactores y caracterizarlos mediante espectrometría de masas, encontraron que la ubiquitina que contenía acetillisina, TFAcK o KeK compartía patrones de interacción muy similares, mientras que las formas con glutamina o alanina formaban un grupo distinto. Las variantes con carga positiva (lisina o arginina) constituían otro grupo más. Esta comparación sistemática mostró que los análogos no removibles TFAcK y, especialmente, KeK imitan tanto la estructura como el comportamiento de unión de la acetilación real mucho mejor que la sustitución tradicional por glutamina.
Bloquear la acetilación en el supresor tumoral p53
Para ver si estas herramientas funcionan dentro de células vivas, los autores se centraron en p53, un supresor tumoral clave a menudo llamado el “guardián del genoma”. Lisinas específicas en la región de unión al ADN de p53 pueden acetilarse, cambiando los genes que activa, como los que detienen el ciclo celular o desencadenan la muerte celular. El equipo diseñó células humanas de modo que p53 incorporara acetillisina, TFAcK o KeK en dos posiciones lisina importantes (120 y 164) solo cuando se suministraba el aminoácido no convencional correspondiente. Las tres pudieron incorporarse en p53, pero medidas detalladas mostraron que, en células, los grupos acetil y TFAcK eran mayormente eliminados por desacetilasas, mientras que KeK permanecía intacto. Cuando probaron la capacidad de p53 para activar un gen reportero y el gen natural p21, las variantes que llevaban KeK en estos sitios eran mucho menos activas, lo que coincide con lo esperado cuando la acetilación en esas posiciones queda bloqueada, mientras que la acetillisina y TFAcK se comportaron más como p53 normal porque habían sido desacetiladas.
Qué significa esto para estudiar las decisiones celulares
En conjunto, el estudio muestra que KeK es un sustituto fiel y no removible de la acetillisina: reproduce de forma cercana los cambios estructurales, las preferencias de unión y las consecuencias funcionales de la acetilación, pero no puede ser borrado por las enzimas celulares. Para el público no especializado, esto significa que los investigadores disponen ahora de una forma de “congelar” un interruptor químico normalmente reversible en un único sitio de una proteína y observar cómo afecta procesos como la regulación génica y las decisiones sobre el destino celular. Esto debería facilitar mucho separar los roles específicos de la acetilación de los de otras modificaciones superpuestas y, en última instancia, podría aclarar cómo la acetilación de proteínas mal regulada contribuye a enfermedades como el cáncer.
Cita: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Palabras clave: acetilación de proteínas, modificación postraduccional, ubiquitina, p53, expansión del código genético