Clear Sky Science · es
Remodelado transcriptómico dinámico en células progenitoras neuronales humanas trasplantadas descubre mecanismos de preservación de la visión en un modelo de rata con retinitis pigmentosa
Por qué importa proteger la visión que se apaga
La retinitis pigmentosa es un conjunto de enfermedades hereditarias que privan lentamente a las personas de la vista, con frecuencia comenzando por la ceguera nocturna y avanzando hasta la ceguera legal. Dado que cientos de mutaciones génicas diferentes pueden causar esta afección, tratar cada una individualmente mediante terapia génica resulta complicado. Este estudio explora un enfoque más universal: trasplantar células progenitoras neuronales humanas —células nerviosas inmaduras cultivadas en laboratorio— en el ojo para proteger las células restantes que detectan la luz. Comprender exactamente cómo se comportan estas células injertadas y cómo ayudan a preservar la visión podría orientar tratamientos futuros no solo para la retinitis pigmentosa, sino también para otros trastornos que causan ceguera.
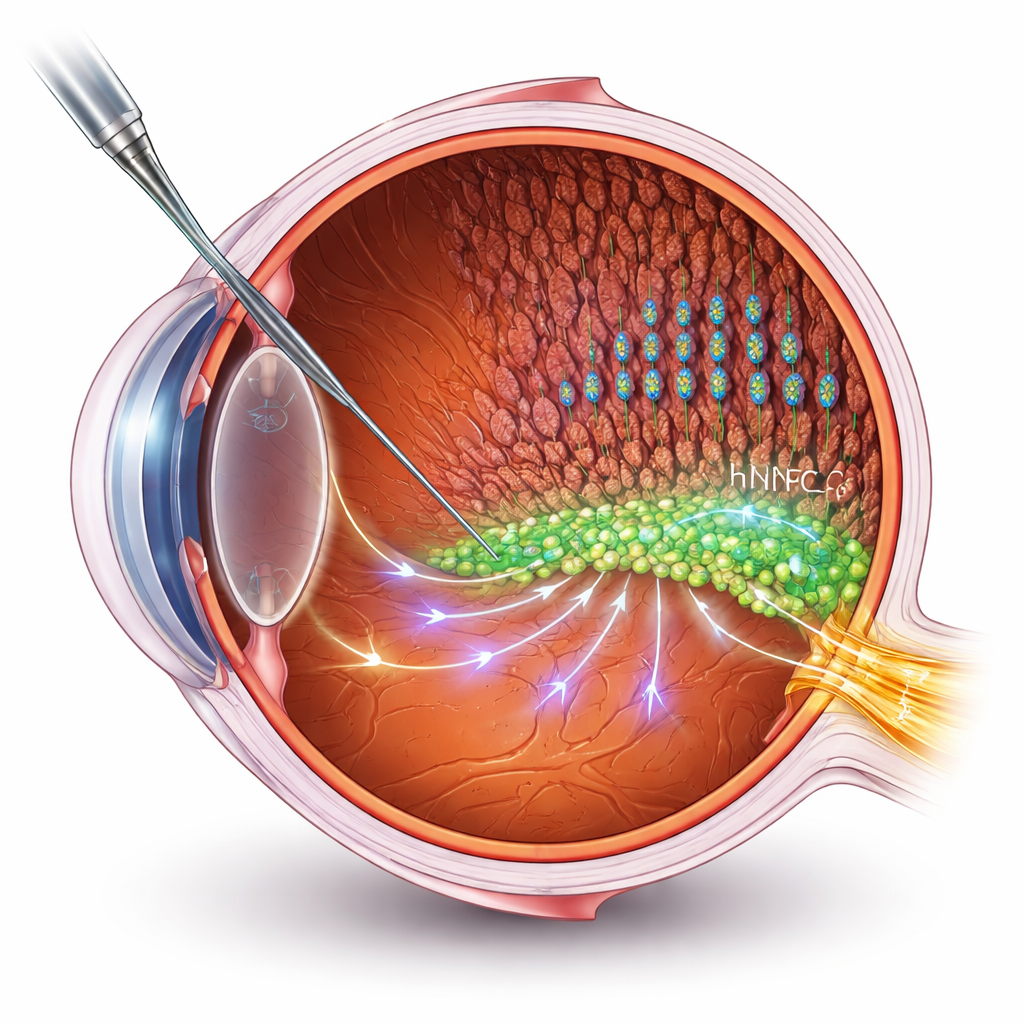
Ayudar a las células en lugar de reemplazarlas
Muchas terapias con células madre persiguen reemplazar células muertas o dañadas. Pero en las enfermedades retinianas avanzadas, reconstruir nuevas conexiones con el cerebro supone un obstáculo técnico importante. Aquí, los investigadores siguen una vía distinta: usar células progenitoras neuronales humanas (hNPCs) como “asistentes” que apoyan las propias células retinianas del paciente. Trasplantaron hNPCs en el espacio subretiniano de un conocido modelo de rata con retinitis pigmentosa y midieron la visión mediante registros eléctricos y pruebas de comportamiento. Las ratas tratadas mantuvieron mejor función visual y capas de fotorreceptores —los bastones y conos que captan la luz— más intactas que los animales no tratados, aunque la degeneración siguió progresando lentamente.
Cómo cambian las células injertadas dentro del ojo enfermo
Para ver qué ocurre a nivel molecular, el equipo empleó secuenciación de ARN a escala de célula única, una técnica que perfila qué genes están activados en miles de células individuales. Siguieron a las hNPCs injertadas en dos puntos temporales, aproximadamente en estadios temprano y más avanzado tras el trasplante. En lugar de convertirse en nuevos fotorreceptores, la mayoría de las células trasplantadas maduraron hacia tipos similares a astrocitos, con una fracción menor mostrando marcadores de oligodendrocitos o neuronas inmaduras. Con el tiempo, estas células se estabilizaron, adoptando rasgos que sugieren adaptación para sobrevivir en un entorno estresante y degenerativo e interactuar estrechamente con las células retinianas vecinas.
Señales protectoras, metabolismo y limpieza
Las hNPCs produjeron una mezcla rica de proteínas protectoras conocidas como factores tróficos. Entre ellas figuraban MANF y MYDGF, vinculadas a la supervivencia celular, la reducción del estrés oxidativo y la atenuación de la inflamación, así como otros factores como midkina y pleiotrofina que respaldan el crecimiento y la movilidad de células neuronales. Estas moléculas parecieron actuar tanto sobre el injerto como sobre la retina circundante. En las ratas tratadas, los bastones y conos presentaron patrones de actividad génica más cercanos a controles saludables, con mejor soporte para la señalización visual y el mantenimiento celular. Las células injertadas también potenciaron vías implicadas en la eliminación de desechos celulares y en el ajuste del metabolismo, lo que sugiere que ayudan a los fotorreceptores a manejar las demandas energéticas y los subproductos tóxicos que se acumulan durante la enfermedad.
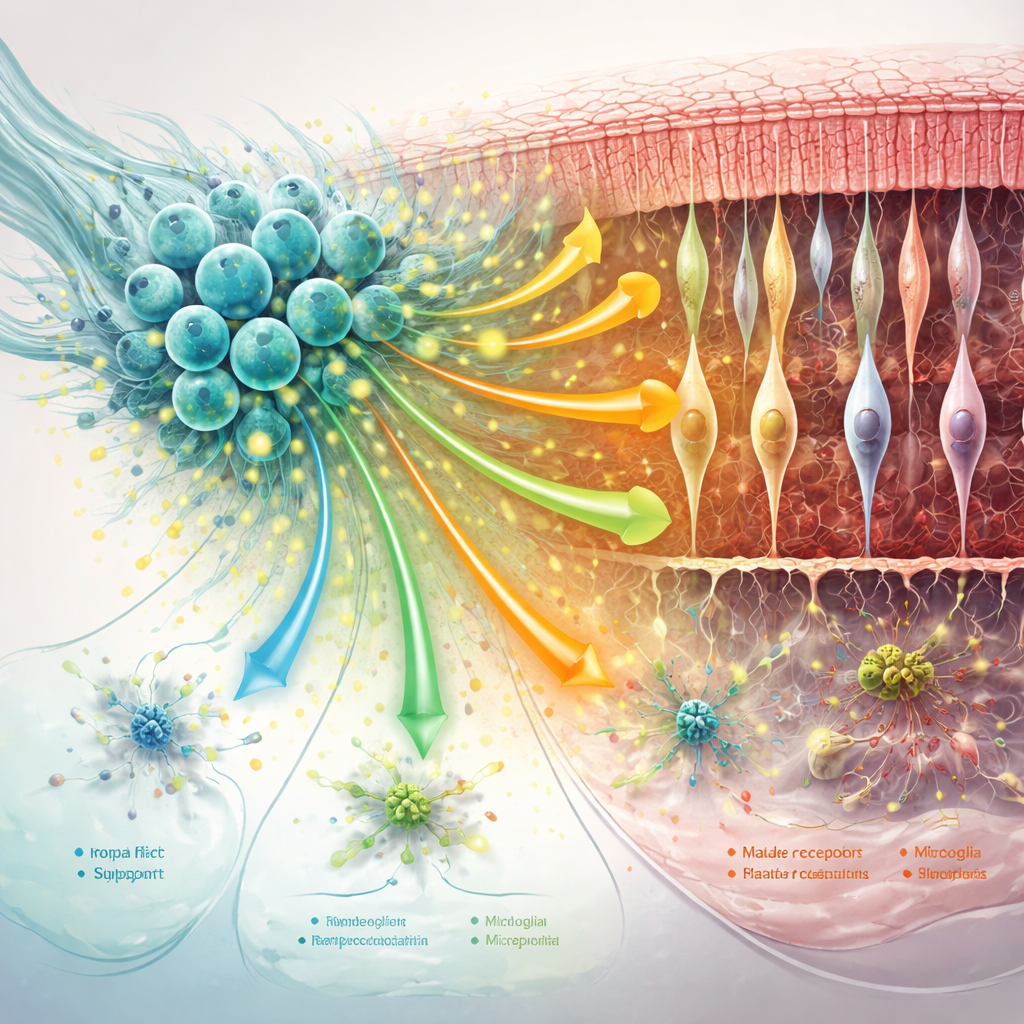
Calmar las células de soporte y remodelar el vecindario retiniano
La red de soporte de la retina —glía de Müller, microglía y la matriz proteica circundante— desempeña un papel importante tanto en agravar como en ralentizar la degeneración. El estudio encontró que el tratamiento con hNPC redujo marcadores clave de los cambios “reactivos” perjudiciales en la glía de Müller y desplazó a la microglía fuera de estados excesivamente inflamatorios, especialmente en los primeros tiempos. Al mismo tiempo, se reforzaron señales de comunicación que ayudan a estabilizar sinapsis, a mantener la adhesión celular y a preservar el andamiaje alrededor de los fotorreceptores. A medida que la enfermedad avanzó, algunos de estos beneficios se atenuaron: la comunicación entre células en general se debilitó, ciertas vías protectoras —incluida la señalización relacionada con MANF— disminuyeron, y las células de soporte adoptaron perfiles más centrados en el estrés y la respuesta inmune.
Qué significa esto para futuras terapias oculares
Para el lector no especialista, la conclusión es que las células progenitoras neuronales humanas trasplantadas pueden actuar como “primeros intervinientes” en el lugar en una retina en degeneración. No reconstruyen la retina desde cero, pero liberan moléculas protectoras, ajustan el metabolismo, calman la inflamación dañina y ayudan a mantener la estructura local, todo lo cual ralentiza la pérdida de visión. Sin embargo, este efecto protector disminuye con el tiempo a medida que el entorno se vuelve más hostil y el diálogo entre injerto y células huésped se debilita. Los autores sugieren que potenciar factores clave como MANF y mejorar la salud de la retina huésped —posiblemente mediante la ingeniería genética del injerto o tratamientos combinados— podría ser esencial para convertir este respiro temporal en una preservación duradera de la vista.
Cita: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Palabras clave: retinitis pigmentosa, terapia con células madre, degeneración retiniana, neuroprotección, secuenciación de ARN a escala de célula única