Clear Sky Science · es
Limitaciones de la clonación seriada en mamíferos
Por qué copiar mamíferos no es tan sencillo como parece
Durante décadas, la idea de copiar animales—hasta su ADN—ha cautivado al público, desde la oveja Dolly hasta los sueños de resucitar especies desaparecidas. Pero, ¿pueden los mamíferos sostenerse únicamente mediante la clonación, generación tras generación, como hacen algunas plantas y animales sencillos? Este estudio siguió a una línea de ratones producida íntegramente por clonación durante casi 20 años para responder a esa pregunta. Los resultados revelan por qué, a pesar de nuestros avances técnicos, la naturaleza sigue confiando en la reproducción sexual para mantener la salud de los mamíferos a largo plazo.
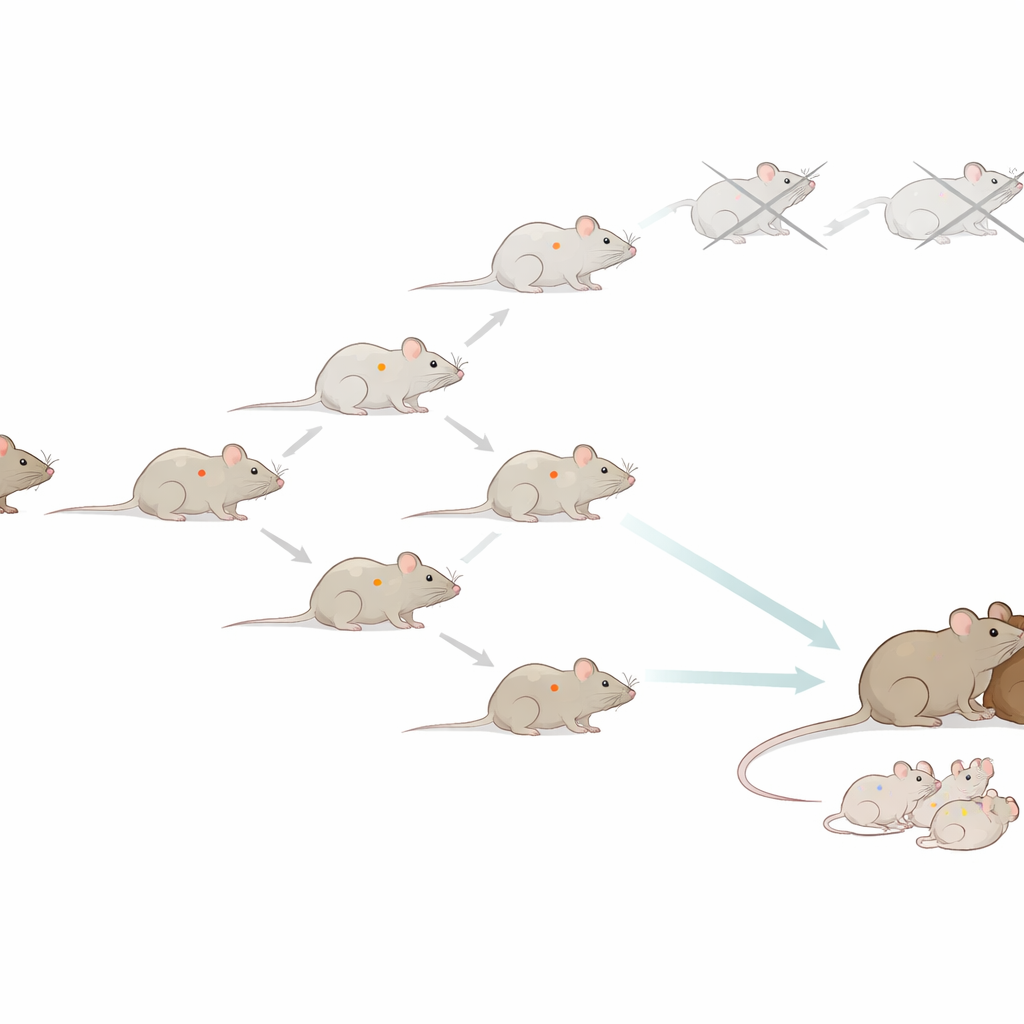
Siguiendo una línea de ratones durante veinte años
Los investigadores partieron de una única ratona y usaron sus células somáticas para crear un ratón clonado. Cuando ese primer clon creció, tomaron células de él para hacer el siguiente clon, y repitieron el proceso una y otra vez. En total intentaron más de 30.000 procedimientos de transferencia nuclear y produjeron más de 1.200 animales clonados, alcanzando 58 generaciones desde el donante original. Muchos de estos ratones parecían y se comportaban como animales normales, con vidas útiles de alrededor de dos años y pesos corporales similares. Al principio, la tasa de éxito de la clonación incluso mejoró con cada generación, lo que sugería que la clonación seriada de mamíferos podría ser práctica a largo plazo.
Cuerpos sanos, pero daño oculto
En apariencia, los ratones clonados estaban bien. Sus órganos internos y, en especial, sus placentas mostraron las anomalías habituales observadas en experimentos de clonación, como ser más grandes que las de ratones concebidos de forma natural, pero estas anormalidades no empeoraron con cada generación. El equipo también comprobó cómo se desarrollaban los embriones en el laboratorio y examinó los patrones de marcas químicas en las proteínas que empaquetan el ADN—características que a menudo fallan en la clonación. Los embriones tempranos procedentes de clones de generaciones tardías se parecían mucho a los de la primera generación clonada. Esto sugería que los problemas conocidos de “reprogramación” en la clonación no se estaban acumulando de forma constante con el tiempo.
Las mutaciones se acumulan con cada copia
La historia real emergió cuando los científicos secuenciaron los genomas de ratones de distintas generaciones de clonación. Con cada ronda de copiado aparecían nuevos cambios en el ADN: en promedio unas 70 mutaciones puntuales por generación y entre una y dos alteraciones estructurales, incluidas grandes reordenaciones y pérdidas cromosómicas. Muchos de estos cambios recordaban a las mutaciones naturales observadas en la reproducción ordinaria, pero la diferencia clave es que, en la clonación, no hay mezcolanza de cromosomas mediante el apareamiento que ayude a eliminar variantes dañinas. Con el tiempo, especialmente tras aproximadamente la generación 25, empezaron a acumularse mutaciones perjudiciales—como la pérdida de un cromosoma X entero o roturas e intercambios entre cromosomas. La proporción de mutaciones probablemente capaces de alterar genes importantes prácticamente se duplicó en generaciones tardías.
Los óvulos muestran el punto de ruptura
Para ver cómo afectaba este daño oculto a la reproducción, el equipo se centró en los óvulos de ratonas clonadas de generaciones tardías. Cuando estos óvulos fueron inducidos a desarrollarse sin espermatozoides, casi ninguno llegó a formar embriones tempranos saludables, lo que indica que muchos cargaban combinaciones letales de mutaciones. La fertilización con esperma de machos normales mejoró algo el desarrollo, pero la tasa de éxito seguía cayendo drásticamente en generaciones tardías. Experimentos que intercambiaron los núcleos y el citoplasma entre óvulos de ratonas normales y de generaciones clonadas tardías mostraron que tanto el material genético como el citoplasma del óvulo se habían visto comprometidos. Finalmente, en la generación 58, todos los descendientes clonados murieron poco después del nacimiento y la línea de clonación no pudo continuarse.
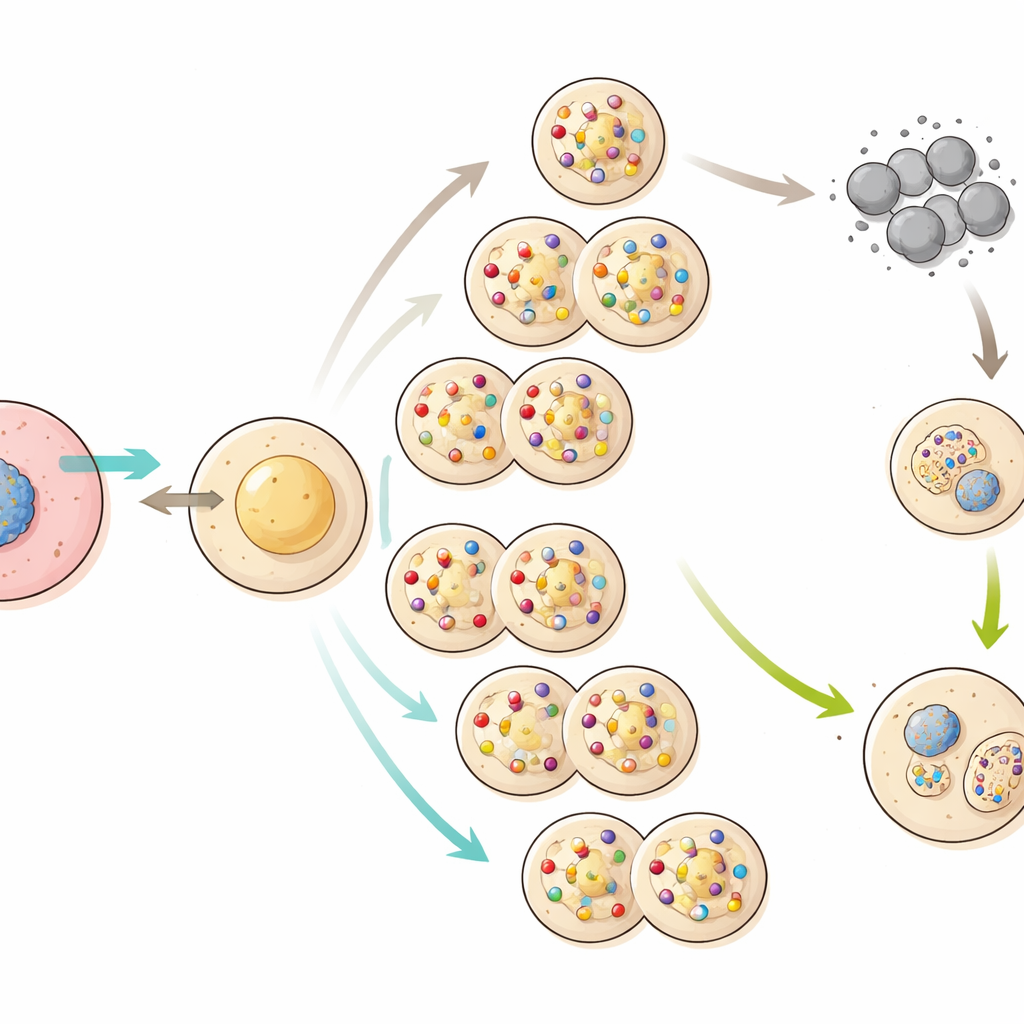
La reproducción sexual como sistema de reparación
Cuando los científicos permitieron que los ratones clonados de generaciones tardías se aparearan de forma natural con machos normales, apareció un patrón distinto. Aunque estas madres clonadas tuvieron camadas pequeñas, algunos de sus críos—y en especial sus nietos—estaban mucho más sanos. Las placentas de la generación siguiente volvieron a reducirse hacia tamaños más normales y el desarrollo en general mejoró. Esto sugiere que la mezcla y el reparto de cromosomas durante la formación de óvulos y espermatozoides, seguido de la fertilización, puede fragmentar combinaciones dañinas de mutaciones y eliminar muchas de las peores alteraciones. En otras palabras, el sexo actuó como un sistema de limpieza incorporado que la clonación pura no tiene.
Lo que esto significa para el futuro de la clonación
Al seguir con detalle una sola línea clonada de ratones a lo largo de 57 generaciones exitosas, este trabajo muestra que los mamíferos no pueden depender únicamente de la clonación para sostener una línea indefinidamente. La salud visible y las vidas útiles normales pueden enmascarar un declive genético lento, a medida que las mutaciones se acumulan hasta que la reproducción falla. Aunque la clonación sigue siendo una herramienta poderosa—para rescatar animales en peligro, multiplicar ganado valioso o preservar recursos genéticos—no es probable que reemplace a la reproducción sexual como estrategia a largo plazo para la supervivencia de los mamíferos. El estudio aporta un sólido respaldo experimental a la idea de que, en animales complejos, el sexo no solo sirve para producir descendencia: es la limpieza esencial del genoma.
Cita: Wakayama, S., Ito, D., Inoue, R. et al. Limitations of serial cloning in mammals. Nat Commun 17, 2495 (2026). https://doi.org/10.1038/s41467-026-69765-7
Palabras clave: clonación animal, mutaciones genéticas, reproducción en ratones, reproducción asexual, evolución del sexo