Clear Sky Science · es
GCN5 impulsa la progresión de la MASLD mediante la vía de señalización LXRα/SREBP1c–mediada por lipogénesis de novo
Por qué importa esta historia hepática
La enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD), antes denominada enfermedad del hígado graso no alcohólica, afecta hoy a aproximadamente una de cada cuatro personas en todo el mundo. A menudo se desarrolla de forma silenciosa, pero puede progresar a fibrosis, cáncer de hígado y graves problemas metabólicos. Este estudio descubre un “control de volumen” molecular que contribuye a la acumulación nociva de grasa en el hígado y muestra cómo reducir su actividad podría tanto proteger el hígado como potencialmente hacer más seguras las estrategias farmacológicas cardiovasculares existentes.
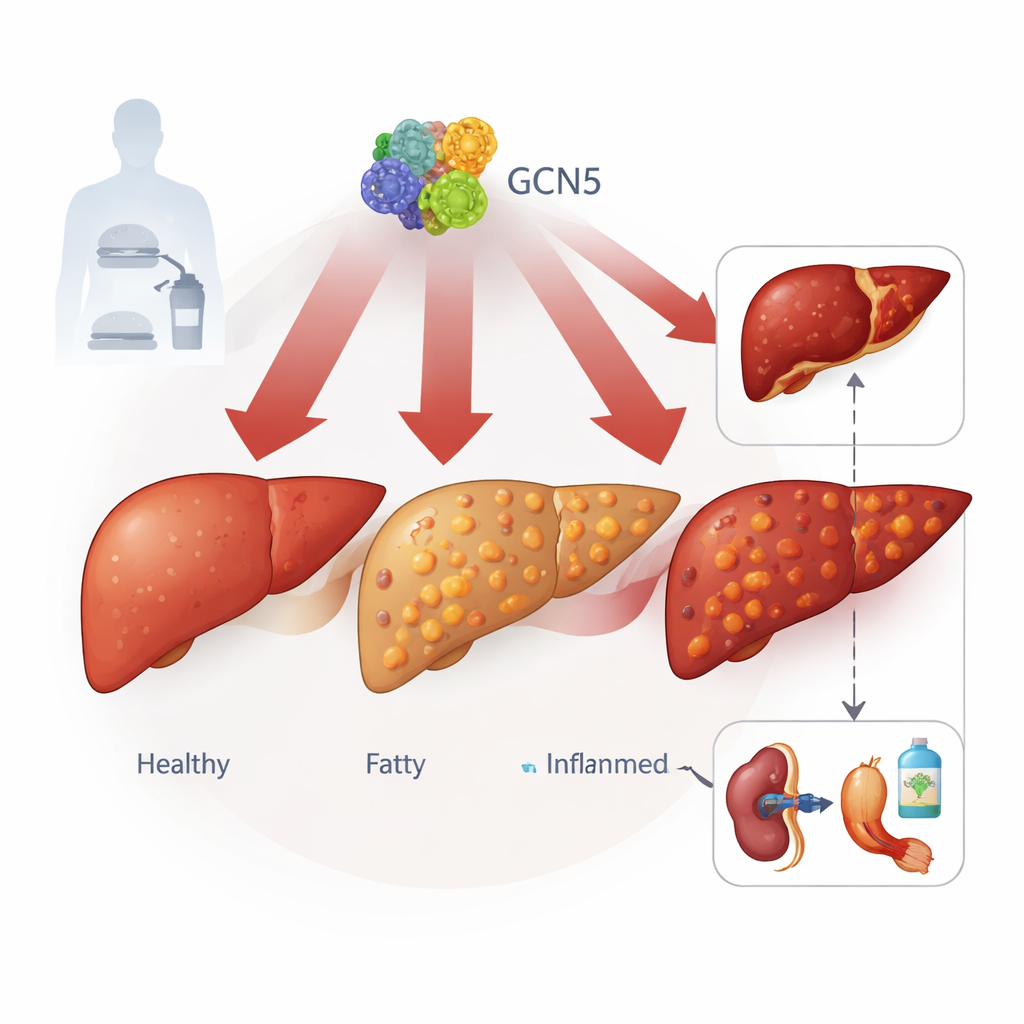
Un interruptor oculto dentro de las células hepáticas
Los autores se centran en una proteína llamada GCN5, conocida principalmente por regular el grado de empaquetamiento del ADN. Al estudiar tejido hepático de más de 100 personas, desde individuos sanos hasta casos graves de MASLD, y de varios modelos murinos de hígado graso inducido por dieta, hallaron que los niveles de GCN5 en las células hepáticas aumentan de forma sostenida a medida que empeora la enfermedad. Una proteína estrechamente relacionada, PCAF, no mostró este patrón, lo que sugiere que GCN5 desempeña un papel específico. Niveles altos de GCN5 se asociaron con más grasa hepática, lípidos sanguíneos elevados y marcadores más intensos de daño hepático, vinculando este interruptor molecular con la gravedad clínica real de la enfermedad.
Subir o bajar GCN5 en animales
Para probar causalidad, el equipo aumentó genéticamente o eliminó GCN5 específicamente en las células hepáticas de ratones. Cuando GCN5 se incrementó, los animales alimentados con dieta alta en grasas desarrollaron hígados más grandes y grasos, niveles más altos de lípidos sanguíneos y mayor daño celular hepático, aun cuando no comieron más ni ganaron peso corporal adicional. Las células hepáticas cultivadas en placa mostraron un comportamiento similar: exceso de GCN5 produjo gotículas lipídicas más grandes y numerosas. En contraste, los ratones diseñados para carecer de GCN5 solo en sus hepatocitos quedaron fuertemente protegidos. En varios modelos dietéticos que imitan la MASLD humana y su forma inflamatoria más severa, estos animales acumularon menos grasa hepática, mostraron lípidos sanguíneos y enzimas hepáticas más bajas y desarrollaron menos inflamación y fibrosis.
Cómo GCN5 empuja al hígado a fabricar grasa
Al profundizar en el metabolismo, los investigadores midieron numerosos ácidos grasos y sus precursores en el hígado. La pérdida de GCN5 redujo principalmente las grasas que el hígado sintetiza desde cero, un proceso conocido como lipogénesis de novo, mientras que las grasas poliinsaturadas de origen dietario permanecieron en gran medida sin cambios. Experimentos de expresión génica y trazado isotópico mostraron que GCN5 actúa aguas arriba de un regulador maestro de la síntesis de grasas llamado SREBP1c. Cuando GCN5 estaba activo, se activaban genes que construyen y modifican ácidos grasos, y la tasa interna de fabricación de grasas del hígado aumentaba. Eliminar o bloquear GCN5 atenuó este programa, reduciendo el flujo de carbono desde el azúcar hacia las grasas hepáticas recién sintetizadas.
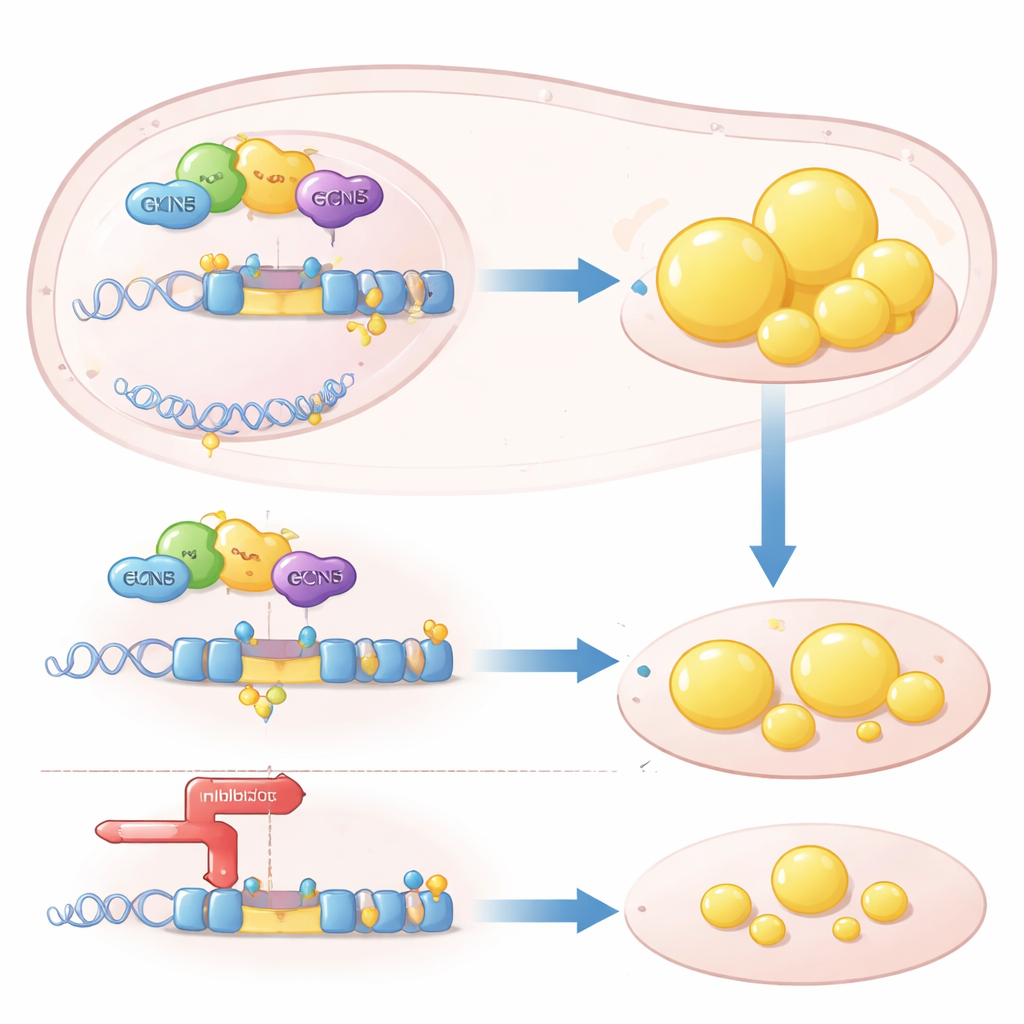
Una palanca epigenética sobre un gen clave de las grasas
Mecánicamente, GCN5 actúa como una palanca “epigenética”: modifica químicamente las histonas en el ADN para facilitar la lectura de ciertos genes. Los autores demostraron que GCN5 se recluta en la región de control del gen SREBP1c junto con un receptor nuclear llamado LXRα, que detecta moléculas relacionadas con el colesterol. Una vez allí, GCN5 añade marcas de acetilo a la histona H3, relajando la cromatina local y potenciando la transcripción de SREBP1c. Este efecto fue altamente selectivo: GCN5 aumentó la capacidad de LXRα para activar SREBP1c pero no otro blanco de LXR, ABCA1, que ayuda a eliminar colesterol de los tejidos. Sin GCN5, LXRα ya no podía reclutar eficazmente el promotor de SREBP1c y el programa de síntesis de grasas aguas abajo se detenía.
Un candidato farmacológico y una combinación prometedora
El equipo probó entonces CPTH2, un inhibidor de pequeña molécula de GCN5 que se concentra en el hígado. En modelos murinos ya sometidos a dietas grasas, CPTH2 redujo el tamaño del hígado, su contenido graso y los marcadores de daño sin toxicidad aparente ni cambios en la ingesta de alimentos. En células hepáticas humanas y murinas cultivadas, CPTH2 redujo las gotículas grasas y los triglicéridos únicamente cuando GCN5 estaba presente, confirmando la especificidad de su acción. Importante: tanto en células como en ratones tratados con compuestos activadores de LXR (diseñados para mejorar la eliminación de colesterol y combatir la aterosclerosis), CPTH2 bloqueó selectivamente el aumento indeseado de la producción de grasa impulsada por SREBP1c, mientras preservaba los genes que fomentan el transporte inverso del colesterol. Al combinarse con un agonista de LXR en ratones alimentados con dieta alta en grasas, CPTH2 redujo aún más los lípidos sanguíneos nocivos y el colesterol hepático y evitó la acumulación adicional de grasa en el hígado.
Qué significa esto para los pacientes
El estudio sitúa a GCN5 como un impulsor central de la acumulación de grasa hepática en la MASLD al vincular señales dietarias y hormonales con el interruptor de producción de grasa SREBP1c. Dado que GCN5 parece prescindible para el brazo beneficioso de LXR relacionado con la eliminación de colesterol, los fármacos que inhiban GCN5 —como CPTH2 o sucesores más avanzados— podrían atenuar la grasa y la inflamación hepáticas al tiempo que permiten que las terapias cardioprotectoras actúen. Para personas en riesgo tanto de enfermedad hepática grasa como de enfermedad cardiovascular, dirigir este interruptor epigenético podría algún día ofrecer una forma de proteger el hígado sin renunciar a los beneficios de mejorar el manejo del colesterol.
Cita: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Palabras clave: enfermedad del hígado graso, epigenética, metabolismo de lípidos, metabolismo hepático, receptores nucleares