Clear Sky Science · es
Control no por quelación en alilaciones de cetonas α‑oxi usando alilatránes de grupo 14
Construir formas moleculares con mayor precisión
Muchos fármacos y productos naturales funcionan únicamente cuando sus átomos están dispuestos en una forma tridimensional concreta. Por ello, los químicos dedican enormes esfuerzos a aprender cómo «empujar» nuevos fragmentos sobre una molécula desde un lado u otro. Este artículo describe una forma nueva de incorporar grupos alilo —cadenas cortas de tres carbonos— a una clase común de moléculas, proporcionando acceso a estructuras imagen‑espejo que hasta ahora eran muy difíciles de obtener.
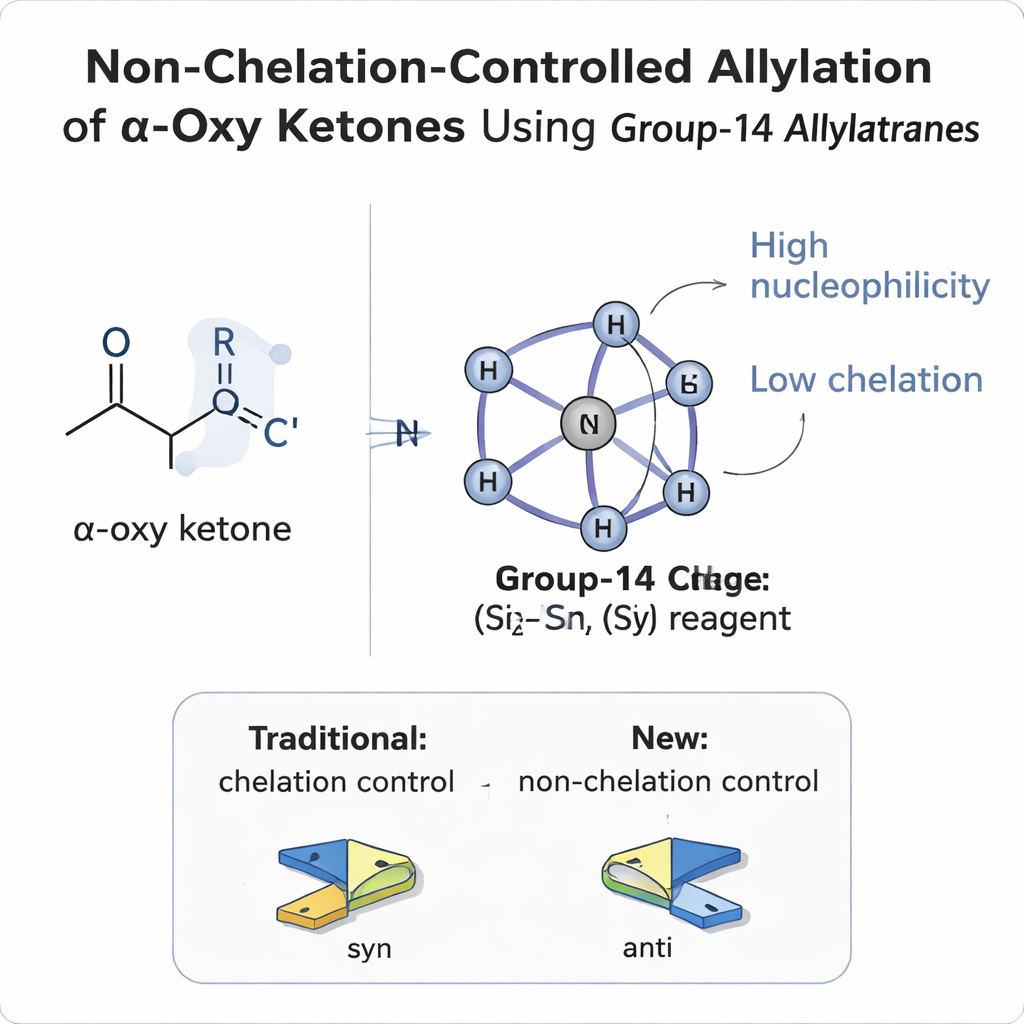
Por qué es tan difícil controlar los lados de una molécula
Cuando se añade un nuevo grupo a un doble enlace carbono‑oxígeno plano (un carbonilo), puede atacar desde cualquiera de las dos caras, como una bola que choca contra una moneda por encima o por debajo. Si ya existe un sustituyente vecino en el carbono contiguo (la posición α), el resultado son dos posibles productos tridimensionales, llamados diastereómeros. Durante décadas, los químicos han confiado en modelos sencillos —Felkin–Anh, Felkin–Anh polar, Cram y modelos de quelación— para predecir qué cara preferirá un reactivo. En compuestos carbonílicos α‑oxi, donde ese sustituyente vecino contiene oxígeno (como un éter o un éster), el oxígeno suele comportarse como una garra que atrapa reactivos metálicos. Esta «quelación» bloquea la molécula en una conformación y casi siempre conduce a los llamados productos sin (syn), donde los grupos alcohol recién formados quedan en el mismo lado de la cadena carbonada.
El problema antiguo con vecinos oxígenados
Aunque la vía por quelación resulta muy útil, también es limitante: sesga fuertemente las reacciones hacia productos sin y dificulta obtener la disposición opuesta, anti, donde los dos alcoholes apuntan a lados opuestos. Para aldehídos α‑oxi —moléculas en las que el carbono carbonílico está unido al menos a un hidrógeno— algunos trucos ingeniosos con reactivos de silicio especiales y ácidos de Lewis seleccionados han logrado producir productos anti. Pero para cetonas α‑oxi, que son menos reactivas y más comunes en objetivos complejos, el desafío es mayor. Los nucleófilos más fuertes tienden a ser más ácidos de Lewis, lo que a su vez favorece precisamente la quelación que el químico quiere evitar. Así, equilibrar «suficientemente reactivo» con «no demasiado adherente» al oxígeno ha sido un problema central sin resolver.
Un reactivo en forma de jaula que rompe la regla
Los autores introducen una nueva familia de reactivos llamados alilatránes, construidos alrededor de elementos del grupo 14 —silicio, germanio y estaño— retenidos en una estructura rígida tipo jaula. En estas moléculas, un átomo de nitrógeno interno alcanza a través de la jaula para enlazarse con el átomo central, creando un centro metálico altamente coordinado, casi encapsulado. Este diseño tiene dos efectos cruciales. Primero, aumenta la nucleofilicidad del fragmento alilo unido, haciéndolo predispuesto a formar un nuevo enlace carbono‑carbono. Segundo, domestica la acidez de Lewis del átomo central, de modo que tiene mucha menos tendencia a unirse fuertemente a los átomos de oxígeno del substrato. Cálculos cuánticos y datos de resonancia magnética nuclear confirman que la carga se localiza en el fragmento alilo mientras que la comunicación electrónica con el centro de silicio se reduce, lo que explica cómo el reactivo puede ser potente y, sin embargo, reacio a quelar.
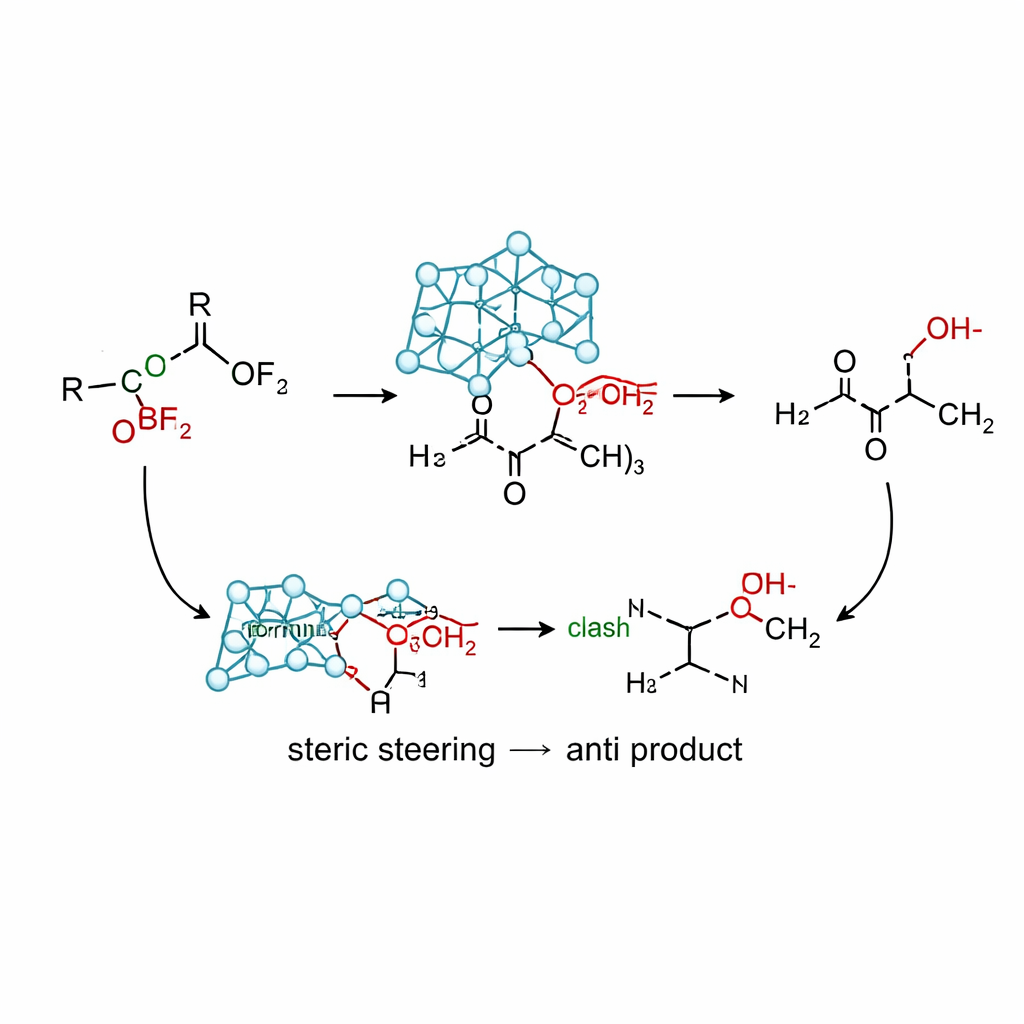
Cómo funciona la nueva reacción en la práctica
Usando la versión de silicio de este reactivo, el alilsilatrano, junto con un ácido de Lewis suave (trifluoruro de boro), el equipo desarrolló condiciones que proporcionan altos rendimientos de alcoholes homoalílicos anti a partir de una amplia gama de cetonas α‑oxi. Experimentos comparativos muestran que muchas fuentes alilo tradicionales —basadas en estaño, indio, magnesio, litio y silanos simples— o bien favorecen el producto sin, dan mezclas o se descomponen. En contraste, el alilsilatrano ofrece rutinariamente relaciones anti/sin por encima de 95:5 en sustratos que portan grupos metoxi, isopropoxi, fenoxi, acetoxi, silyloxi y aminoxi, así como diversos anillos aromáticos y cetonas cíclicas. Los cálculos sugieren una vía no por quelación en la que el voluminoso armazón atrane orienta el abordaje del grupo alilo hacia una conformación que recuerda el modelo de Cram: el sustituyente oxígeno queda opuesto al carbonilo mientras que la repulsión estérica entre la jaula y anillos fenilo próximos favorece la trayectoria que conduce al producto anti.
Implicaciones para la síntesis de fármacos y productos naturales
El método también funciona en sistemas cíclicos más rígidos, donde el volumen del alilsilatrano fomenta el ataque desde posiciones menos impedidas, y en derivados especializados que transfieren grupos alilo sustituidos con una selectividad anti igualmente alta. Dado que los anti‑1,2‑dioles resultantes con un fragmento homoalílico son motivos comunes en moléculas con actividad biológica, incluidos candidatos a moduladores enzimáticos, esta transformación ofrece a los químicos una vía fiable para acceder a variantes estructurales que antes requerían soluciones de varios pasos o eran sencillamente imprácticas. De forma importante, los mismos sustratos pueden dirigirse para dar productos sin o anti cambiando entre un sistema quelante a base de estaño y el nuevo sistema no quelante de silatrano, lo que otorga un control preciso sobre la forma molecular.
Qué significa esto en términos sencillos
En esencia, los investigadores han construido una herramienta inteligente de entrega de alilo que golpea el carbono diana desde el lado «menos favorecido» sin quedar atrapada por átomos de oxígeno cercanos. Al diseñar cuidadosamente una jaula alrededor del silicio, desacoplaron fuerza y adherencia: el reactivo es lo bastante potente para forjar un nuevo enlace pero no tan pegajoso como para atrapar átomos circundantes y arruinar la geometría deseada. Para los no especialistas, esto significa que los químicos disponen ahora de un mejor control para esculpir estructuras moleculares tridimensionales que sustentan muchos fármacos y productos naturales, ampliando el espacio de diseño para futuras medicinas y moléculas sintéticas complejas.
Cita: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Palabras clave: alilación estereoselectiva, cetonas alfa‑oxi, alilsilatrano, control no por quelación, alcoholes homoalílicos