Clear Sky Science · es
La región N-Myc MB0-MBI interacciona de forma específica y dinámica con el lóbulo N de la quinasa Aurora A
Por qué esto importa para el tratamiento del cáncer
Muchos cánceres infantiles agresivos dependen de una proteína llamada N-Myc para mantener el crecimiento de las células tumorales. N-Myc en sí es difícil de bloquear con fármacos porque se comporta más como un trozo flexible de espagueti que como una cerradura rígida en la que una llave pueda encajar. Este estudio revela, con un detalle sin precedentes, cómo N-Myc se une a otra proteína, la enzima Aurora quinasa A (AurA), para potenciar su actividad y ayudar a la supervivencia de las células cancerosas. Al cartografiar esta asociación, los investigadores descubren una vía realista para romperla con pequeñas moléculas.
Un alborotador flexible encuentra un socio sólido
N-Myc pertenece a la familia MYC de interruptores maestros que controlan el crecimiento celular, el metabolismo y la división. Cuando se producen en exceso, estos interruptores se convierten en potentes impulsores del cáncer, especialmente en tumores del sistema nervioso como el neuroblastoma de alto riesgo en niños. A diferencia de muchas enzimas o receptores, N-Myc no se pliega por sí mismo en una forma 3D fija; es una proteína “intrínsecamente desordenada” que se mueve y reconfigura constantemente. Esta flexibilidad la hace adaptable pero también notoriamente difícil de dirigir con fármacos. AurA, en contraste, es una enzima bien estructurada que ayuda a organizar la división celular. Trabajos previos mostraron que AurA contribuye a estabilizar N-Myc en células tumorales y que ambas proteínas interactúan físicamente, pero la naturaleza exacta y la importancia de los puntos de contacto seguían sin aclararse.
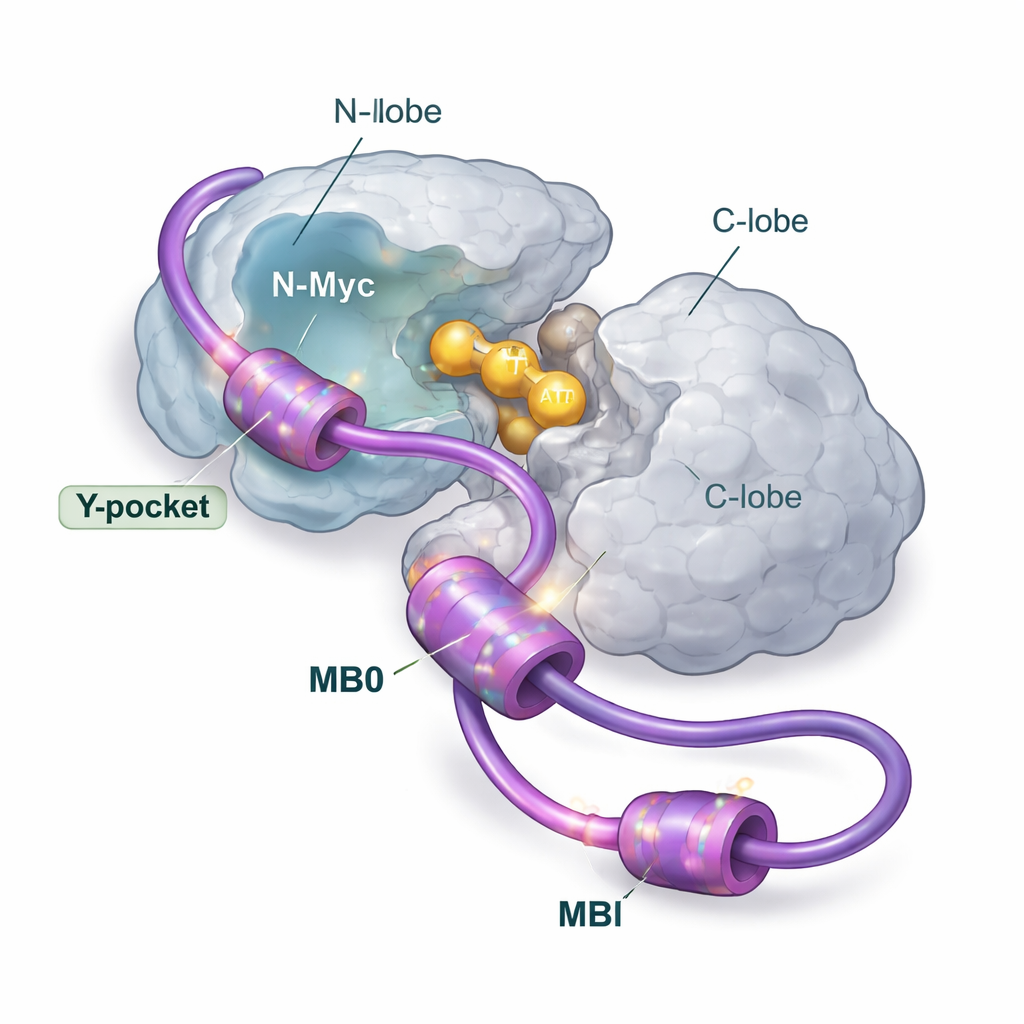
Múltiples puntos de agarre, una plataforma principal
Utilizando un amplio conjunto de métodos estructurales y biofísicos, incluyendo resonancia magnética nuclear, dispersión de rayos X, espectrometría de masas, calorimetría y modelado por ordenador, los autores desmenuzan cómo N-Myc y AurA se juntan en solución. Se centraron en el extremo frontal de N-Myc, que contiene dos regiones conservadas llamadas MB0 y MBI. Estos segmentos cortos son ricos en residuos aromáticos (como fenilalanina, tirosina y triptófano) que tienden a adherirse a bolsillos hidrofóbicos en proteínas compañeras. El equipo muestra que N-Myc se une a AurA principalmente en una proporción 1:1, con MB0 y MBI actuando como las zonas de contacto principales. Otro tramo de N-Myc que llamó la atención en estructuras cristalinas anteriores resulta desempeñar solo un papel secundario cuando está presente la región completa MB0–MBI.
Un apretón dinámico que activa la enzima
En lugar de encajar en una única pose rígida, N-Myc permanece en gran medida desordenada cuando se une a AurA. Los datos apuntan a un complejo “borroso”: varios segmentos de N-Myc se turnan para contactar diferentes parches en el lóbulo N de AurA, especialmente una hendidura conocida como el bolsillo Y y un bucle cercano que conecta señales con el sitio activo. A pesar de esta laxitud, el efecto es claro: la unión de MB0 y MBI estabiliza el lóbulo N de AurA y aumenta su actividad quinasa, es decir, mejora su capacidad para transferir grupos fosfato a sus dianas. Cuando los investigadores sustituyeron sistemáticamente residuos aromáticos clave en MB0 y MBI por alanina, el complejo N-Myc–AurA se debilitó, la enzima se estabilizó menos y su actividad cayó. Esto demuestra que anclas aromáticas específicas en la cadena por lo demás flexible de N-Myc son esenciales para activar AurA.
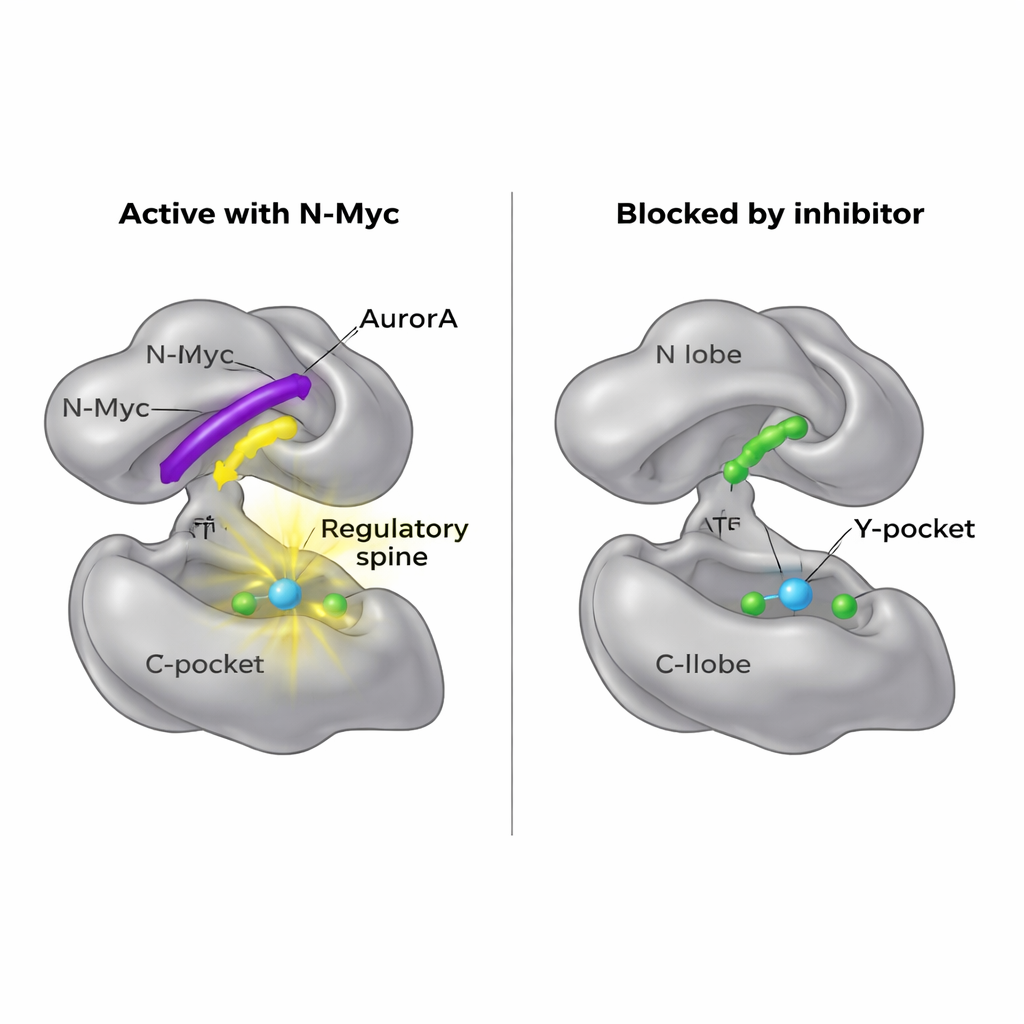
Abrir un nuevo punto de entrada para fármacos
Puesto que N-Myc en sí es difícil de atacar con fármacos, los investigadores se preguntaron si podrían bloquear en su lugar su sitio de acoplamiento en AurA. Sus mapas estructurales revelaron que MB0 y MBI ocupan la misma región general del lóbulo N que utiliza otra proteína asociada, TPX2, para activar AurA. Ya se conoce una pequeña molécula llamada AurkinA que se inserta en el bolsillo Y y desplaza a TPX2. En experimentos de unión, AurkinA compitió eficazmente con N-Myc por el lóbulo N de AurA, impidiendo que se adhirieran tanto los fragmentos N-Myc1–69 como N-Myc1–100. Este resultado demuestra que la superficie del lóbulo N, y especialmente el bolsillo Y, es un punto caliente farmacológicamente explotable que controla no solo reguladores clásicos como TPX2, sino también oncoproteínas desordenadas como N-Myc.
Qué significa esto para futuras terapias
Este trabajo replantea la asociación N-Myc–AurA como un abrazo dinámico de contactos múltiples centrado en el lóbulo N de AurA, en lugar de un único sitio de unión rígido. Para lectores no especializados, el mensaje clave es que incluso una proteína cancerígena amorfa como N-Myc puede abordarse indirectamente apuntando a un parche de acoplamiento sólido en su enzima compañera. Al mostrar que compuestos existentes que se unen al lóbulo N pueden desplazar a N-Myc de AurA, el estudio abre un camino claro hacia fármacos que interrumpan selectivamente esta interacción. Tales agentes podrían debilitar un soporte crítico para N-Myc en tumores infantiles de alto riesgo y, con desarrollo adicional, ofrecer una nueva vía terapéutica para cánceres considerados durante mucho tiempo “no farmacologables”.
Cita: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Palabras clave: N-Myc, Aurora quinasa A, proteínas intrínsecamente desordenadas, neuroblastoma, inhibidores de interacción proteína–proteína