Clear Sky Science · es
Promoción simultánea de la conversión fotocatalítica de CH4 y la producción de H2O2 mediante confinamiento de agua en nanoporos
Convertir un gas de efecto invernadero en líquidos útiles
El metano, el componente principal del gas natural, es a la vez un recurso valioso y un potente gas de efecto invernadero. Convertirlo de forma suave en productos químicos y combustibles líquidos podría ayudar a reducir las emisiones mientras se fabrican artículos cotidianos como disolventes y desinfectantes. Este estudio muestra una forma de emplear luz, agua y nanopartículas cuidadosamente diseñadas para transformar el metano en líquidos ricos en oxígeno y, al mismo tiempo, producir peróxido de hidrógeno, un desinfectante habitual y un oxidante ecológico.
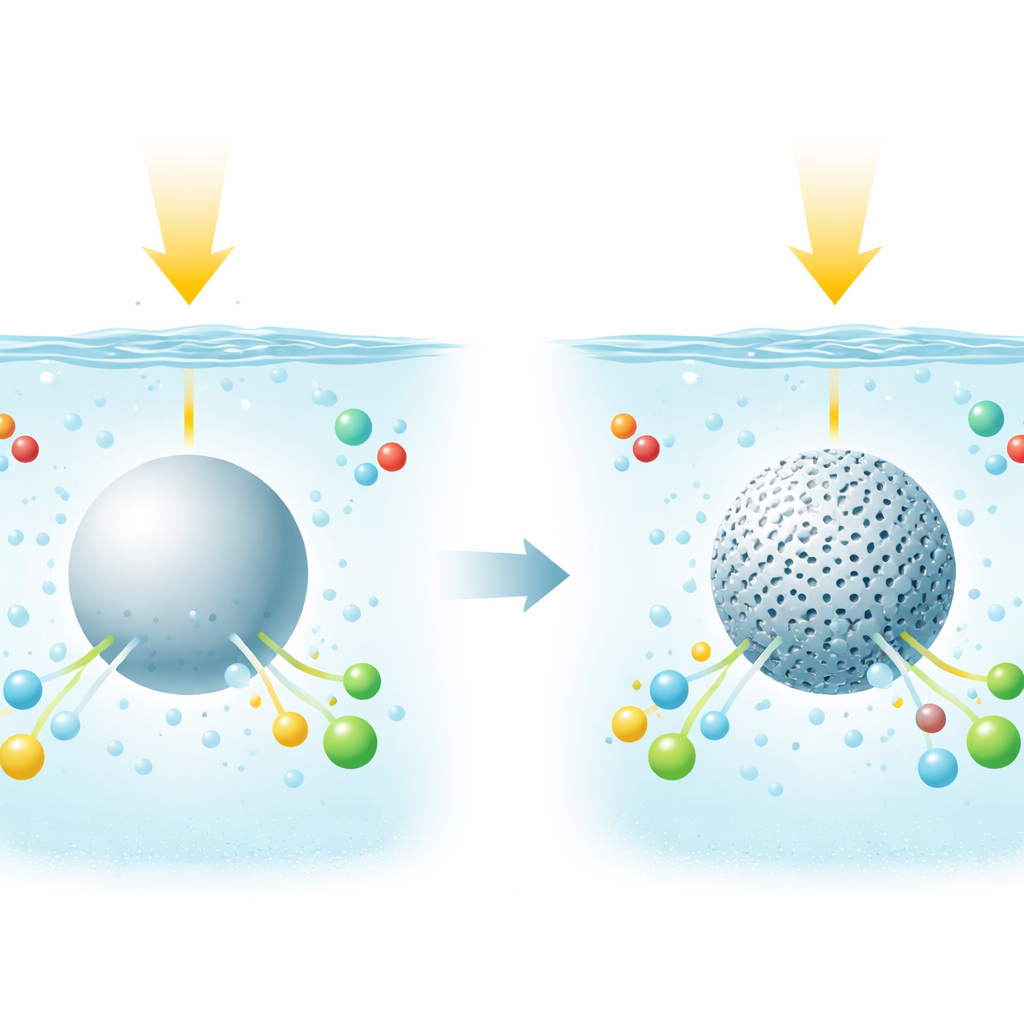
Por qué importa la estructura del agua
Muchas reacciones para energía limpia ocurren en agua, donde electrones y protones deben moverse coordinados en pasos estrechamente coreografiados. En el agua líquida corriente, las moléculas se mantienen en una red de enlaces de hidrógeno que cambia constantemente y que determina de forma silenciosa cuán fácilmente pueden desplazarse cargas y átomos. Los autores se preguntaron: ¿y si se comprimiera suavemente el agua en espacios diminutos para que esta red cambiara? ¿Facilitaría eso que los catalizadores excitados por luz guiaran el metano hacia los productos deseados en lugar de quemarlo completamente a dióxido de carbono?
Una jaula diminuta alrededor de un núcleo activo
Para probar esta idea, el equipo fabricó partículas núcleo–capa. En el centro hay un fotocatalizador bien conocido, dióxido de titanio decorado con pequeñas partículas metálicas como oro o platino. Alrededor de ese núcleo hicieron crecer una capa delgada de sílice transparente perforada con poros de escala nanométrica llenos de agua. Ajustando el tamaño de los poros hasta aproximadamente 1,7 nanómetros —apenas unos pocos diámetros de molécula de agua— crearon una capa de agua confinada abrazando la superficie del catalizador. Es importante que la absorción de luz y las propiedades básicas del catalizador permanecieran casi sin cambios; lo que varió fue cómo se acomodaba y movía el agua en estos diminutos canales.
De metano y oxígeno a líquidos y peróxido
Cuando estas partículas se iluminaron en agua bajo metano y oxígeno, el diseño con agua confinada mejoró el rendimiento de forma dramática. En comparación con el mismo catalizador sin la capa porosa, la conversión de metano se triplicó aproximadamente y la producción de peróxido de hidrógeno aumentó alrededor de veintidós veces. El proceso generó productos líquidos con oxígeno, como metanol y moléculas relacionadas, con alta selectividad, lo que significa mucha menos sobreoxidación desperdiciadora a dióxido de carbono. El efecto fue robusto: se mantuvo bajo distintas fuentes de luz, persistió a lo largo de muchos ciclos de reacción y pudo reproducirse usando otros metales e incluso otros núcleos semiconductores, lo que muestra que la estrategia es aplicable de forma amplia y no un truco puntual.
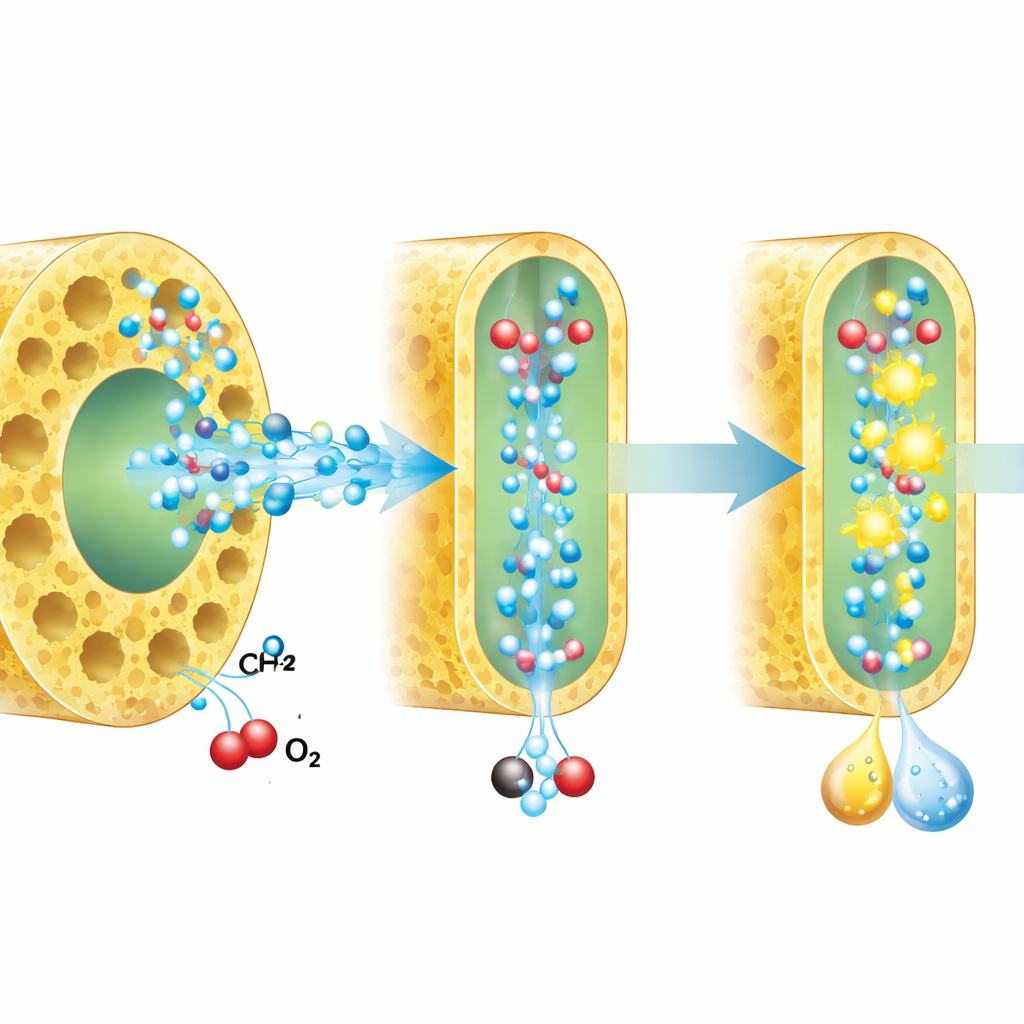
Cómo el agua comprimida cambia la vía de reacción
Para entender por qué el confinamiento ayuda, los investigadores combinaron mediciones espectroscópicas, experimentos de captura de radicales, etiquetado isotópico y simulaciones por ordenador. Encontraron que el agua confinada forma una red de enlaces de hidrógeno más débil y más lineal que el agua en volumen. En este entorno alterado, las especies reactivas clave —radicales con oxígeno de vida corta que atacan el metano— se generan con mayor eficiencia y permanecen más tiempo cerca de la superficie del catalizador. Al mismo tiempo, la vía de reducción del oxígeno se encamina hacia la producción directa de peróxido de hidrógeno en lugar de otros intermedios menos útiles. Estudios isotópicos, en los que el hidrógeno fue reemplazado por deuterio o se relabelaron átomos de oxígeno, confirmaron que el movimiento de protones pasa a ser más central en los pasos lentos y controlantes tanto de la oxidación del agua como de la reducción del oxígeno una vez que el agua está confinada.
Un nuevo control para una química más limpia
En términos cotidianos, la capa de sílice actúa como una esponja diseñada que obliga al agua a entrar en pasillos estrechos alrededor del catalizador activo, cambiando sutilmente cómo se organiza y cuán fácilmente pueden moverse protones y electrones. Este microambiente reorganizado facilita que las cargas excitadas por la luz fragmenten el metano en líquidos valiosos y transformen el oxígeno en peróxido de hidrógeno, en lugar de simplemente quemar el combustible. El trabajo sugiere que ajustar la "sensación" del agua cerca de superficies sólidas —sin cambiar el material activo en sí— podría convertirse en una herramienta de diseño poderosa para procesos químicos más limpios, desde la conversión de gases de efecto invernadero hasta la producción de oxidantes y combustibles verdes.
Cita: Lv, F., Wei, S., Wu, X. et al. Simultaneous promotion of photocatalytic CH4 conversion and H2O2 production via nanopore water confinement. Nat Commun 17, 2119 (2026). https://doi.org/10.1038/s41467-026-69719-z
Palabras clave: oxidación fotocatalítica del metano, catalizadores núcelo-capa nanoporosos, agua confinada, producción de peróxido de hidrógeno, transferencia de electrones acoplada a protones