Clear Sky Science · es
Un atlas humano espacialmente resuelto de glioblastoma revela patrones celulares y moleculares distintos en nichos anatómicos
Por qué importa este mapa del cáncer cerebral
El glioblastoma es uno de los cánceres cerebrales más letales, en parte porque cada tumor es un mosaico de distintos tipos celulares y microambientes. Las pruebas estándar y las imágenes suelen ver el tumor como una masa única. Este estudio construye un “atlas” de alta resolución que muestra dónde se localiza cada tipo celular importante dentro de los glioblastomas humanos, cómo se agrupan estos células en vecindarios distintos y cómo algunos de esos vecindarios podrían contribuir a la reaparición del tumor y a acortar la supervivencia de los pacientes.
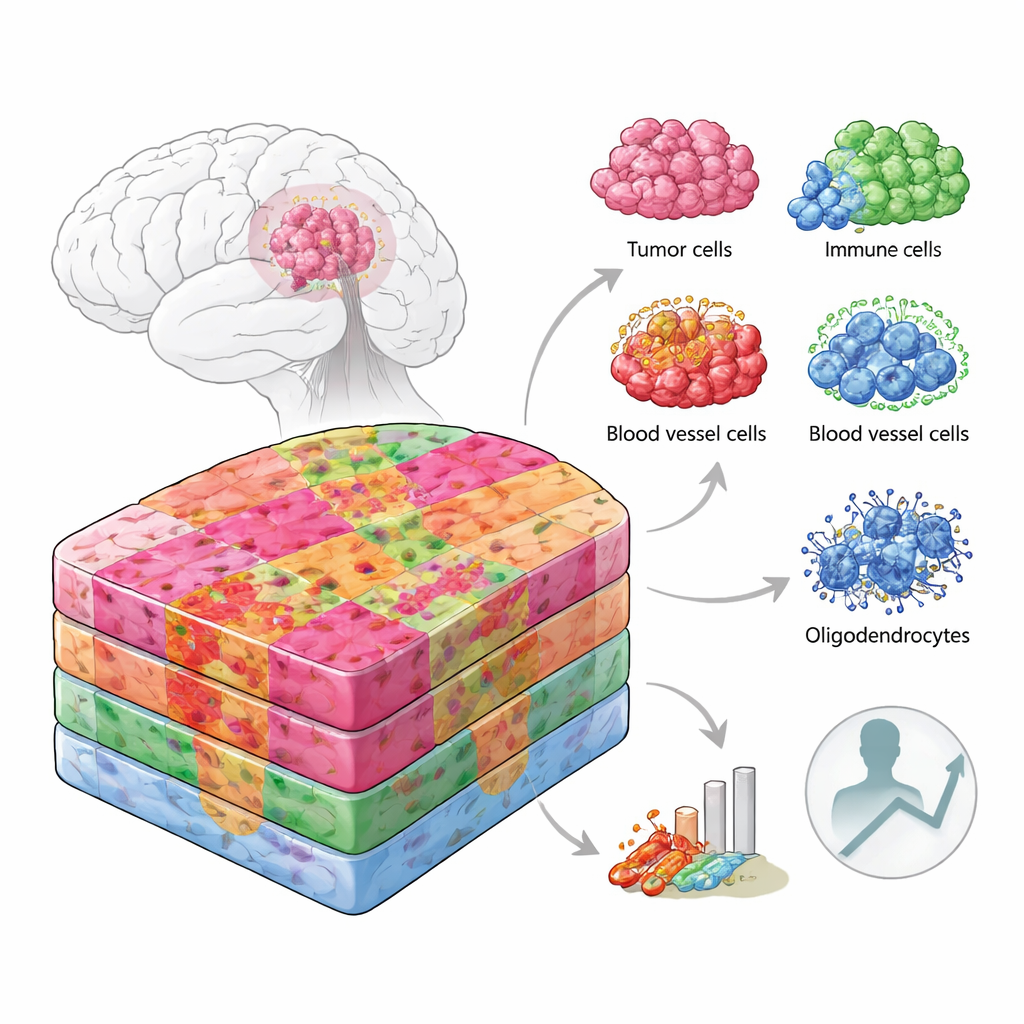
Mirar los tumores como mapas de ciudad
En lugar de tratar una lámina tumoral como uniforme, los investigadores la abordaron como un mapa urbano, en el que cada distrito tiene su propia distribución y habitantes. Combinaron varias técnicas de última generación que leen la actividad génica en miles de pequeñas ubicaciones a lo largo del tejido tumoral, y empataron esto con datos de una sola célula y mediciones de proteínas. Es importante que lo hicieron no solo en muestras congeladas frescas procedentes del quirófano, sino también en tejido hospitalario rutinario embebido en parafina, que es lo que la mayoría de los laboratorios de patología almacenan. En total analizaron más de 100.000 regiones con códigos espaciales y más de 220.000 células individuales de pacientes de diferentes edades y antecedentes genéticos, cubriendo tanto el núcleo denso del tumor como sus márgenes más difusos.
Vecindarios ocultos dentro del glioblastoma
Al superponer la actividad génica sobre imágenes microscópicas de alta magnificación, el equipo dividió cada tumor en “nichos” anatómicos, como el borde invasivo donde las células cancerosas infiltran el cerebro sano, las zonas centrales más densas, áreas ricas en vasos sanguíneos y regiones alrededor de tejido muerto o con falta de oxígeno. Cada nicho resultó albergar su propia mezcla de tipos celulares. El borde tumoral en sustancia gris era rico en neuronas y células de soporte típicas, mientras que el borde en sustancia blanca contenía muchos oligodendrocitos, las células que normalmente aíslan las fibras nerviosas. Ciertos nichos vasculares estaban repletos de células especializadas de los vasos y células de soporte, mientras que otros estaban dominados por células inmunitarias y tejido similar a una cicatriz. Las zonas hipóxicas próximas a tejido muerto contenían mayoritariamente células tumorales agresivas de tipo mesenquimal y macrófagos, con mucha menos diversidad celular.
Un papel sorprendente para las células de soporte
Uno de los hallazgos más llamativos involucra a los oligodendrocitos, normalmente considerados como silenciosos “aislantes” del cerebro. El atlas reveló cuatro estados distintos de oligodendrocitos, incluido un tipo hasta ahora poco apreciado que apareció casi exclusivamente en los núcleos de los glioblastomas. Estas células habían perdido muchos de sus genes relacionados con la mielina y, en cambio, activaron genes vinculados a la inflamación y al estrés, pareciéndose a oligodendrocitos asociados a enfermedad observados en la esclerosis múltiple y otros trastornos cerebrales. Espacialmente, esta población de oligodendrocitos con rasgos inmunes se agrupó en un “nicho inmuno‑glial” junto a microglía activada, macrófagos, células vasculares anormales y células tumorales de tipo mesenquimal, pero notablemente no en las regiones más privadas de oxígeno.
Vincular patrones microscópicos con el pronóstico del paciente
Los autores preguntaron luego si los programas génicos que definen estos estados de oligodendrocitos aparecen en grandes colecciones de muestras tumorales vinculadas a registros clínicos. En dos cohortes independientes de gliomas, una firma de oligodendrocitos convencionales productores de mielina se asoció con mejor supervivencia, incluso después de ajustar por edad y marcadores genéticos clave. En contraste, la firma de oligodendrocitos con activación inmune se correlacionó con peor supervivencia y fue más prominente en tumores agresivos y resistentes al tratamiento, especialmente en aquellos que habían recidivado tras la terapia y carecían de una alteración de metilación relacionada con la reparación del ADN. Esto sugiere que la reprogramación de los oligodendrocitos dentro del tumor, y su localización relativa frente a células tumorales e inmunitarias, puede influir en la respuesta a tratamientos y en la probabilidad de recaída.
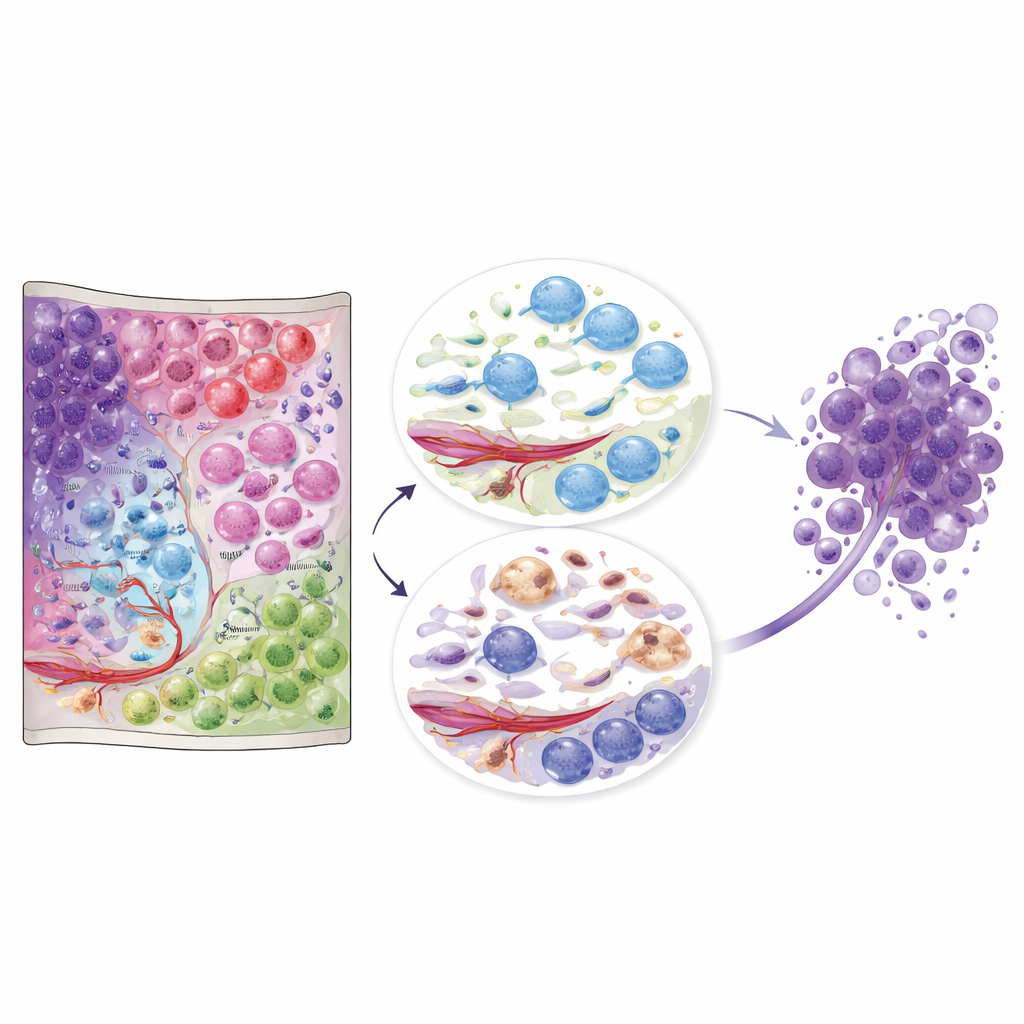
Lo que este atlas significa para la atención futura
En conjunto, estos datos transforman al glioblastoma de una masa borrosa a un paisaje detallado de comunidades celulares que interactúan. Para no especialistas, el mensaje clave es que la ubicación y los vecinos importan: los mismos tipos celulares generales se comportan de forma muy distinta según el nicho que ocupen. El atlas, disponible públicamente, ofrece una referencia que otros investigadores y clínicos pueden usar para situar sus propias muestras en este contexto espacial. A largo plazo, las terapias podrían diseñarse no solo para eliminar células tumorales, sino para desmantelar nichos nocivos —como regiones de cicatrización inmune o bolsillos de oligodendrocitos con activación inmune— que parecen favorecer la supervivencia tumoral y la recaída.
Cita: Sonpatki, P., Park, H.J., Xing, Y.L. et al. A spatially resolved human glioblastoma atlas reveals distinct cellular and molecular patterns of anatomical niches. Nat Commun 17, 2951 (2026). https://doi.org/10.1038/s41467-026-69716-2
Palabras clave: glioblastoma, transcriptómica espacial, microambiente tumoral, oligodendrocitos, atlas del cáncer cerebral