Clear Sky Science · es
Spatial perturb-seq: genómica funcional a nivel de célula única dentro de la arquitectura tisular intacta
Ver los genes en acción en circuitos cerebrales vivos
Muchas enfermedades cerebrales, desde el Alzheimer hasta el Parkinson, están vinculadas a genes de riesgo, pero todavía sabemos poco sobre cómo esos genes afectan a células individuales dentro del cerebro vivo. Este estudio presenta una manera potente de observar qué ocurre cuando genes específicos se apagan en células individuales, mientras esas células permanecen en sus vecindarios naturales dentro del tejido cerebral. El enfoque, llamado Spatial Perturb-Seq, ayuda a conectar el riesgo genético con la alteración del comportamiento celular y la comunicación entre células en el cerebro intacto.
Una nueva forma de probar muchos genes a la vez
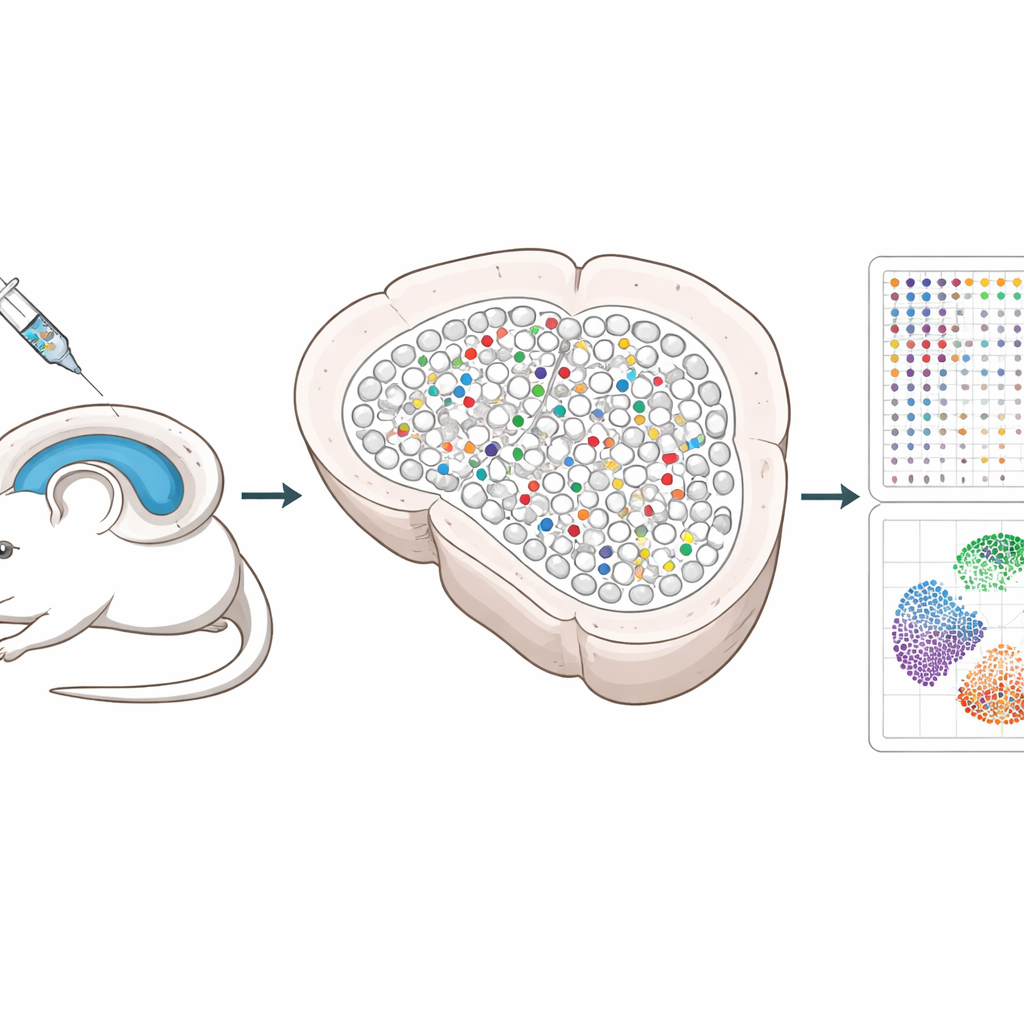
Los investigadores construyeron un sistema que usa herramientas de edición genética CRISPR entregadas por virus inofensivos al hipocampo, una región cerebral importante para la memoria. Cada virus lleva tres guías que desactivan un gen elegido, junto con un “código de barras” de ADN único y un marcador fluorescente para poder localizar las células editadas más tarde. Al mezclar estos virus e inyectarlos en dosis bajas, solo una pequeña fracción dispersa de células queda editada y la mayoría de las vecinas permanecen intactas. Este patrón escaso permite a los científicos separar los cambios que ocurren dentro de las células editadas de los que suceden en las células sanas cercanas.
Mantener intacto el mapa del cerebro
Los métodos tradicionales de célula única requieren disociar los tejidos, lo que destruye las posiciones precisas de las células e incluso puede perder neuronas frágiles. Spatial Perturb-Seq, en cambio, lee la actividad génica directamente de cortes finos de tejido cerebral, de modo que se preserva la ubicación de cada célula. Usando una tecnología llamada Stereo-seq, el equipo capturó perfiles completos de expresión génica de más de 200.000 células, además de leer los códigos de barras CRISPR y registrar las coordenadas de cada célula en el tejido. Luego emplearon algoritmos avanzados basados en imagen para delinear cada célula y herramientas computacionales para identificar tipos celulares y vecindarios locales, poniendo especial foco en las neuronas del hipocampo y sus contactos próximos.
Cómo las células editadas influyen en sus vecinas
Con el mapa tisular en mano, los científicos compararon neuronas editadas con neuronas no editadas y, por separado, con las vecinas no editadas que rodeaban a cada célula editada. Esto les permitió distinguir efectos «célula-autónomos» (dentro de la célula editada) de efectos «no célula-autónomos» (en el microambiente circundante). La eliminación de 18 genes diferentes, muchos vinculados al riesgo de enfermedades neurodegenerativas, produjo patrones distintos de cambios génicos dentro de las neuronas editadas. Algunas ediciones, como las dirigidas al gen Cfap410, también desencadenaron cambios fuertes en la actividad génica de las células cercanas, reflejando una alteración en la señalización local y el apoyo celular.
Pistas sobre vías de enfermedad neurodegenerativa
Varios genes ofrecieron ideas especialmente interesantes. Desactivar Lrrk2, un gen de riesgo principal para la enfermedad de Parkinson, provocó importantes cambios en las neuronas editadas, incluidos niveles reducidos de Bc1, una molécula de ARN importante para ajustar la producción de proteínas en las sinapsis. Al mismo tiempo, las células vecinas mostraron una expresión alterada de genes implicados en la estructura sináptica, el tráfico de proteínas y el manejo del calcio, lo que sugiere que los problemas vinculados a Lrrk2 se propagan por los circuitos locales. Eliminar otro gen, Srf, alteró una red de genes relacionados con el crecimiento neuronal y la plasticidad, y debilitó vías específicas de señalización ligando–receptor entre neuronas, lo que indica una comunicación célula a célula perturbada. Al puntuar sistemáticamente estos pares de señalización, el equipo pudo señalar qué rutas de comunicación se veían más afectadas para cada gen.
Herramientas flexibles para mapear efectos genéticos
Para mostrar que Spatial Perturb-Seq no está ligado a una sola plataforma, los investigadores también lo adaptaron a un sistema basado en imagen llamado Xenium. Allí, paneles de sondas predefinidos y sondas de códigos de barras personalizadas leen genes seleccionados y códigos de barras directamente en el tejido. Aunque este enfoque dirigido cubre menos genes que el Stereo-seq de transcriptoma completo, los patrones de cambios génicos para ediciones clave como Lrrk2 y Srf coincidieron bien entre ambos métodos y con un gran atlas cerebral externo. Esta verificación cruzada refuerza la solidez de los efectos observados sobre genes y vecindarios.
Qué significa esto para la investigación en salud cerebral
En términos cotidianos, Spatial Perturb-Seq permite a los científicos apagar muchos genes diferentes en células cerebrales individuales y luego observar cómo reaccionan esas células y sus vecinas inmediatas, todo mientras el diagrama de conexiones del tejido permanece intacto. Esto hace posible rastrear cómo los factores de riesgo genético perturban no solo células individuales sino también las conversaciones entre ellas, que son cruciales para el funcionamiento cerebral sano. Con el tiempo, a medida que la secuenciación se abarate y se realicen experimentos más amplios, este enfoque podría ayudar a revelar qué genes y circuitos locales son más importantes en las etapas tempranas de trastornos como Alzheimer, Parkinson y ELA, orientando estrategias de tratamiento más precisas.
Cita: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Palabras clave: genómica espacial, pantallas CRISPR, secuenciación de célula única, neurodegeneración, comunicación célula a célula