Clear Sky Science · es
Conversión eficiente de metanol en etilenglicol y glicolaldehído mediante síntesis divergente de acoplamiento C−C
Convertir un combustible sencillo en bloques de construcción útiles
El metanol, un alcohol simple que puede obtenerse a partir de dióxido de carbono, gas natural, carbón o biomasa, ya es un combustible y un químico clave. Este estudio muestra cómo haces de luz y nanomateriales cuidadosamente diseñados pueden transformar el metanol en moléculas más complejas y de mayor valor—mientras liberan simultáneamente hidrógeno como portador de energía limpio. El trabajo revela una nueva manera de dirigir un único material de partida hacia dos productos útiles distintos simplemente cambiando cómo se disponen átomos metálicos individuales sobre la superficie de un catalizador diminuto. 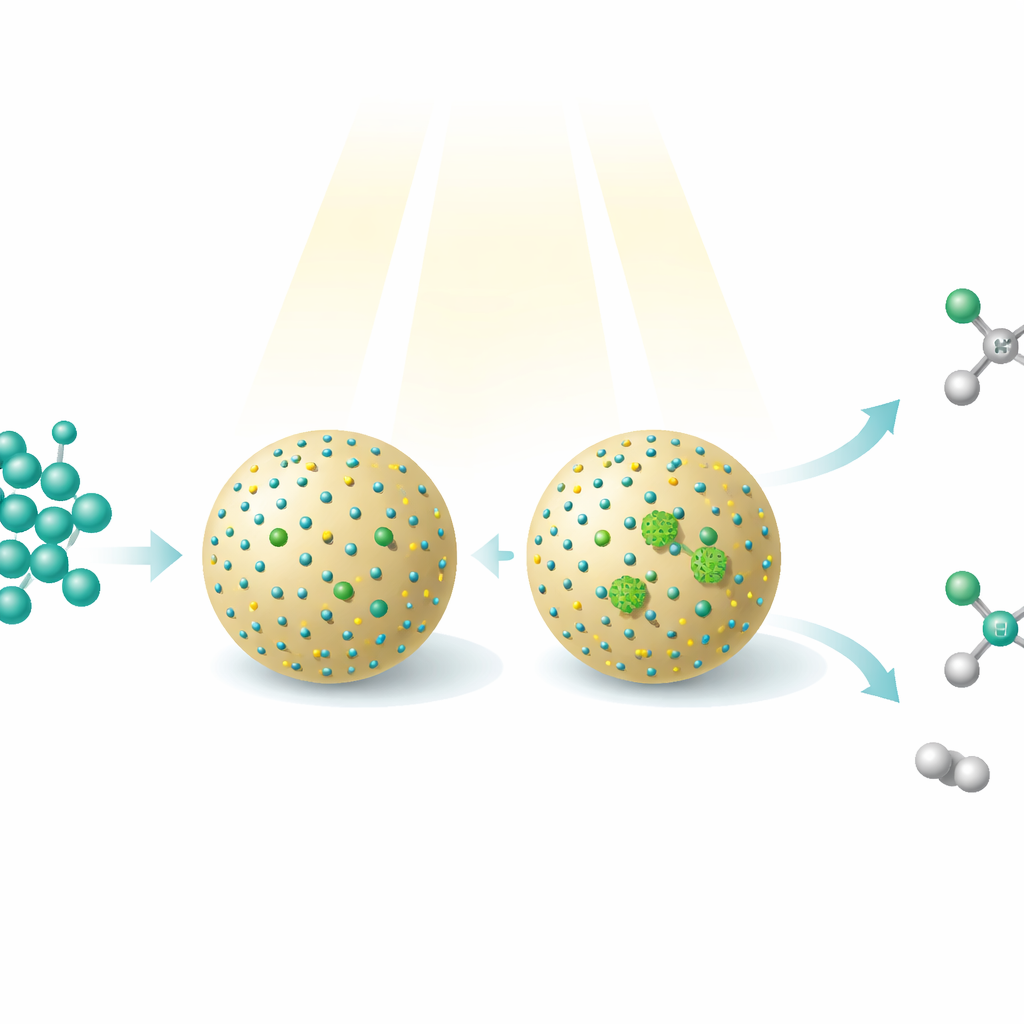
Por qué es importante mejorar el metanol
Mientras el mundo busca alternativas al petróleo, el metanol ha surgido como un líquido atractivo que puede almacenar energía y carbono. Sin embargo, la mayoría de los procesos industriales que convierten metanol en moléculas más grandes son herramientas poco precisas: requieren altas temperaturas, dependen de rutas de origen fósil y a menudo generan muchos subproductos no deseados. Los químicos quieren acoplar moléculas de metanol con alta precisión para poder fabricar selectivamente solo los compuestos deseados. Hacer esto en condiciones suaves usando luz en lugar de calor facilitaría la integración de la producción química con energía renovable.
Nanobolas activadas por luz hacen el trabajo
Los investigadores construyeron un fotocatalizador—literalmente un catalizador impulsado por la luz—decorando puntos cuánticos de sulfuro de cadmio sobre partículas esféricas de sílice. Estos puntos cuánticos absorben luz y generan electrones y huecos energéticos que pueden arrancar átomos de hidrógeno del metanol, formando fragmentos altamente reactivos. Luego se depositaron átomos de níquel sobre los puntos cuánticos de dos maneras distintas. En un material, el níquel existía mayoritariamente como átomos aislados; en el otro, el níquel formaba pequeños cúmulos de varios átomos. Aunque la composición global apenas cambiaba, esta sutil diferencia en la disposición del níquel alteró drásticamente qué reacciones tenían lugar en la superficie.
Dos diseños de níquel, dos productos limpios
Cuando el catalizador con átomos individuales de níquel se expuso a la luz en metanol, favoreció el emparejamiento de dos fragmentos idénticos derivados del metanol, conduciendo principalmente al etilenglicol—un diol de dos carbonos ampliamente usado en anticongelantes y plásticos. Esta vía alcanzó alrededor del 90% de selectividad, lo que significa que casi todo el metanol convertido terminó como este único producto, mientras que se producía gas hidrógeno en cantidades correspondientes a los átomos de hidrógeno arrancados. En contraste, el catalizador con cúmulos de níquel canalizó los mismos fragmentos de metanol por una ruta diferente. Aquí, una porción del metanol se oxidó más hasta formar un intermedio efímero similar a la formaldehído, que luego se combinó con otro fragmento para formar glicolaldehído, otro compuesto de dos carbonos con múltiples usos en productos químicos finos y potencialmente en procesos de origen biológico. Esta vía entregó glicolaldehído con un 96% de selectividad, nuevamente junto con hidrógeno. El soporte de sílice ayudó a que los puntos cuánticos captaran la luz de forma más eficiente y aumentó la robustez de las partículas a lo largo de muchos ciclos de uso. 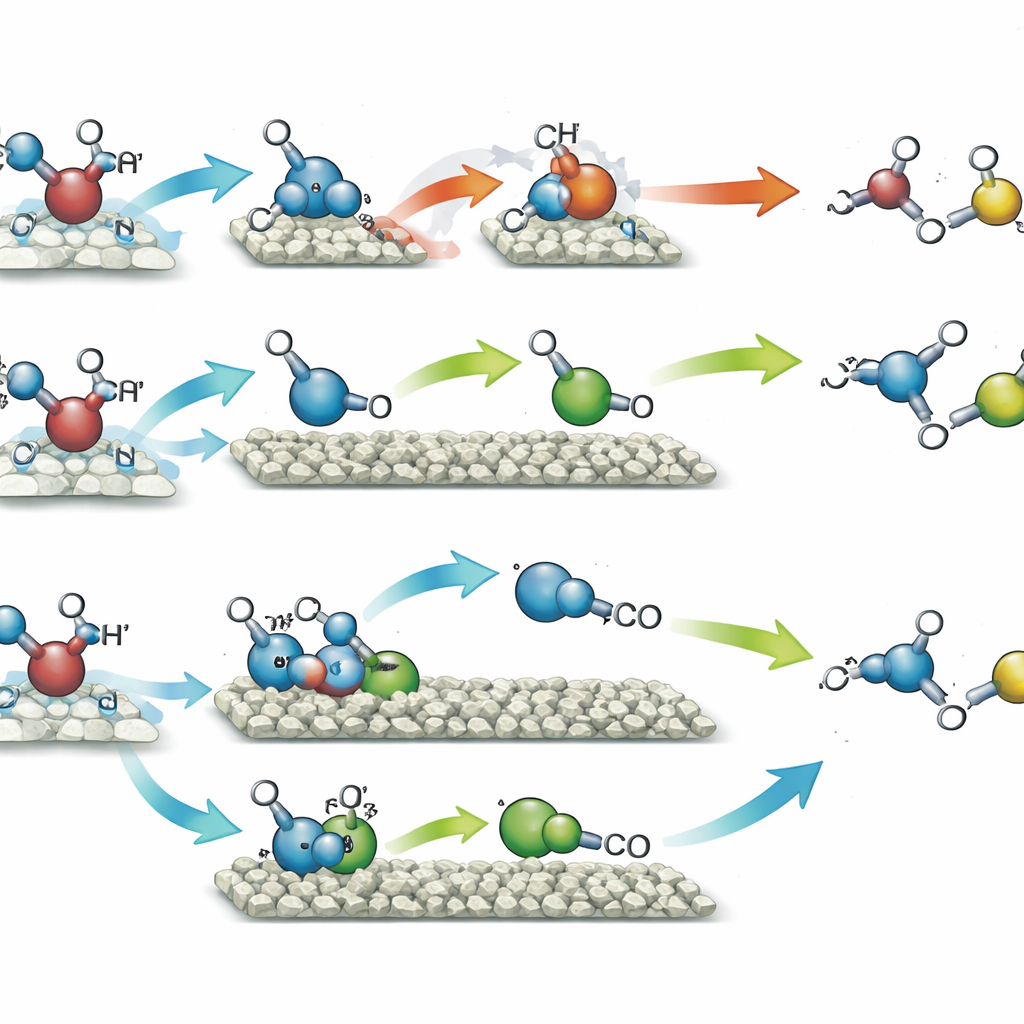
Mirando debajo del capó de la reacción
Para entender por qué las dos disposiciones de níquel se comportaban tan distinto, el equipo combinó una serie de mediciones avanzadas con simulaciones por ordenador. Experimentos de resonancia paramagnética electrónica mostraron que ambos catalizadores generaban radicales derivados del metanol bajo la luz, pero el catalizador con cúmulos promovía además la ruptura del enlace oxígeno–hidrógeno, dando lugar a fragmentos de reacción más diversos y al intermedio de tipo formaldehído. Pruebas resolvidas en el tiempo confirmaron que este intermedio aumentaba y luego disminuía en concentración a medida que se consumía para formar glicolaldehído. Cálculos cuántico-químicos trazaron los costes energéticos de cada pequeño paso. En los átomos individuales de níquel, el acoplamiento directo de dos radicales idénticos para formar etilenglicol fue la ruta más fácil. En los cúmulos de níquel, ese mismo acoplamiento retenía el producto con demasiada fuerza, dificultando su liberación, mientras que la vía que primero formaba el intermedio asimétrico y luego el glicolaldehído se volvió preferida desde el punto de vista energético.
Una nueva palanca para una química más limpia
En términos cotidianos, este trabajo muestra que el "dónde" se sitúa cada átomo de níquel en una superficie a escala nanométrica puede decidir "qué" molécula se obtiene del metanol cuando se ilumina con luz. Al cambiar entre átomos individuales y pequeños cúmulos de níquel, los investigadores pueden alternar el producto principal entre etilenglicol y glicolaldehído, ambos fabricados de forma eficiente y limpia junto con hidrógeno combustible. Esta estrategia de diseñar catalizadores átomo a átomo ofrece una ruta prometedora para convertir materias primas sencillas y renovables como el metanol en una gama de productos químicos útiles sin depender del petróleo, de condiciones agresivas o de reacciones secundarias derrochadoras.
Cita: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Palabras clave: valorización del metanol, fotocatálisis, átomos únicos de níquel, etilenglicol, glicolaldehído