Clear Sky Science · es
Las firmas de inclusión de exones permiten estimar con precisión la actividad de factores de splicing
Leyendo las marcas de edición ocultas de la célula
Cada célula de nuestro cuerpo edita constantemente sus mensajes de ARN antes de convertirlos en proteínas. Esta edición, llamada empalme, ayuda a decidir si una célula permanece sana o se vuelve cancerosa. El estudio detrás de este artículo muestra que, al observar con atención qué fragmentos de ARN se conservan o se omiten —denominados firmas de inclusión de exones—, los científicos pueden inferir con precisión la actividad de los “editores” moleculares que controlan el empalme, incluso en enfermedades complejas como el cáncer.
Cómo cortan y pegan las células sus mensajes
Los genes no se leen de una sola tirada continua. En lugar de ello, las células eliminan segmentos no codificantes y cosen entre sí las piezas codificantes, conocidas como exones, para construir los mensajes finales de ARN. Proteínas especializadas llamadas factores de empalme guían este proceso de cortar y pegar, decidiendo qué exones se incluyen. Su comportamiento está influido por muchas capas de regulación: cuánto ARN y proteína de ellos mismos se produce, cómo se modifican químicamente, dónde se localizan dentro de la célula y cómo interactúan con otras proteínas. Debido a que tantos factores pueden alterar la conducta de los factores de empalme, medir solo un tipo de dato —por ejemplo, la expresión génica— a menudo no revela lo que estos factores realmente están haciendo.
Convertir patrones de exones en lecturas de actividad
Inspirados por trabajos previos sobre factores de transcripción, los autores proponen una estrategia distinta: en lugar de intentar medir los factores de empalme directamente, leer su actividad a partir de sus efectos. Cuando un factor de empalme cambia, la inclusión de sus exones diana varía en patrones reconocibles. El equipo recopiló cientos de experimentos en los que factores de empalme individuales fueron silenciados, eliminados o sobreexpresados, y usó esos datos para construir “redes empíricas” que vinculan cada factor con los exones que claramente afectan. Luego adaptaron un marco computacional llamado VIPER para leer una nueva firma de inclusión de exones y puntuar cuán activo debe estar cada factor de empalme para explicar el patrón observado.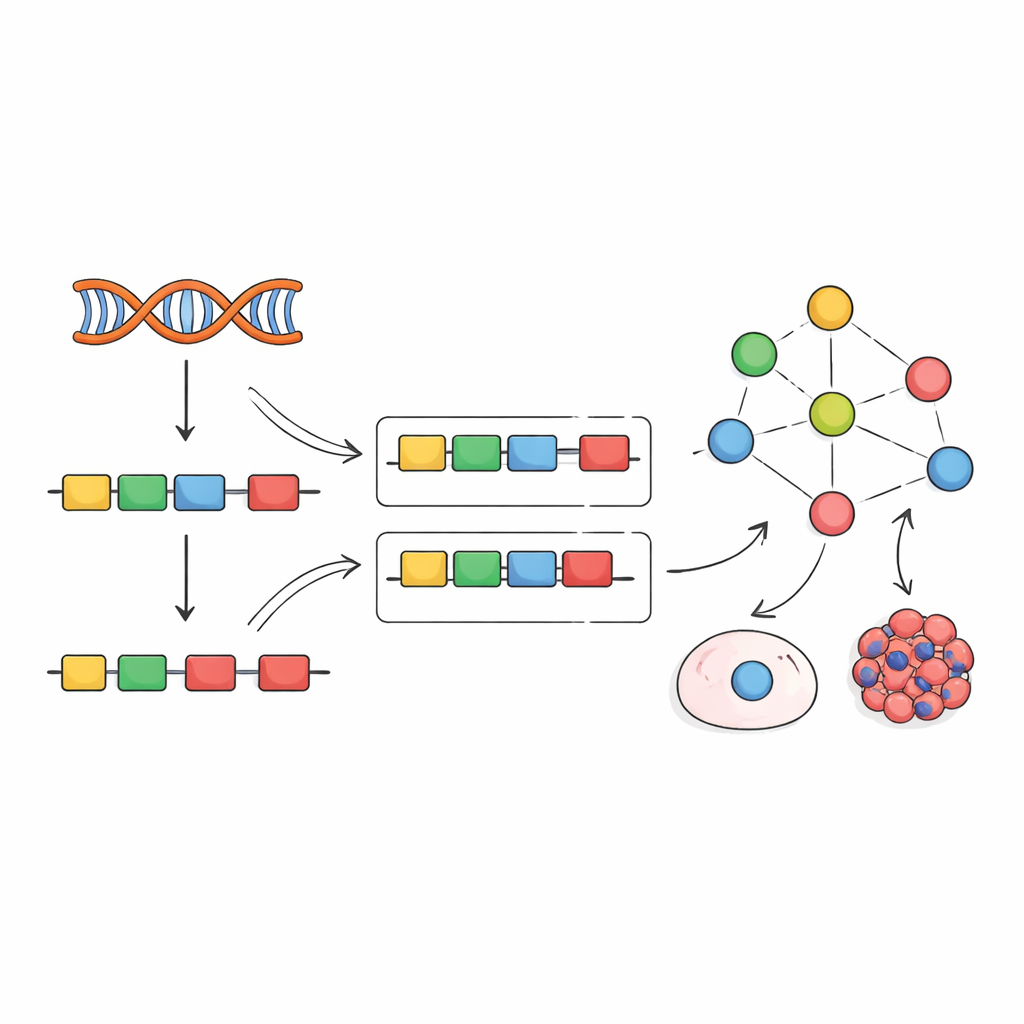
Probar el método en perturbaciones del mundo real
Para comprobar si este enfoque funciona, los investigadores compararon varias formas de construir redes y calcular puntuaciones de actividad. Las redes empíricas derivadas directamente de experimentos de perturbación, combinadas con el análisis de enriquecimiento de VIPER, superaron claramente a las alternativas basadas únicamente en inferencia estadística. El método identificó correctamente el factor de empalme perturbado experimentalmente en la mayoría de las pruebas, incluso entre distintos tipos celulares y estudios. También captó mecanismos regulatorios más sutiles. Por ejemplo, un fármaco contra el cáncer llamado Indisulam provoca la degradación de la proteína del factor de empalme RBM39 mientras que sus niveles de ARN aumentan en lo que parece un intento de compensación. El análisis tradicional de expresión induciría de forma engañosa la idea de que RBM39 está más activo, pero la puntuación de actividad basada en exones reveló correctamente una fuerte pérdida de función, coincidiendo con la acción conocida del fármaco.
Descubrir programas de empalme ocultos en el cáncer
Con esta herramienta, los autores analizaron los datos de The Cancer Genome Atlas a nivel de exón de múltiples tipos tumorales y tejidos sanos correspondientes. Descubrieron dos programas amplios y recurrentes de empalme. Un programa consiste en factores de empalme que tienden a estar más activos en tumores y se asocian con una peor supervivencia de los pacientes —un programa con rasgos oncogénicos—. El otro presenta factores sistemáticamente menos activos en tumores y vinculados a mejores resultados, asemejándose a supresores tumorales. Estos programas afectan a genes involucrados en características fundamentales del cáncer, como la división celular acelerada y la capacidad de los tumores para ocultarse del sistema inmunitario. Por ejemplo, algunos exones regulados por el programa similar a supresor tumoral parecen influir en la respuesta de los pacientes a terapias de bloqueo de puntos de control inmunitario, lo que señala nuevos marcadores o puntos de intervención.
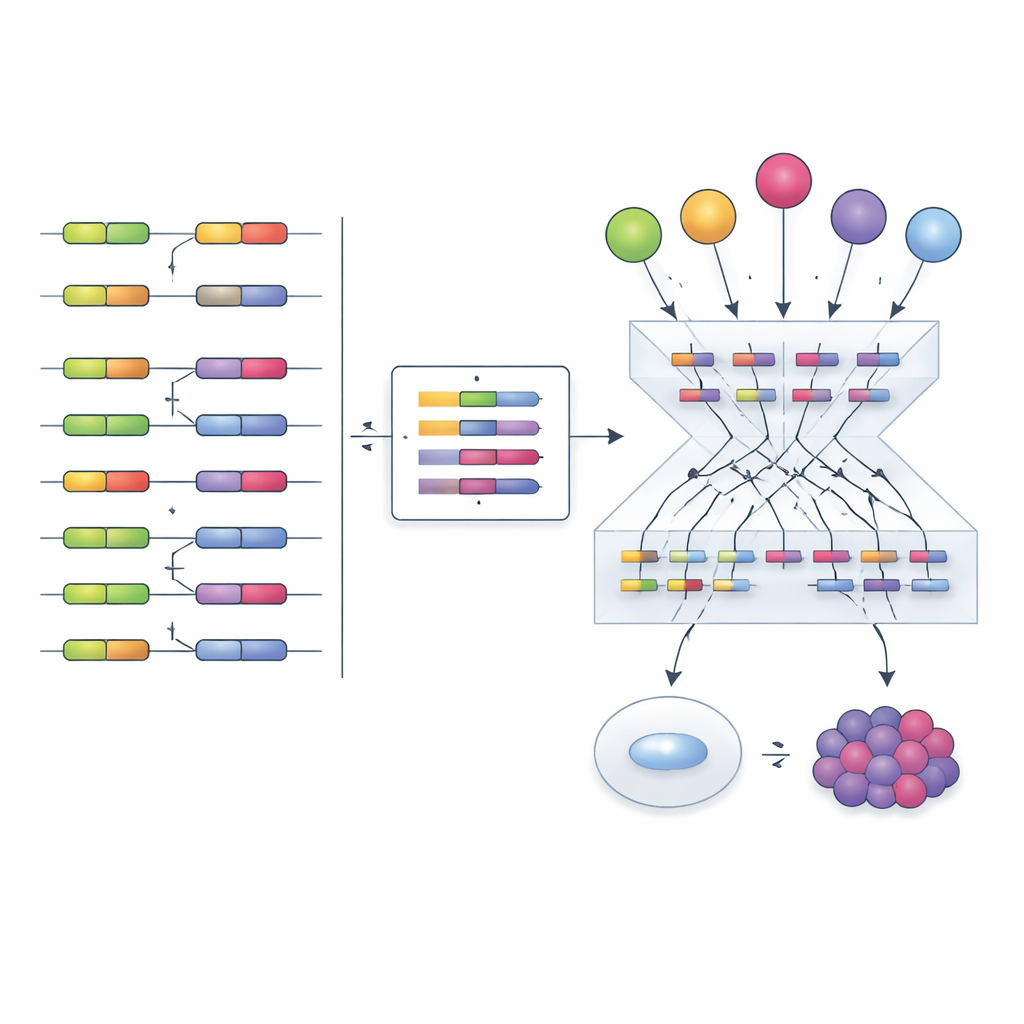
Seguir los cambios de empalme en el camino hacia el cáncer
El equipo también examinó un modelo paso a paso de células humanas que progresan de normales a inmortalizadas, formadoras de tumores y, finalmente, metastásicas. Encontraron que el programa con rasgos oncogénicos se vuelve más activo a medida que las células adquieren mutaciones que impulsan el cáncer, mientras que el programa similar a supresor tumoral se atenúa. Al integrar múltiples capas de datos —niveles de ARN, abundancia proteica, modificaciones químicas y cambios de empalme dentro de los factores de empalme mismos— identificaron un conjunto focalizado de eventos moleculares candidatos que podrían impulsar estos cambios de programa, ofreciendo una lista priorizada para futuras pruebas experimentales.
Por qué esto importa para pacientes e investigación futura
En esencia, el estudio muestra que el comportamiento complejo de los factores de empalme puede destilarse en una única puntuación de actividad interpretable derivada de cómo se incluyen u omiten los exones. Esto hace posible estudiar la regulación del empalme en grandes cohortes de pacientes y en experimentos diversos usando únicamente datos estándar de secuenciación de ARN, sin requerir costosos perfiles multiómicos. Para el lector no especializado, el mensaje clave es que los patrones en cómo se cortan y pegan los genes contienen información rica sobre los sistemas de control ocultos de la célula, y que decodificar esos patrones puede revelar nuevos impulsores del cáncer, mejorar el pronóstico y guiar la búsqueda de tratamientos más precisos.
Cita: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Palabras clave: Empalme de ARN, factores de empalme, genómica del cáncer, transcriptómica, inferencia de actividad proteica