Clear Sky Science · es
Ingeniería genética del microambiente tumoral inducida por LOAd703 en combinación con atezolizumab en melanoma maligno metastásico: un ensayo de fase I/II
Por qué importa este nuevo estudio sobre melanoma
Para las personas con melanoma cutáneo avanzado que ya no responde a las potentes inmunoterapias actuales, las opciones de tratamiento son limitadas y con frecuencia duras. Este estudio pone a prueba una idea distinta: usar un virus modificado genéticamente inyectado directamente en los tumores, junto con un fármaco inmunoestimulador ya disponible, para reactivar las defensas del organismo y recuperar el control sobre el cáncer. Los resultados preliminares sugieren que este enfoque puede administrarse con seguridad y podría ayudar a una proporción relevante de pacientes cuya enfermedad había resistido los cuidados estándar.
Un cáncer cutáneo persistente que elude el tratamiento
El melanoma es uno de los cánceres cutáneos graves más frecuentes en los países occidentales, y su incidencia ha aumentado con fuerza en las últimas décadas. Los fármacos modernos que inhiben puntos de control inmunitarios—que liberan el freno sobre las células T—han transformado los resultados, elevando la supervivencia a cinco años en el melanoma avanzado a cerca de la mitad de los pacientes. Sin embargo, muchos tumores acaban dejando de responder. Con frecuencia, estos cánceres resistentes están rodeados por un vecindario “frío” de células y moléculas que impiden la entrada de células inmunitarias o las desactivan. Encontrar formas de reconectar este microambiente tumoral para que las células T vuelvan a reconocer y atacar el cáncer es una prioridad importante en la investigación.
Un virus diseñado para reconfigurar el entorno tumoral
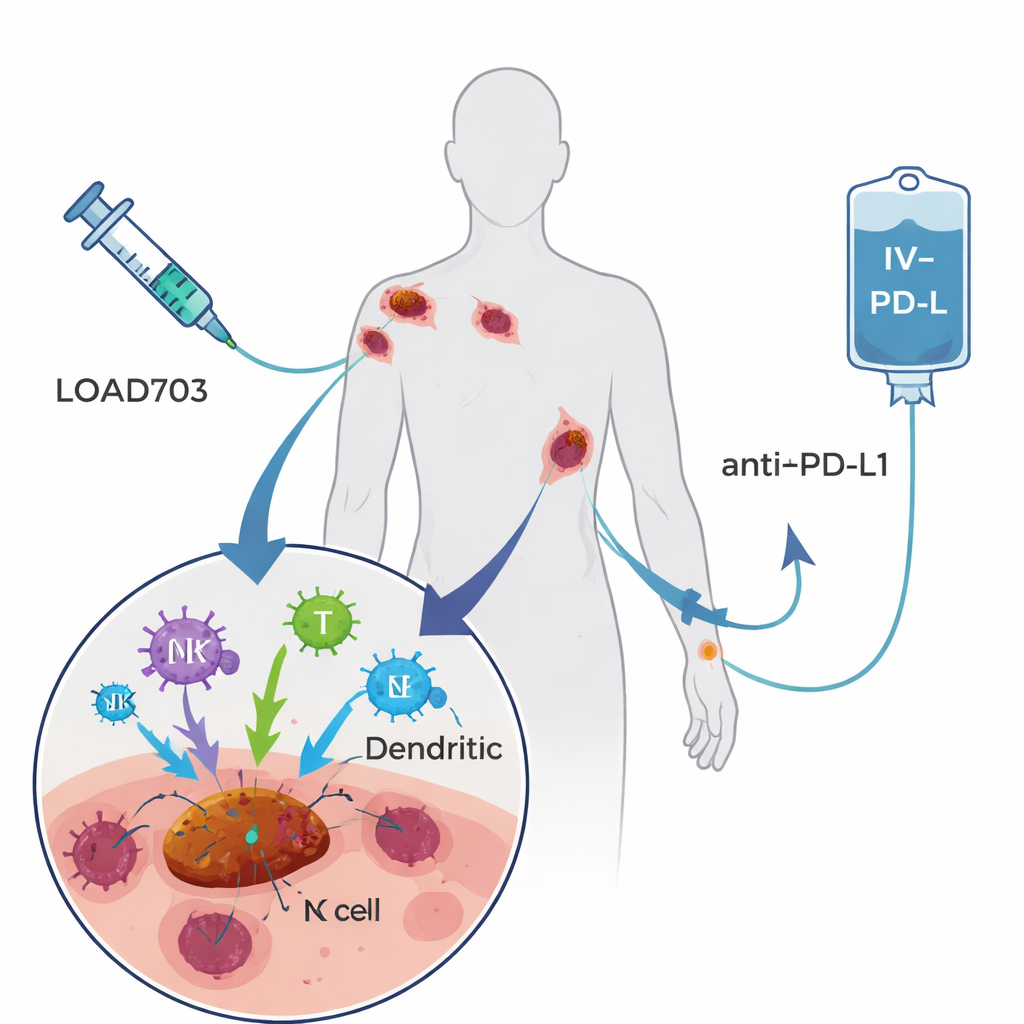
El tratamiento evaluado aquí, denominado LOAd703, es un adenovirus modificado—un tipo de virus del resfriado común—diseñado para cumplir dos funciones. Primero, tiene preferencia por replicarse en y destruir células tumorales, una estrategia conocida como viroterapia oncolítica. Segundo, transporta instrucciones genéticas para dos potentes señales inmunoestimuladoras expresadas en las células infectadas. Estas señales, CD40L y 4‑1BBL, ayudan a que las células centinela profesionales del sistema inmunitario (células dendríticas) maduren y presenten fragmentos tumorales, y refuerzan y expanden las células T y las células asesinas naturales (NK) que combaten el cáncer. Los pacientes en el ensayo recibieron LOAd703 inyectado directamente en uno o varios tumores cada tres semanas, junto con atezolizumab, un anticuerpo establecido administrado por vía intravenosa que bloquea el freno PD‑L1 en las células T. La esperanza era que el virus convirtiera los tumores en fábricas de vacuna dentro del cuerpo, mientras que el anticuerpo mantenía activas a las células T reanimadas.
Quién fue tratado y cómo les fue
El ensayo de fase I/II incluyó a 24 personas con melanoma en estadio IV que había progresado claramente a pesar de al menos un tratamiento previo bloqueador de PD‑1; muchos habían recibido varias líneas de inmunoterapia y fármacos dirigidos. Se probaron dos niveles de dosis del virus. En general, la combinación fue bien tolerada. Los efectos secundarios más comunes relacionados con el virus—fiebre, escalofríos, náuseas y síntomas tipo gripe—fueron en su mayoría leves y temporales. Solo dos pacientes experimentaron reacciones más graves pero reversibles en la dosis más alta, y nadie tuvo que interrumpir el tratamiento por problemas relacionados con el virus. Cuando los investigadores evaluaron las respuestas tumorales, cuatro pacientes (17%) presentaron reducción medible de sus tumores, y más de la mitad mantuvo al menos enfermedad estable durante algún tiempo. A los dos años tras entrar en el estudio, casi la mitad de los participantes seguía con vida, incluidos algunos cuyas pruebas de imagen mostraron control duradero o desaparición completa de enfermedad detectable después de finalizar la terapia.
Señales de que el sistema inmunitario se reactivó
Para ver qué ocurría dentro de los tumores y en la sangre, el equipo analizó biopsias tisulares y muestras de sangre tomadas antes del tratamiento y alrededor de nueve semanas después de iniciado. En los tumores inyectados observaron una mayor actividad de genes vinculados a respuestas inmunitarias tipo 1, incluidos marcadores de células T y células NK activadas, y moléculas que ayudan a estas células a entrar en los tumores desde los vasos sanguíneos cercanos. También aumentaron las señales asociadas con la presentación de antígenos—el proceso por el cual los fragmentos tumorales se muestran a las células T—lo que sugiere que la terapia viral estaba transformando el microambiente tumoral de supresor a más favorable para la inmunidad. En sangre, varias proteínas relacionadas con la inmunidad, incluido el propio PD‑L1, aumentaron tras la terapia, coherente con una activación amplia de vías inmunitarias. Los pacientes con supervivencia más prolongada tendían a mostrar patrones génicos ligados a una función robusta de células T y protección antiviral, mientras que aquellos con supervivencia más corta mostraban patrones asociados con tipos celulares supresores y señales de remodelado tisular.
Qué podría significar esto para la atención futura
Este fue un estudio pequeño, de un solo brazo y sin grupo de comparación, por lo que sus cifras de supervivencia y respuesta deben interpretarse con prudencia. Aun así, la combinación de buena tolerabilidad, activación inmune en los tumores y un control de la enfermedad alentador en pacientes muy previamente tratados sugiere que virus oncolíticos modificados genéticamente como LOAd703 podrían ayudar a re‑sensibilizar el melanoma al bloqueo de puntos de control—o incluso mantener los tumores bajo control por sí solos. Los resultados respaldan ensayos más amplios y controlados, posiblemente combinando el virus con fármacos adicionales que apunten al sistema inmune, para aclarar qué pacientes se benefician más y cómo integrar mejor esta estrategia en el tratamiento del melanoma.
Cita: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Palabras clave: melanoma, inmunoterapia, virus oncolítico, microambiente tumoral, resistencia a inhibidores de puntos de control