Clear Sky Science · es
Detección masivamente paralela basada en nanoporo para el perfilado de péptidos e identificación de proteínas
Leer proteínas molécula a molécula
Las proteínas son las encargadas del trabajo en nuestras células, y saber exactamente cuáles están presentes, cómo se modifican y cómo interactúan es fundamental para comprender la salud y la enfermedad. Las herramientas actuales para estudiar proteínas son potentes, pero con frecuencia son lentas, caras y difíciles de escalar. Este artículo describe una nueva manera de “escuchar” fragmentos individuales de proteína a medida que pasan por un pequeño orificio en una membrana, usando inteligencia artificial para convertir esas señales en huellas detalladas. El enfoque podría abrir la puerta a pruebas más rápidas y económicas para seguir marcadores de enfermedad y comprobar hasta qué punto los anticuerpos de investigación y diagnóstico funcionan realmente.
Convertir las proteínas en piezas legibles
Los investigadores se basan en la tecnología de nanoporos, desarrollada originalmente para la secuenciación de ADN. En su sistema, las proteínas naturales se cortan primero en fragmentos más cortos llamados péptidos y se modifican suavemente para que cada pieza pueda enlazarse por ambos extremos a cortos tramos de ADN. Esto crea una estructura “Oligo–Péptido–Oligo” que se comporta bien en dispositivos de nanoporo diseñados originalmente para ADN. El equipo usa una enzima de corte específica que tiende a dejar un aminoácido particular, la lisina, al final de cada fragmento, lo que hace la química más predecible y compatible con muchas proteínas diferentes. El resultado final es una biblioteca purificada de muchos de estos constructos péptido–ADN preparada en solo unas horas.
Escuchar con muchos nanoporos a la vez
Para detectar realmente estos fragmentos de péptido, los autores usan una matriz de nanoporos biológicos —pequeños orificios fabricados por proteínas insertados en una membrana y conectados a electrodos. Cuando se aplica una tensión, las estructuras ADN–péptido–ADN son arrastradas, una a una, a través de cada poro por un motor molecular. A medida que el péptido pasa por la parte más estrecha, bloquea parcialmente el flujo de iones y cambia la corriente eléctrica. Debido a que la plataforma usa 256 poros en paralelo y puede recoger más de 100.000 de estos eventos a partir de una sola biblioteca en menos de dos horas, produce un flujo masivo de señales de una sola molécula que capturan cómo cada péptido específico interactúa con el poro. 
De señales ruidosas a huellas distintivas
A simple vista, estos trazados de corriente parecen ruidosos y variables; el mismo péptido puede entrar en distintas orientaciones y adoptar diferentes conformaciones. Las medidas resumen tradicionales, como la corriente media y la duración del evento, a menudo se solapan entre péptidos similares. El avance clave de este trabajo es una canalización de inteligencia artificial en dos pasos. Primero, una red neuronal convolucional profunda se entrena con gran número de trazados para clasificar qué péptido produjo cada patrón. Segundo, el equipo crea “matrices de densidad” que resumen cómo tiende a variar la señal a lo largo de cada evento, convirtiendo esencialmente nubes de trazados ruidosos en huellas 2D estables. Solo se conservan las lecturas cuyos patrones temporales detallados coinciden con estas huellas. Esta estrategia de CNN más huella aumenta la precisión hasta alrededor del 99 % para péptidos de prueba y puede distinguir de forma fiable fragmentos que difieren en un solo aminoácido, ciertos isómeros y muchas modificaciones químicas comunes que las proteínas adquieren en las células.
Comprobar anticuerpos y localizar proteínas completas
Dado que los anticuerpos reconocen tramos cortos de proteínas, los autores aplican su plataforma para mapear qué fragmentos reconocen realmente diversos anticuerpos comerciales. Mezclando péptidos superpuestos de un precursor hormonal, enriqueciendo los fragmentos retenidos por cada anticuerpo y leyéndolos con el sistema de nanoporo, pueden identificar regiones de unión preferidas y mostrar cuándo pares de anticuerpos recomendados por el proveedor reconocen el mismo sitio y, por tanto, están mal emparejados para ensayos tipo sándwich. En otra prueba, examinan una secuencia de etiqueta bien conocida y cuatro variantes casi idénticas, mostrando que el número relativo de lecturas por nanoporo para cada péptido sigue de cerca la fuerza de unión del anticuerpo, coherente con mediciones más laboriosas basadas en superficie. Finalmente, demuestran la identificación de proteínas: entrenan el sistema con huellas de péptidos de tres proteínas humanas, luego digieren a ciegas las proteínas completas y muestran que el patrón combinado de péptidos clasificados es suficiente para identificar correctamente qué proteína es cuál, incluso con algunos fragmentos ambiguos o ausentes. 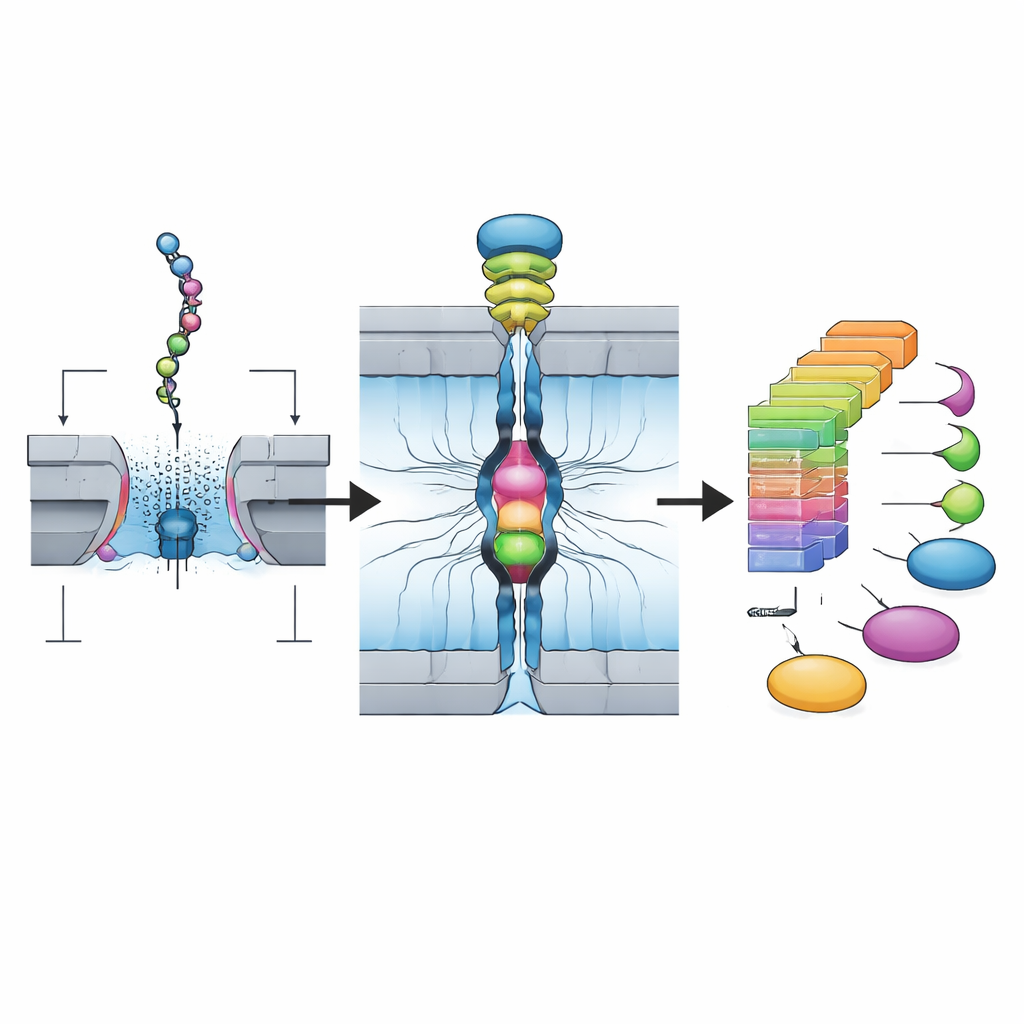
Por qué esto importa para las pruebas futuras
En términos sencillos, el estudio muestra que un secuenciador de nanoporos al estilo del ADN, combinado con química ingeniosa e IA, puede actuar como un “estetoscopio” altamente paralelo para fragmentos proteicos. En lugar de tener que leer cada aminoácido en orden, el sistema se apoya en ricas huellas estadísticas procedentes de miles de eventos de una sola molécula para distinguir diferencias sutiles de carga, tamaño y modificación. Esto permite comprobaciones rápidas y de bajo coste de la calidad de anticuerpos y ofrece un camino hacia el reconocimiento de proteínas completas a partir de sus patrones de péptidos. Aunque aún existen límites —como dificultades con ciertos tipos de péptidos y la necesidad de buenos datos de entrenamiento—, el trabajo describe una canalización de extremo a extremo que podría ayudar a acercar el análisis de proteínas de alto rendimiento a los laboratorios de investigación cotidianos y, eventualmente, a la práctica diagnóstica clínica.
Cita: Wang, J., Chen, J., Pan, H. et al. Nanopore-based massively parallel sensing for peptide profiling and protein identification. Nat Commun 17, 3058 (2026). https://doi.org/10.1038/s41467-026-69628-1
Palabras clave: detección por nanoporo, proteómica, huella de péptidos, validación de anticuerpos, identificación de proteínas