Clear Sky Science · es
Fármacos enjaulados permiten la desprotección foto-catalítica simultánea de óxido nítrico y anestésicos para analgesia antibacteriana
Combatir gérmenes y dolor al mismo tiempo
Las infecciones bacterianas no solo amenazan nuestra salud; también causan mucho dolor. Los tratamientos habituales suelen centrarse en los gérmenes y dejan a los pacientes dependiendo de analgésicos aparte, que pueden perder efecto rápidamente o provocar efectos secundarios. Este estudio presenta un medicamento controlado por luz que pretende matar bacterias y aliviar el dolor en un único paso coordinado, ofreciendo una visión de cuidados infecciosos más inteligentes y cómodos.
La idea de un medicamento dos en uno
Los investigadores basaron su enfoque en la tetracaína, un anestésico local conocido que se usa para adormecer piel y nervios. Unieron químicamente óxido nítrico, una pequeña molécula gaseosa con potentes acciones antibacterianas y antiinflamatorias, a la tetracaína. Así crearon un “profármaco” llamado TTC-NO que es mayormente inactivo hasta que se activa. El TTC-NO se encapsuló junto con una molécula auxiliar fotosensible en pequeñas burbujas poliméricas llamadas micelas que pueden desplazarse en medios acuosos como la sangre o el fluido tisular. 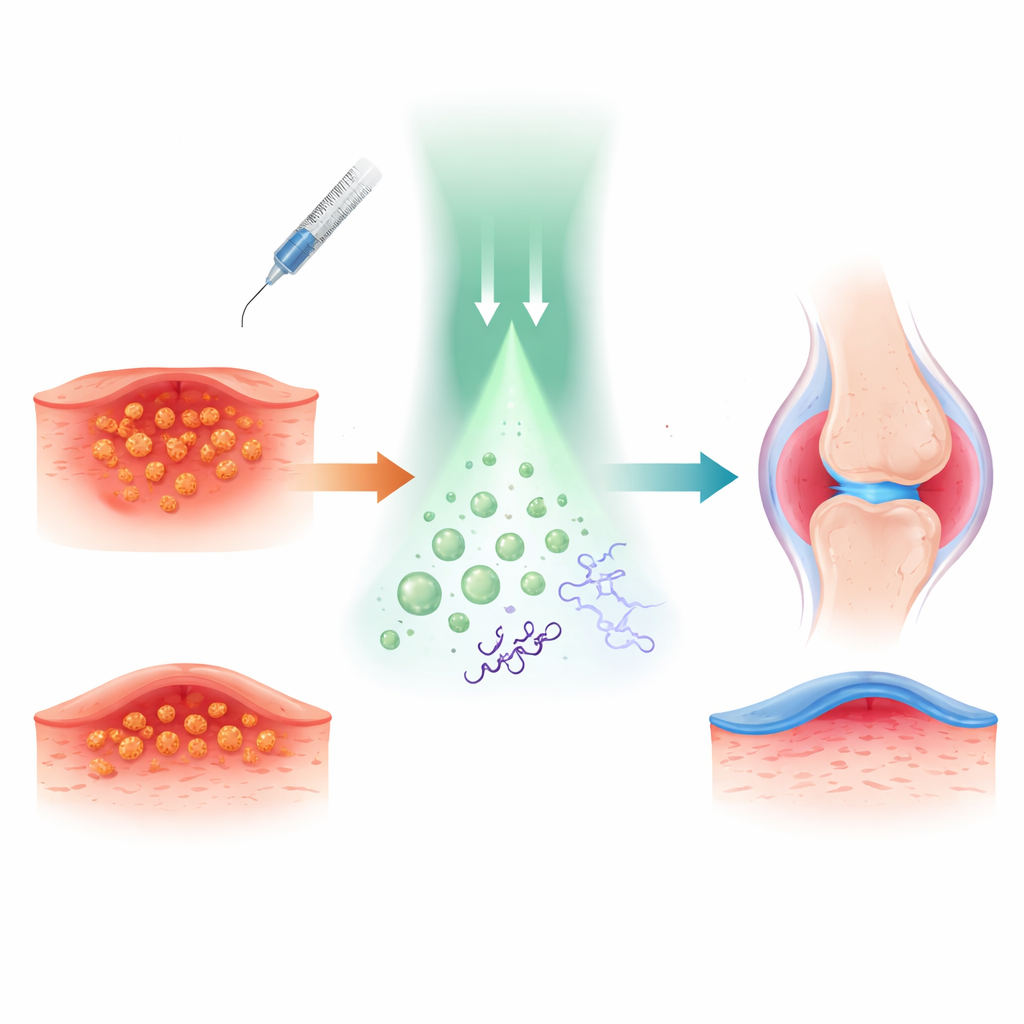
Encender el medicamento con luz suave
Para entender cómo funciona este interruptor luminoso, el equipo estudió la química en solución. Demostraron que un fotocatalizador a base de iridio puede transferir un electrón al TTC-NO cuando se ilumina con luz verde. Esto debilita un enlace específico, provocando la liberación del óxido nítrico y la restauración de la tetracaína a su forma activa. Mediciones mediante espectroscopía y cromatografía confirmaron que TTC-NO se convierte casi por completo en tetracaína y óxido nítrico bajo estas condiciones, mientras permanece esencialmente sin cambios en la oscuridad. Cuando los dos componentes se encapsularon en micelas, las partículas se mantuvieron estables, de unos 80 nanómetros de diámetro, y solo liberaron su contenido al irradiarse, demostrando que el concepto de “fármaco enjaulado” puede controlarse desde fuera del cuerpo con luz.
Ayudar a que las heridas infectadas sanen más rápido
El equipo continuó con ratones que presentaban heridas cutáneas deliberadamente infectadas con Staphylococcus aureus resistente a meticilina (MRSA), un patógeno problemático en hospitales. Algunas heridas recibieron tratamientos estándar como un antibiótico o un factor de crecimiento, mientras que otras fueron tratadas con las micelas de TTC-NO, con o sin luz. Cuando se encendió la luz, el sistema TTC-NO redujo drásticamente los recuentos bacterianos, calmó la inflamación, favoreció el crecimiento de nuevos vasos sanguíneos y aumentó la deposición de colágeno, todo lo cual es esencial para una reparación adecuada. Las heridas tratadas de esta manera cerraron más rápido y más completamente que las que recibieron solo tetracaína o micelas mantenidas en la oscuridad, y su rendimiento fue comparable al de un antibiótico de primera línea. De forma importante, las pruebas de seguridad no mostraron daños significativos en órganos ni en la química sanguínea.
Aliviar el dolor y silenciar las señales nerviosas
Puesto que la infección y la lesión tisular activan con fuerza las vías del dolor, los científicos midieron cuidadosamente los comportamientos relacionados con el dolor en el mismo modelo de heridas. La tetracaína tradicional aumentó brevemente la fuerza necesaria para provocar una respuesta dolorosa, pero su efecto desapareció en pocas horas. En contraste, las micelas de TTC-NO activadas por luz proporcionaron alivio hasta por 12 horas. Estudios microscópicos de los grupos de nervios cerca de la médula espinal y registros de actividad en la corteza sensorial del cerebro revelaron que el tratamiento combinado atenuó el disparo de las neuronas sensoriales del dolor mucho tiempo después de que la tetracaína pura hubiera perdido su efecto. Experimentos adicionales sugirieron que la mayor duración procede de la reducción de la carga bacteriana y de la inflamación por el óxido nítrico, no solo del entumecimiento de los nervios.
Proteger articulaciones dolorosas e infectadas
Los investigadores también probaron el sistema en ratones con artritis séptica, una infección grave por MRSA dentro de la articulación de la rodilla que provoca hinchazón, pérdida ósea y dolor intenso. Las micelas de TTC-NO activadas por luz redujeron la anchura de la articulación, disminuyeron el número de bacterias y protegieron la estructura ósea como se observó en escaneos de alta resolución. Los niveles de moléculas inflamatorias dañinas en la sangre cayeron, mientras que aumentaron moléculas de señalización protectoras. En términos de comportamiento, los ratones tratados toleraron una presión mecánica más intensa en la pata afectada y se movieron con más libertad en un área abierta, mostrando nuevamente un alivio de mayor duración que la tetracaína sola. Las mediciones en nervios y cerebro reflejaron estas mejoras conductuales, indicando una atenuación amplia de las vías del dolor sin toxicidad local o sistémica aparente. 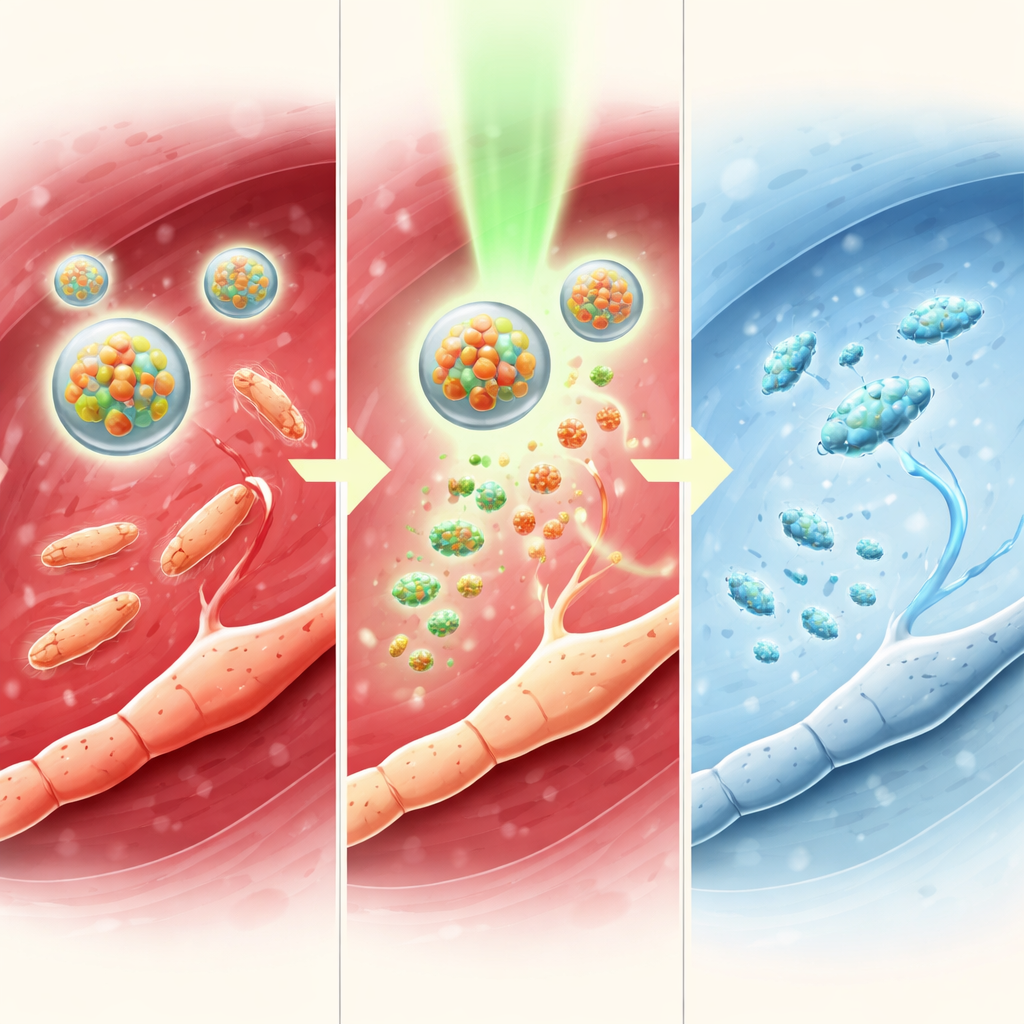
Qué podría significar esto para los pacientes
En conjunto, el trabajo demuestra un nanosistema único activado por luz que puede tanto eliminar infecciones bacterianas persistentes como reducir significativamente el dolor asociado. Al “enjaular” químicamente un anestésico dentro de una estructura liberadora de óxido nítrico y empaquetarlo en micelas, los autores logran una liberación localizada y a demanda de dos agentes útiles mediante luz visible suave. En modelos animales de heridas cutáneas e infecciones articulares, este diseño acelera la cicatrización y prolonga el alivio del dolor más allá de lo que puede ofrecer un anestésico local convencional. Aunque hacen falta muchas pruebas antes de su uso humano, el estudio subraya cómo los medicamentos inteligentes y conmutables podrían algún día hacer que los tratamientos de infecciones sean a la vez más eficaces y más confortables.
Cita: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Palabras clave: terapia con óxido nítrico, fármacos activados por luz, analgesia antibacteriana, nanomedicina, infecciones por MRSA